浅水湖泊藻源性湖泛以水体发黑、发臭为最显著的物理特征[1],并以此区别于正常湖体,是我国富营养化浅水湖泊面临的严重次生水环境灾害之一.自2007年由太湖湖泛造成无锡水危机以来,有关湖泛的特征[2-4]、发生过程[5-6]、可能的成因[7-8]及其环境影响[9-11]和防控措施[12-13]等方面均被重点研究.野外分析及室内模拟结果均表明:以二甲基硫醚类物质,如二甲基一硫醚(dimethyl sulfide,DMS)、二甲基二硫醚(dimethyl disulfide,DMDS)、二甲基三硫醚(dimethyl trisulfide,DMTS)和甲硫醇(methanethiol,MTL)等为代表的挥发性有机硫化物(volatile organic sulfur compounds,VOSCs)是造成湖泛水体发臭的主要嗅味物质[1-2];蓝藻等生源性物质的大规模死亡降解是嗅味物质产生的主要途径[1-2, 14-15].但有关湖泛水体呈现为黑色的原因以假设和推测居多[3, 7-8],缺乏足够的直接证据.然而,水柱呈现明显的黑色是湖泛水体区别于正常湖体的第一要素,水柱变黑与否是判断湖泛是否发生的最重要依据[5].因此,研究并分析湖泛水体显黑的原因,是科学解释湖泛现象的重要命题.
在自然状态下,河流、湖泊等原本非黑色地表水体发黑的原因主要有3种:其一,受污染水体在缺氧厌氧的环境下生成黑色金属硫化物而发黑,如美国Big Pit湖[16]和Lower Mystic湖[17];其二,土壤中腐殖质等深色或黑色有机颗粒物质受长期淋溶作用影响迁移进入水体而使河流、湖泊等变为棕褐直至黑色,如巴西亚马逊河流域的Lago Tupé湖[18]和印度尼西亚苏门答腊的Siak河[19];其三,由于某种原生动物或微型后生动物突然暴发而造成水体视觉上的黑色效应,如意大利的Garda湖[20].关于太湖等浅水湖泊藻源性湖泛水体变黑的原因,不同的研究人员提出不同的假设.有分析认为:厌氧还原态环境中形成的黑色表层沉积物在风浪扰动作用下进入水体,使得水体呈现黑色[7, 21].该假设的主要问题在于:湖泛发生时往往处于平静无风或微风等物理扰动微小的状态[8],不具备所谓底泥上翻的物理条件.另外一种观点认为:在湖泛缺氧厌氧的环境下,水环境中具备形成黑色金属硫化物的客观条件,水体中存在大量以黑色FeS为代表的金属硫化物可能是藻源性湖泛水体显黑的主要原因[3].然而,该观点建立在理论判断的基础上,缺乏足够的直接证据支撑.还有一种观点认为:湖泛水体中大量增加的有色可溶性有机物(CDOM)对光线有一定的吸收,并通过这种消光作用使得水体在表观上向暗色靠近[22],可能是湖泛水体呈现黑色的原因.然而,该观点无法解释野外和实验室观测到的湖泛黑色物质存在的问题.因此,浅水湖泊藻源性湖泛致黑的原因和机理均需要进一步探讨和明辨.
基于上述背景,本文以藻源性湖泛显黑颗粒物质为研究对象,结合一系列基于X-射线的分析技术对其进行鉴定与分析,以期获得浅水湖泊藻源性湖泛显黑颗粒物质的组分特征,并进一步分析其可能的致黑物质,为揭示湖泛致黑机理提供一定的理论补充.
1 实验设计与方法 1.1 实验设计由于藻源性湖泛在野外的发生具有时间和地点上的不确定性,难以及时发现和跟踪,因此本研究以室内模拟实验为基础,在成功模拟湖泛之后,分离湖泛水体中黑色颗粒物质,并进行相关的鉴定与分析.模拟实验在湖泊与环境国家重点实验室Y-型沉积物再悬浮发生模拟装置[23]中进行.该装置拥有6个可独立控制风浪等级的模拟柱,被成功用于湖泛发生[6]及消退[5]等过程的模拟与研究.模拟实验所需对象主要为沉积物、水样和藻类.选择藻源性湖泛易发区太湖月亮湾水域为采样点,利用重力式大口径沉积物采样器采集深度>20cm的原位沉积物柱状样若干,同时采集上覆水并装于25L聚乙烯桶中,并用浮游生物网现场采集水华蓝藻并妥善盛装,所有样品均于当天带回实验室并于24 h内在Y-型沉积物再悬浮发生模拟装置中进行湖泛模拟实验.实验设置对照和湖泛模拟两组处理,在每个模拟柱中底部装入20cm深带界面水的原位上层沉积物,其后无扰动注入原位湖水并控制水深达到与太湖实际水深相似的170cm,最后在湖泛模拟柱中添加47.5g(鲜重)经滤网过滤过的蓝藻(对照样不添加)进行模拟,所有实验控制条件和参数均参照文献[5-6]进行.
1.2 样品处理与分析待湖泛稳定发生后,采集上覆水水样,在厌氧手套箱中分别利用孔径为0.45 μm的玻璃纤维滤膜(whatman,GF/F)和中速定量滤膜对水体中颗粒物质进行拦截过滤,然后将过滤获得的滤膜连同膜上物质在真空状态下进行冷冻干燥处理.经冷冻干燥处理后的玻璃纤维滤膜及截留物在液氮环境下低温厌氧保存,用于物质形态及致黑敏感物质结合形态分析;干燥后的定量滤膜及膜上物质则保存在干燥器中,用于分析颗粒物质中主要元素含量.在本研究中,对照处理中截留的样品记为“对照”,湖泛处理中截留的样品记为“湖泛”.
对照及湖泛水体截留悬浮颗粒物质形态观察和分析利用场发射扫描电子显微镜(SEM,日立S-3000N)与X射线能谱仪(energy dispersive X-ray spectroscopy,EDS)联用技术即SEM-EDS进行,其中SEM用于形态观察,EDS用于微区元素相对含量分析.利用X-射线荧光光谱仪(X-ray fluorescence spectrometer,XRFS,ARL-9800)对悬浮颗粒物进行全量分析,以获得样品中主要主导元素成份及所占份额.此外,还利用X-射线光电子能谱技术(X-ray photoelectron spectroscopy,XPS,Thermo Fischer ESCALAB250)对颗粒物质中致黑敏感元素化学结合信息进行分析,进一步推导颗粒物中致黑物质的化学赋存形式.
2 结果与分析 2.1 显黑颗粒物SEM-EDS分析湖泊湖泛以水体发黑、发臭为最典型的特征,水体是否变为黑色是判断湖泛是否发生的依据[5-8, 13].本研究湖泛模拟成功后,截留湖泛水体上覆水颗粒物质如图 1所示.在真空抽滤之后,水体中不同粒径及来源的悬浮颗粒物质被富集在滤膜之上,与对照样相比,湖泛样品呈现明显的黑色.在SEM放大2000倍的情况下,对照和湖泛样品中均未发现原生动物和微型后生动物存在的证据. SEM-EDS元素含量分析结果如图 2和表 1所示.

|
图 1 湖泛水体截留颗粒物质图像(左边为对照样品,右边为湖泛样品) Fig.1 Photos of suspended particles of black bloom(left: check; right: black bloom) |

|
图 2 水体截留颗粒物质SEM-EDS分析((a)和(b)为对照样品,(c)和(d)为湖泛样品) Fig.2 SEM-EDS analysis of water trapped suspended particles ((a) and (b): check; (c) and (d): black bloom) |
| 表 1 颗粒物质SEM-EDS元素含量分析(At. %)* Tab.1 SEM-EDS element contents analysis of suspended particles |
图 2(a)为对照样品截留颗粒物致密区EDS微区分析,图 2(b)为对照样品粒状颗粒类物质EDS分析,结果表明两种不同类型微区元素均以C、O、Si为主.表 2显示其主要区别在于图 2(a)所示致密区C : O原子比约为2.47 : 1,图 2(b)所示粒状颗粒区约为0.38 : 1,且粒状颗粒区Si含量明显高于致密区.高C : O原子比表明相应区域C素主要以有机物形式存在,而二者又是其最主要的组成元素,因此该部分应以生物质分解物残体为主.对应地,低C : O原子比表明C素主要以无机形式存在,外加其较高的Si含量,因此可以认为粒状颗粒区应以悬浮无机颗粒为主.
| 表 2 水体悬浮颗粒物质XRFS全量分析(w %) Tab.2 XRFS analysis of suspended particles in the water |
图 2(c)和图 2(d)分别为湖泛样品截留颗粒物的EDS微区分析,其中图 2(c)为絮状物质区域、图 2(d)为致密区.湖泛样品两类不同类型截留颗粒物均以C、O元素为主,与对照样相比Si的比重下降较多,而Fe、S、Cu元素所占比例增加明显.湖泛样品截留颗粒物C : O比例较高,C素主要以有机物形式存在,外加C、O元素是其最主要组成元素(表 1),因此,湖泛样品颗粒物质以蓝藻等生物体分解物残体为主.值得注意的是,与对照样相比湖泛样品中Fe、S元素所占比例明显上升.考虑到FeS通常被认为是造成受污染自然水体发黑的主要物质[17],这意味着厌氧还原性环境下悬浮态或吸附于蓝藻等生物质或无机悬浮颗粒物上的黑色FeS沉淀,可能是造成湖泛水体视觉上发黑的重要原因.
2.2 水体悬浮颗粒物质XRFS分析对厌氧过滤真空冷冻干燥后的截留颗粒物质进行XRFS分析,获得其全量组分信息(表 2).烧除有机质后的湖泛样品及对照样品均以Si作为第一主要组成元素,Al、P、K、N等常量元素也占有一定的比例.值得注意的是,与黑色FeS相关的Fe、S两种元素,其相对含量在对照样品和湖泛样品中具有明显差异.
与对照样相比,湖泛样品中的Fe和S的含量明显更高.这说明除颗粒物质自身本底值外,湖泛样品颗粒物质上还汇集了外来Fe、S类物质.湖泛水体中具有不同价态含量较高的Fe、S类物质[1],这为水体黑色颗粒物中较高含量的Fe、S提供来源.其富集途径可能主要有二:其一,湖泛水体中相对丰富的离子态或胶体态Fe、S类物质直接吸附于悬浮颗粒物表面,使得湖泛黑色颗粒物中Fe和S含量升高;其二,湖泛厌氧水体中的Fe2+和ΣS2-通过化学共沉淀形成黑色FeS,该物质或自成颗粒悬浮于水体或吸附沉降在原有悬浮颗粒物质表面并使得颗粒物成为黑色FeS的载体,从而造成湖泛样品颗粒物中Fe和S含量升高.
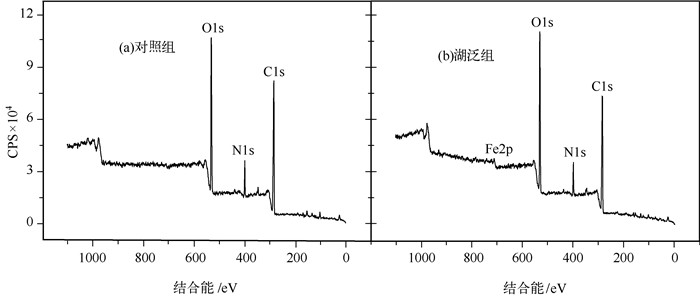
2.3 湖泛显黑悬浮颗粒物质XPS分析对截留获得的湖泛样品及对照样品颗粒物质分别进行XPS分析,结果如图 3及表 3所示.与对照样相比,湖泛样具有明显的Fe元素特征峰(图 3).主要元素相对含量分析结果进一步表明,颗粒物中元素组成以C、O、N、Si为主,Fe、S也占有一定的比例(表 3).两类样品中C : O原子比均较高,这与SEM-EDS分析得出的结果基本吻合.与对照样相比,湖泛水体颗粒物中Fe和S含量明显较高,二者分别比对照样高10.6倍和3.5倍.
| 表 3 水体悬浮颗粒物质元素组成XPS分析 Tab.3 XPS element contents analysis of suspended particles in the water |
|
图 3 湖泛水体悬浮颗粒物XPS图谱 Fig.3 XPS analysis of suspended particles in black bloom water |
在自然水体黑臭现象中,黑色FeS或金属硫化物被认为是很多受污染黑臭水体发黑的直接原因[17].通过一系列分析表明,在湖泛黑色颗粒截留物中Fe、S含量明显高于对照样.然而,这两种元素在自然界中赋存形态多样且化合形式复杂多变,尤其S元素具有丰富的化合价.因此,湖泛样品中Fe和S元素以及其它可形成黑色金属硫化物的元素以何种形式赋存,对湖泛黑色颗粒物显黑原因具有重要意义.为此,对颗粒物样品针对Hg、Pb、Mn、Fe、S等元素利用XPS进行特征峰微区分析.分析显示,Hg、Pb、Mn这3种元素含量低于可检出光子数,没有出现明显的特征峰,S和Fe含量较为丰富,特征峰明显.
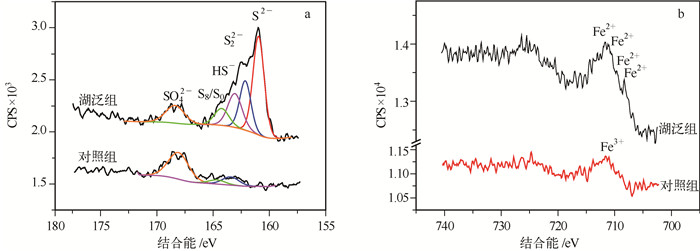
颗粒物中S元素XPS微区分析结果如图 4a所示.与对照样品相比,湖泛水体颗粒物样品中S含量更加丰富,其S 2p谱线具有更强的特征峰.分峰拟合之后可以清楚地看到,湖泛样品中S的赋存形式以还原态S为主,里面包含有S2-、S22-、HS-、S8、S0等一些列终端还原态或中间还原态产物.最强特征峰出现在结合能约为161.3 eV处,该处S元素主要以S2-化合态形式存在[24],这表明以硫化物形式存在的S2-在湖泛截留颗粒物S中占有最多的份额.由于除了Fe之外,并无足够的其它金属元素可以与S形成硫化物,因此,在湖泛样品中这部分S主要是以FeS的形式存在.形成鲜明对比的是,对照样中S的存在形式以SO42-为主,以还原态形式存在的S只占据很小的比例,基本可以忽略不计.
|
图 4 截留悬浮颗粒物S元素(a)和Fe元素(b)XPS微区分析 Fig.4 Detailed S (a) and Fe (b) XPS analysis of suspended particles |
颗粒物中Fe元素XPS微区分析结果如图 4b所示.湖泛样品与对照样颗粒物质Fe 2p能谱线具有相似的变化特征,均呈典型的马鞍形特征峰.由于Fe的化合物繁多,Fe 2p3/2轨道的电子具有非常多且间隔很小的峰位,因此对于来自自然环境中成分复杂的样品我们很难将其一一区分出.对XPS谱图分析后发现,湖泛样品在大约713.6、712.1、710.3 eV处有小的特征峰出现,根据数据库[25]资料对比发现,这些特征峰应该为FeS类物质,这与S元素微区分析结果相吻合.对照样品在大约713.3 eV附近出现较弱的Fe3+特征峰,对比数据库资料并结合该样品S元素微区分析结果,可以判定该样品中Fe与S主要以Fe2(SO4)3的方式赋存.
3 讨论湖泛黑臭水体的形成与湖泊富营养化紧密相关,与受污染黑臭河流等黑臭水体既具有一定的共性又存在明显差别.城市黑臭河道大多受居民生活用水和市政污水的影响,水体长期处于高生化需氧量、高化学需氧量和高有机负荷的状态,其水体发黑被认为主要是金属硫化物增加、有机质腐殖化以及污染底泥再悬浮共同造成的结果[19, 26-28].湖泛的发生与蓝藻的大规模暴发和积聚有关[1-10],在发生湖泛前水体处于富营养化湖泊的常规状态,其最终暴发是大型水体缺氧现象发展第4个阶段的必然结果.在该阶段,大量积聚的水华藻类死亡降解并引起水体和表层沉积物缺氧而形成还原性环境[29],水环境中Fe3+失去稳定存在的依据而不断被还原为Fe2+,同时硫酸盐还原菌(sulfate reducing bacteria,SRB)开始增殖并代谢还原高价态的SO42-而生成终端还原产物H2S[1, 26],给FeS致黑物质的形成提供了初始的物质条件.野外原位观测[1]和室内等比例模拟[13]均良好地印证了湖泛致黑物质物源基础的假设.
与野外实际情况相比,室内湖泛模拟实验尽量控制为理想条件,获得的湖泛水色更黑、臭味更强烈暨发生程度往往更深一些,湖泛体系组成也较野外实际情况简单,但却有利于湖泛致黑致臭机理研究.本研究湖泛水体黑色悬浮颗粒物SEM-EDS和XRFS分析结果表明:水柱黑色颗粒态物质表面Fe、S含量较高,其原子比通常接近1 : 1.在湖泛水体中,较高的Fe2+和ΣS2-含量是其水环境的重要化学特征之一[1].在湖泛这样的厌氧环境中,这类Fe、S物质极有可能通过化学共沉淀作用形成黑色FeS,其会以细微颗粒存在于水柱中、或者吸附于较大悬浮颗粒物之上,从而使得水体呈现视觉上的黑色. XPS分析进一步表明,在湖泛水体黑色悬浮颗粒物中,S主要以S2-硫化物的形式存在,Fe主要以Fe(Ⅱ)还原态硫化物FeS的形式存在.由于颗粒物质样品中并未出现除Fe以外的其它足够含量可与S2-形成黑色硫化物的金属元素,外加XPS分析结果显示Fe : S原子比基本为1 : 1,由此可以确定湖泛黑色悬浮颗粒物中Fe和S主要以FeS的化合形式存在.因此,综合多种分析认为:厌氧条件下形成的黑色FeS是引起湖泛水体发黑的重要原因,该类物质或悬浮于水柱或吸附在水体悬浮颗粒物质之上而广泛分布于湖泛水体,从而造成湖泛水体强烈的黑色视觉效应.
水柱中黑色颗粒物在湖体中稳定存在与否,指示了湖泛的发生、维持与消退.对于具有水深较深且存在水温季节性分层的大型水体,黑水或缺氧/厌氧层能稳定存在于从春季到秋季的较长时间尺度[14, 30].但对太湖湖泛野外调查跟踪结果显示,湖泛黑色水体持续时间从1 d到25 d不等[31],不同时间和地点发生的湖泛持续时间差异明显.公认的解释是:水体保持缺氧厌氧状态是黑色FeS类致黑物质稳定存在的前提与基础[16-17].一旦这种还原态环境状态被破坏,水柱中黑色FeS将被氧化消耗,从而使得湖泛黑色水体消失且水色回归正常.在自然湖体中,风浪扰动造成的水体复氧效应非常重要,在风浪持续作用下,水体复氧能力加强并造成湖泛水体从还原态环境向氧化态环境转化,使得湖泛水体FeS类致黑物质最终受氧化而消失,进而造成湖泛水体的恢复[5],是湖泛黑色水体消失的主要原因.相反,在水动力条件稳定的条件下,水体缺氧厌氧状态不易被打破,黑色FeS类物质在该条件下继续稳定存在,湖泛黑色水体得以保持[5].
4 结论在室内模拟藻源性湖泛的基础上,分离截留湖泛水体显黑颗粒物质,并借助SEM-EDS、XRFS、XPS等一系列基于X射线的分析手段,对湖泛样品显黑颗粒物质进行分析. SEM-EDS和XRFS分析结果显示,湖泛水体显黑颗粒物质以生物质残体和悬浮沉积物颗粒为主.与非湖泛对照样相比,其主要化学组分除C、N、O、Si外还含有含量较高的Fe、S. XPS分析进一步表明,湖泛颗粒中Fe、S主要以还原态形式存在,二者大量地以FeS的化合形式共存,这是湖泛水体颗粒物质呈现黑色的最主要原因.可以认为,在湖泊水体缺氧厌氧环境下,当氧化还原环境适宜时,水体中丰富的Fe2+和ΣS2-通过化学共沉淀作用化合成黑色FeS而广泛分布于水体和悬浮颗粒物中,从而造成湖泛的暴发和持续.然而,有关致黑物质反应物来源和迁移转化过程目前尚不清楚,还需进一步跟进研究,为科学解释湖泛发生机理及合理预控湖泛提供更深入的理论基础.
| [1] |
Shen QS, Zhou QL, Shang JG et al. Beyond hypoxia:Occurrence and characteristics of black blooms due to the decomposition of the submerged plant Potamogeton crispus in a shallow lake. Journal of Environmental Sciences, 2014, 26(2): 281-288. DOI:10.1016/S1001-0742(13)60452-0 |
| [2] |
Yang M, Yu JW, Li ZL et al. Taihu Lake not to blame for Wuxi's woes. Science, 2008, 319(5860): 158. |
| [3] |
刘国锋, 钟继承, 何俊等. 太湖竺山湾藻华黑水团沉积物中Fe-S-P的含量及其形态变化. 环境科学, 2009, 30(9): 2520-2526. |
| [4] |
中国科学院南京地理与湖泊研究所. 太湖梅梁湾2007年蓝藻水华形成及取水口污水团成因分析与应急措施建议. 湖泊科学, 2007, 19(4): 357-358. DOI:10.18307/2007.0401 |
| [5] |
申秋实, 邵世光, 王兆德等. 风浪条件下太湖藻源性"湖泛"的消退及其水体恢复进程. 科学通报, 2012, 57(12): 1060-1066. |
| [6] |
申秋实, 邵世光, 王兆德等. 太湖月亮湾湖泛发生过程模拟及水土物化性质的响应. 水科学进展, 2011, 22(5): 710-719. |
| [7] |
陆桂华, 马倩. 太湖水域"湖泛"及其成因研究. 水科学进展, 2009, 20(3): 438-442. |
| [8] |
陈荷生. 太湖宜兴近岸水域"湖泛"现象初析. 水利水电科技进展, 2011, 31(4): 33-37. DOI:10.3880/j.issn.1006-7647.2011.04.007 |
| [9] |
刘国锋, 申秋实, 张雷等. 藻源性黑水团环境效应:对水沉积物界面氮磷变化的驱动作用. 环境科学, 2010, 31(12): 2917-2924. |
| [10] |
刘国锋, 何俊, 范成新等. 藻源性黑水团环境效应:对水沉积物界面处Fe、Mn、S循环影响. 环境科学, 2010, 31(11): 2652-2660. |
| [11] |
申秋实, 周麒麟, 邵世光等. 太湖草源性"湖泛"水域沉积物营养盐释放估算. 湖泊科学, 2014, 26(2): 177-184. DOI:10.18307/2014.0202 |
| [12] |
He W, Shang JG, Lu X et al. Effects of sludge dredging on the prevention and control of algae-caused black bloom in Taihu Lake, China. Journal of Environmental Sciences, 2013, 25(3): 430-440. DOI:10.1016/S1001-0742(12)60098-9 |
| [13] |
Shen QS, Liu C, Zhou QL et al. Effects of physical and chemical characteristics of surface sediments in the formation of shallow lake algae-induced black bloom. Journal of Environmental Sciences, 2013, 25(12): 2353-2360. DOI:10.1016/S1001-0742(12)60325-8 |
| [14] |
Lu X, Fan CX, Shang JG et al. Headspace soli-phase microextraction for the determination of volatile sulfur compounds in odorous hyper-eutrophic freshwater lakes using gas chromatography with flame photometric detection. Microchemical Journal, 2012, 104: 26-32. DOI:10.1016/j.microc.2012.04.001 |
| [15] |
卢信, 冯紫燕, 商景阁等. 不同有机质诱发的水体黑臭及主要致臭物(VOSCs)产生机制研究. 环境科学, 2012, 33(9): 3152-3159. |
| [16] |
Stahl JB. Black water and 2 peculiar types of stratification in an organically loaded strip-mine lake. Water Research, 1979, 13(5): 467-471. DOI:10.1016/0043-1354(79)90040-X |
| [17] |
Duval B, Ludlam SD. The black water chemocline of meromictic Lower Mystic Lake, Massachusetts, USA. International Review of Hydrobiologia, 2001, 86(2): 165-181. DOI:10.1002/(ISSN)1522-2632 |
| [18] |
Rai H, Hill G. Physical and chemical studies of lago tupe a central amazonian black water ria lake. Internationale Revue Der Gesamten Hydrobiologie, 1981, 66(1): 37-82. DOI:10.1002/(ISSN)1522-2632 |
| [19] |
Rixen T, Baum A, Pohlmann T et al. The Siak, a tropical black water river in central Sumatra on the verge of anoxia. Biogeochemistry, 2008, 90(2): 129-140. DOI:10.1007/s10533-008-9239-y |
| [20] |
Pucciarelli S, Buonanno F, Pellegrini G et al. Biomonitoring of Lake Garda:Identification of ciliate species and symbiotic algae responsible for the "black-spot" bloom during the summer of 2004. Environmental Research, 2008, 107(2): 194-200. DOI:10.1016/j.envres.2008.02.001 |
| [21] |
王成林, 张咏, 张宁红等. 太湖藻源性"湖泛"形成机制的气象因素分析. 环境科学, 2011, 32(2): 401-408. |
| [22] |
Duan HT, Ma RH, Loiselle SA et al. Optical characterization of black water blooms in eutrophic waters. Science of the Total Environment, 2014, 482: 174-183. |
| [23] |
范成新. 一种室内模拟水下沉积物再悬浮状态的方法及装置: 中国, 200410014329. X[P]. 2005-01-12.
|
| [24] |
Shchukarev A, Galman V, Rydberg J et al. Speciation of iron and sulphur in seasonal layers of varved lake sediment:an XPS study. Surface and Interface Analysis, 2008, 40(3/4): 354-357. |
| [25] |
National Institute of Standards and Technology. NIST X-ray Photoelectron Spectroscopy Database 20, Version 4. 1. In http://srdata.nist.gov/xps/, 2012.
|
| [26] |
钱嫦萍, 王启东, 陈振楼等. 生物修复技术在黑臭河道治理中的应用. 水处理技术, 2009, 35(4): 13-17. |
| [27] |
雷恒毅, 余光伟, 刘立光等. 珠江流域中污染感潮河道黑臭治理新技术. 中山大学学报:自然科学版, 2007, 46(3): 134-136. |
| [28] |
钱嫦萍, 陈振楼, 王启东. 城市河流黑臭的原因分析及生态危害. 城市环境, 2002, 16(3): 21-23. |
| [29] |
Diaz RJ, Rosenberg R. Spreading dead zones and consequences for marine ecosystems. Science, 2008, 321(5891): 926-929. DOI:10.1126/science.1156401 |
| [30] |
Turner RE, Rabalais NN, Swenson EM et al. Summer hypoxia in the northern Gulf of Mexico and its prediction from 1978 to 1995. Marine Environmental Research, 2005, 59(1): 65-77. DOI:10.1016/j.marenvres.2003.09.002 |
| [31] |
陆桂华, 马倩. 2009年太湖水域"湖泛"监测与分析. 湖泊科学, 2010, 22(4): 481-487. |
 2015, Vol. 27
2015, Vol. 27 

