双酚A(Bisphenol A,BPA)是一种重要的化工原料,主要用于生产环氧树脂、聚碳酸脂等多种高分子材料,也用于生产增塑剂、阻燃剂、抗氧剂、热稳定剂、涂料等精细化工产品.BPA产量及用量随着社会发展而大量增加的同时[1],不可避免造成严重的环境污染.研究发现,BPA可明显增加动物乳腺癌、卵巢癌、前列腺癌、白血病等癌症的发生[2-4],具有一定的胚胎毒性和致畸性[5],且能导致动物性早熟、精子数目下降等[6].多项研究表明,在人类血清、尿液、羊水、乳汁内均可检测到BPA[7-8].尽管BPA在环境中有较快的降解速率,但随着大量BPA进入环境,研究BPA在环境相中的迁移转化行为对预测其变化趋势和预防其引发的环境污染具有重要意义,也可为区域风险评估提供基础数据.
Mackay[9]提出的逸度模型被广泛地应用于有机物归趋行为的模拟和预测.如董继元等[10-11]和田慧等[12]运用逸度模型模拟稳态条件下兰州区域DDT、PAHs和硫丹的多介质环境归趋行为,指出其主要储库为土壤和沉积物,此外还有苯并(a)芘等的迁移归趋研究[13].此前本实验室已对滇池水域BPA污染状况进行监测分析[14],然而短期而低频的监测并不能体现出BPA污染状况的变化趋势.对滇池水域BPA污染状况进行模拟可以掌握其迁移转化趋势并预测污染状况的变化,但运用四级逸度模型模拟BPA在特定区域环境相中归趋行为的相关研究还未见报道.四级逸度模型建立在非稳态非平衡条件下,直观地表现出有机物的动态归趋变化.因而本文选用四级逸度模型,以滇池为研究区域,在模拟输入的情况下,计算得到各环境相对BPA的容纳能力及估算含量,研究BPA在滇池水域的动态归趋以及影响归趋行为的主要参数,对滇池水域的生态保护以及评价环境内分泌干扰物的环境生态风险具有重要意义.
1 研究方法 1.1 研究区域概况滇池地处云贵高原中部,属长江流域金沙江水系,为断陷构造湖泊,是云贵高原上最大的淡水湖泊.流域面积约2920 km2,山地居多,水域面积约300 km2,平均水深约4.6 m,主要入滇河流有22条.滇池流域属于特殊的高原型亚热带季风气候,流域多年平均气温为15℃,平均降雨量为1000 mm,其中80%集中于5-10月.流域内共有乡镇企业7000多家,自1980s以来,其年增长速度约为40%.由于城市经济和流域工业的快速发展,1980s初滇池水体逐渐被污染,1990s迅速恶化,整个滇池水体处于富营养化状态,底泥也呈现出厌氧状态.1990s后期由于滇池水质污染严重,被纳入国家重点治理的3大湖泊之一.
1.2 模型框架逸度(fugacity)概念常作为热力学平衡的判断标准[15].本研究以Mackay[9]的多介质逸度模型为基础,结合滇池水域构建四级多介质环境归趋模型.在本研究所计算的四级逸度模型中,因BPA主要存在于水相和沉积物相,而大气相中含量较小,BPA通过雨水冲刷等方式进入水体是单向过程,水体的BPA很难通过分子扩散等方式进入周边土壤,故本模型主要研究BPA在滇池水域的环境行为及其主要影响因子,所涉及的环境主相主要包括水相、表层沉积物相(0~5 cm)和中层沉积物相(5~10 cm),而各个主相又包括水相和固相.因滇池水体中的鱼类总量自1980年以来急剧下降[16],尽管后来有所保护,但通过计算发现,滇池鱼类对BPA的富集影响相对较小[17],故本研究没有考虑水体鱼类.本研究根据滇池环境恶化状态[16]及我国BPA使用情况[18],设计模拟时间段定为1991-2011年.各环境相中营养盐浓度C(mol/m3)为逸度f(Pa)和逸度容量Z(mol/(m3·Pa))的乘积,即Ci=fi·Zi.营养盐在各环境相中的迁移通量T(mol/h)为逸度f和迁移速率D(mol/(h·Pa))的乘积,即Tij=fi·Dij,降解通量TR(mol/h)为营养盐在各环境相中的迁移通量,为逸度f和降解速率DR(mol/(h·Pa))的乘积,即TRi=fi·DRi.其中Z、D和DR的计算方法详见文献[12, 19-20].
模型假设营养盐在各环境相间处于非稳态非平衡状态,并据质量守恒定律,建立质量平衡微分方程组,则四级逸度模型转化为一系列微分方程组构成的数学表达式.各环境主相中的质量平衡方程为:
| $ 水相:{V_W} \cdot {Z_W} \cdot \frac{{{\rm{d}}{f_W}}}{{{\rm{d}}t}} = {Q_{_{{\rm{0W}}}}} + {D_{{\rm{AW}}}} \cdot {f_{\rm{A}}} + \\{D_{{\rm{S1W}}}} \cdot {f_{{\rm{S1}}}}-({D_{{\rm{WA}}}} + {D_{{\rm{WS1}}}} + {D_{{\rm{RW}}}} + {D_{{\rm{W0}}}}) \cdot {f_{\rm{W}}} $ | (1) |
| $ 表层沉积物相:{V_{{\rm{S1}}}} \cdot {Z_{{\rm{S1}}}} \cdot \frac{{{\rm{d}}{f_{{\rm{S1}}}}}}{{{\rm{d}}t}} = {D_{{\rm{WS1}}}} \cdot {f_{\rm{W}}} + \\{D_{{\rm{S2S1}}}} \cdot {f_{{\rm{S2}}}}-({D_{{\rm{S1S2}}}} + {D_{{\rm{S1W}}}} + {D_{{\rm{RS1}}}}) \cdot {f_{{\rm{S1}}}} $ | (2) |
| $ 中层沉积物相:{V_{{\rm{S2}}}} \cdot {Z_{{\rm{S2}}}} \cdot \frac{{{\rm{d}}{f_{{\rm{S2}}}}}}{{{\rm{d}}t}} = {D_{{\rm{S1S2}}}}\cdot{f_{{\rm{S1}}}}-({D_{{\rm{S20}}}} + {D_{{\rm{S2S1}}}} + {D_{{\rm{RS2}}}})\cdot{f_{{\rm{S2}}}} $ | (3) |
式中,VW、VS1、VS2分别表示滇池水相、表层沉积物相、中层沉积物相的体积(m3),ZW、ZS1、ZS2分别表示滇池水相、表层沉积物相、中层沉积物相的总逸度容量(mol/(m3·Pa)),fW、fS1、fS2分别表示滇池水相、表层沉积物相、中层沉积物相的逸度(Pa),DAW、DWA、DS1W、DWS1、DS1S2、DS2S1、DW0、DS20分别表示气相到水相、水相到气相、表层沉积物相到水相、水相到表层沉积物相、表层沉积物相到中层沉积物相、中层沉积物相到表层沉积物相、水相到出水去除、中层沉积物相到底层沉积物相的环境过程迁移速率(mol/(h·Pa)),DRW、DRS1、DRS2分别表示BPA在水相、表层沉积物相、中层沉积物相中的降解速率(mol/(h·Pa)).
1.3 过程和参数识别BPA在研究区域内迁移交换过程包括:污染物的平流输入、输出,污染源的排放,污染物在各环境介质间的迁移,相内的降解反应等.本研究共收集两组数据,一组为模型输入参数,包括BPA理化性质及降解速率常数(表 1)、迁移转化参数[21]、滇池流域环境属性参数(表 2);另一组数据为滇池流域BPA实测浓度值,用于模拟结果验证.本研究中,关于云南地区的BPA用量以及排放量数据均缺乏,故根据全国BPA使用量和2010年滇池部分入流量来估算BPA在滇池的排放趋势[17, 22].由于滇池表层沉积物相处于厌氧状态,而BPA在沉积物相中的降解主要依靠好氧微生物,所以本研究以表层沉积物相中固相部分BPA的降解速率为零,水子相部分降解速率与水相一致计,中层沉积物相中以完全没有降解计.为保证模拟结果的精度,尽可能收集较多文献数据,根据所得参数值的分布类型计算参数均值.
1.4 模型求解与验证用Matlab编程解上述微分方程,以各参数均值及BPA排放数据为模型输入数据,计算得到BPA的浓度和迁移通量数据,并将计算所得浓度与不同时段实测浓度数据进行对比验证.对模型可靠性验证的实测值,本研究通过实验室所测得的2010年BPA在滇池水相、表层沉积物相、中层沉积物相中的浓度来验证模型.为确定对研究区域BPA环境行为有重要影响的过程和参数,还对输入参数进行灵敏度分析.
2 结果与讨论 2.1 滇池中BPA的输入量BPA主要通过入滇河流、雨水冲刷、大气沉降和雨水溶解方式进入滇池.因缺乏相关资料,本文根据1996-2002年[18]、2005年[22]全国BPA及其下游产品的生产量和进口量以及相关资料估算滇池水域在1991-2011年间对BPA的纳污量.具体估算参数如下:滇池流域BPA实际使用量与全国BPA及其下游产品的实际使用量比值以滇池流域面积所占全国面积比例计;而形成污染物排放到环境中的BPA浓度以BPA及其下游产品总量的10%计[33];污染物BPA可进入水体、土壤等环境,且BPA在进入污水处理厂沿途会消耗降解,故本研究假定修正系数为0.3;经滇池流域各污水处理厂处理之后,BPA残留率为20%[14].
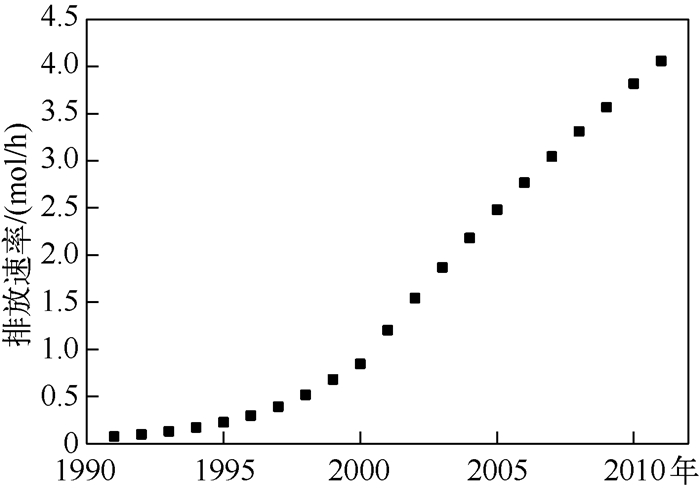
全国BPA及其下游产品的实际使用量包括BPA的表观消费量(约占26.3%)、下游产品环氧树脂和聚碳酸树脂的净进口量(约占73.7%)两部分[18].因相应文献中只有1996-2002年全国BPA及其下游产品的生产量和进口量资料,故本研究参考李小平[22]对2005和2010年BPA的表观消费量的预测信息,假设1991-1999年的BPA及其下游产品消费总量符合文献[22]中1996-1999年的增长趋势,而之后符合2000-2002年的增长趋势.1991-2011年间估算所得滇池BPA排放速率如图 1所示.
|
图 1 滇池水域1991-2011年BPA排放速率 Fig.1 The input rate of BPA to Lake Dianchi during 1991-2011 |
根据环境属性参数和BPA的理化性质参数,计算各环境相对BPA的容纳能力,即Z值,计算结果如表 3所示.滇池水体中,各环境主相中的逸度容纳能力表现为:中层沉积物相(Z=1.09×109 mol/(m3·Pa))>表层沉积物相(Z=5.50×108 mol/(m3·Pa))>水相(Z=1.42×105 mol/(m3·Pa)).而各环境子相逸度容量值比较,固相(2.06×106~2.78×109 mol/(m3·Pa))>水相(1.42×105 mol/(m3·Pa))>气相(4.18×10-4 mol/(m3·Pa)).逸度容量值主要受污染物的有机碳分配系数、环境相有机碳含量和固相体积比的影响,所以BPA在固相中的Z值最大.尽管表层沉积物相中有机碳含量略高于中层沉积物相,但中层沉积物相中固相含量高,所以其Z值大于表层沉积物相.与水相和沉积物相比,气相的Z值较低,这与气相中颗粒物含量低,对BPA容纳能力不高相一致.
| 表 3 滇池逸度容量值 Tab.3 Z values of BPA in Lake Dianchi |
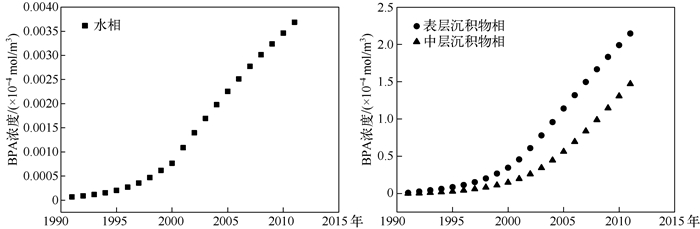
BPA在表层沉积物相中浓度最高,其次为中层沉积物相,水相中浓度最低.以2010年为例,表层沉积物相、中层沉积物相、水相中BPA浓度分别为1.99×10-4、1.31×10-4、3.50×10-7 mol/m3,表层沉积物相的BPA浓度约为中层沉积物相浓度的1.5倍,为水相浓度的575倍.这主要是因为BPA有较大的有机碳分配系数,其浓度与有机质浓度呈正比,且沉积物相对BPA的容纳能力远高于水相,使得BPA在水相中浓度远低于沉积物相.尽管中层沉积物相对BPA的容纳能力强于表层沉积物相,但由于水相中BPA持续迁移至表层沉积物相中,同时BPA在沉积物相中的迁移能力不强,且中层沉积物相BPA浓度受表层沉积物相控制,故中层沉积物相中BPA浓度略低于表层沉积物相.1991-2011年滇池各环境相中的BPA浓度逐年增加,但变化趋势有差别.在水相中1996年之前,受BPA排放量的影响,其浓度变化较缓慢,但1996年之后,由于BPA的广泛应用,BPA浓度增加趋势变强,但在2008年之后,随着BPA的使用方式达到饱和,BPA浓度的增加趋势开始变缓.而表层沉积物相中的变化趋势较水相推迟几年,在1998年之前变化趋势较缓,之后就呈现出较快的增长趋势.而在中层沉积物相中,2000年以前BPA浓度增加较缓慢,2000年之后则一直维持较快的增长趋势.总体来说,BPA浓度变化趋势表现为中层沉积物相滞后于表层沉积物相,表层沉积物相滞后于水相(图 2).
|
图 2 1991-2011年BPA在滇池不同环境相中的浓度变化趋势 Fig.2 The concentrations of BPA in different compartments of Lake Dianchi during 1991-2011 |
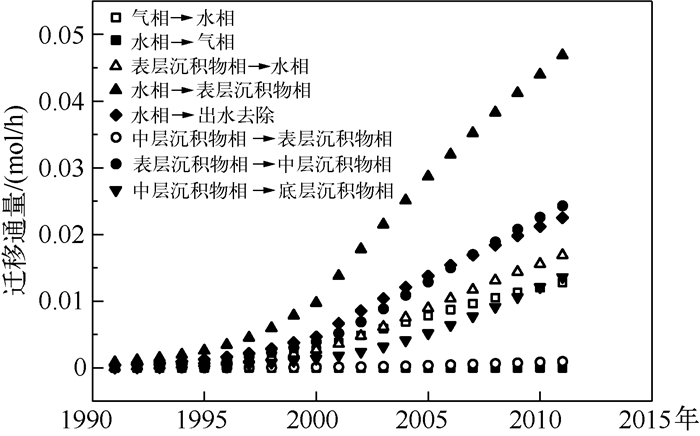
1991-2011年BPA在各相间的迁移通量变化趋势表明,随着时间的推移,各相间的迁移通量都呈现出增加的趋势(图 3).由于迁移通量和浓度计算均是基于逸度,故BPA在相间的迁移通量随时间的变化趋势与其浓度趋势相似.不同相间迁移过程中,水相→表层沉积物相的迁移通量最大.其次是表层沉积物相→中层沉积物相、水相→出水去除两个迁移过程,且这两个过程的迁移通量大小为:2007年之前,水相→出水去除迁移通量高于表层沉积物相→中层沉积物相,而2007年之后,则为表层沉积物相→中层沉积物相的迁移通量略大.这是因为随着时间的推移,沉积物相中BPA浓度逐渐增加,而表层沉积物相中BPA浓度增加速率大于水相中浓度增加速率,使得BPA由表层沉积物相进入中层沉积物相的推动力强于水相.在表层沉积物相→水相、中层沉积物相→底层沉积物相两个迁移过程中,前者的迁移通量大于后者,且迁移通量增加速率相似.而气相到水相的迁移通量增加速率则低于表层沉积物相→水相和中层沉积物相→底层沉积物相迁移过程,所以尽管最初气相→水相迁移通量大于另外两个迁移过程,但2010年之后,其迁移通量呈现出低于表层沉积物相→水相和中层沉积物相→底层沉积物迁移过程.在8个相间迁移过程中,中层沉积物相→表层沉积物相和水相→气相过程迁移通量值最小,相对其他迁移过程,其值可忽略.
|
图 3 滇池中BPA在1991-2011年间的迁移通量 Fig.3 Transfer fluxes of BPA among different compartments of Lake Dianchi during 1991-2011 |
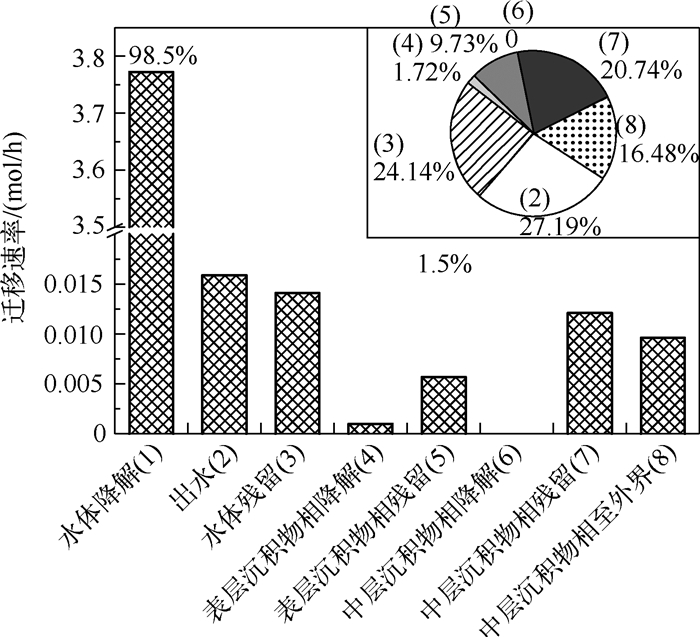
以2010年为例,滇池水域中BPA在水相至表层沉积物过程迁移通量为4.41×10-2mol/h,表层沉积物相至中层沉积物相迁移通量为2.27×10-2 mol/h,平流输出为2.14×10-2 mol/h,以上3个环境过程为BPA在滇池水域的主要迁移过程.其余各环境过程的迁移通量如下:表层沉积物相至水相迁移通量为1.57×10-2 mol/h,中层沉积物相至底层沉积物相为1.22×10-2 mol/h,气相至水相为1.19×10-2 mol/h,中层沉积物相至表层沉积物相为1.08×10-3 mol/h,水相至气相为2.70× 10-4 mol/h(图 3).BPA在不同环境过程的分配比例(图 4)结果表明,进入滇池的BPA主要通过水体降解去除,约占入滇总量的98.5%,是BPA的主要去除过程,而少量余下的BPA中平流输出和水体残留占51.33%,其余部分进入沉积物相,沉积物相中表层沉积物相中BPA的量高于中层沉积物相.
|
图 4 2010年滇池中BPA在不同环境过程的分配 Fig.4 The distribution of BPA in different environment processes in Lake Dianchi in 2010 |
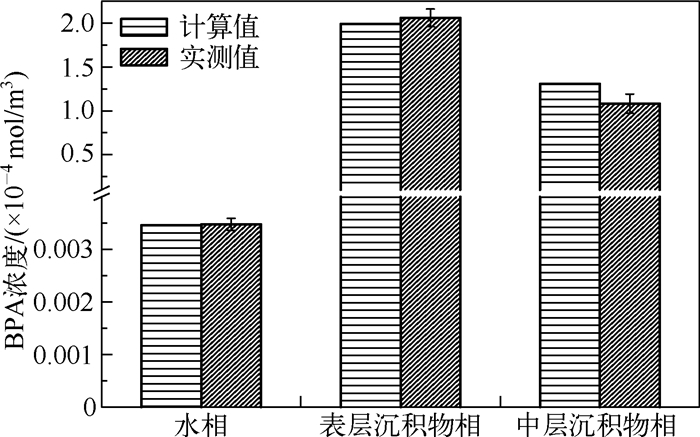
本研究以2010年7月和12月滇池水相、表层沉积物相和中层沉积物相6个国控采样点中的BPA浓度[14]均值为实测值,与计算所得的各相浓度进行对比验证,结果如图 5所示.在水相中,BPA浓度计算值与实测值吻合较好,其偏差小于0.6%;表层沉积物相中,计算浓度值约为实测值的96.6%,而中层沉积物相中的计算浓度值则约为实测值的120%.在水相模拟值偏差较小的情况下,表层沉积物相有3.4%的模拟值负偏差,而中层沉积物相中模拟值正偏差达20%.主要原因可能是:(1)模型假定表层沉积物相中固相部分没有BPA降解,而间隙水相中部分BPA降解速率与水相主相一致,但由于滇池表层沉积物相处于厌氧状态,其水子相中BPA的降解并不能与水相中降解速率完全一致,使得表层沉积物相计算浓度略低于实测值;(2)中层沉积物相中,研究假设BPA没有降解,但滇池部分污染较轻的区域中层沉积物相中BPA有部分降解;(3)参数的不确定性,模型中大部分参数来源于相关文献,而不是滇池实测值.尽管计算结果有偏差,但BPA浓度在3个环境相中的验证结果仍在合理的精度范围.
|
图 5 2010年滇池BPA实测值与计算值比较 Fig.5 Comparison between calculated and measured concentrations of BPA of Lake Dianchi in 2010 |
运用灵敏度分析评估模型输入参数的变化对计算值的影响,确定对模型计算结果影响较大的参数.本研究对参数灵敏度的分析采用Cao等[34]所使用的方法.不同参数间的灵敏度系数比较,引入综合灵敏度系数CS,该值近似等于变化因子为1时的参数灵敏度系数,其公式为:
| $ CS = ({C_{{\rm{F1}}{\rm{.1}}}}-{C_{{\rm{F0}}{\rm{.9}}}})/(0.2 \times {C_{{\rm{F1}}{\rm{.0}}}}) = ({C_{{\rm{SF1}}{\rm{.1}}}}-{C_{{\rm{SF0}}{\rm{.9}}}})/2 $ | (4) |
式中,参数CF0.9、CF1.0和CF1.1分别为当输入参数乘以变化因子0.9、1.0和1.1时所对应的计算浓度,CSF0.9和CSF1.1分别为当输入参数乘以变化因子0.9和1.1时所对应的灵敏度.
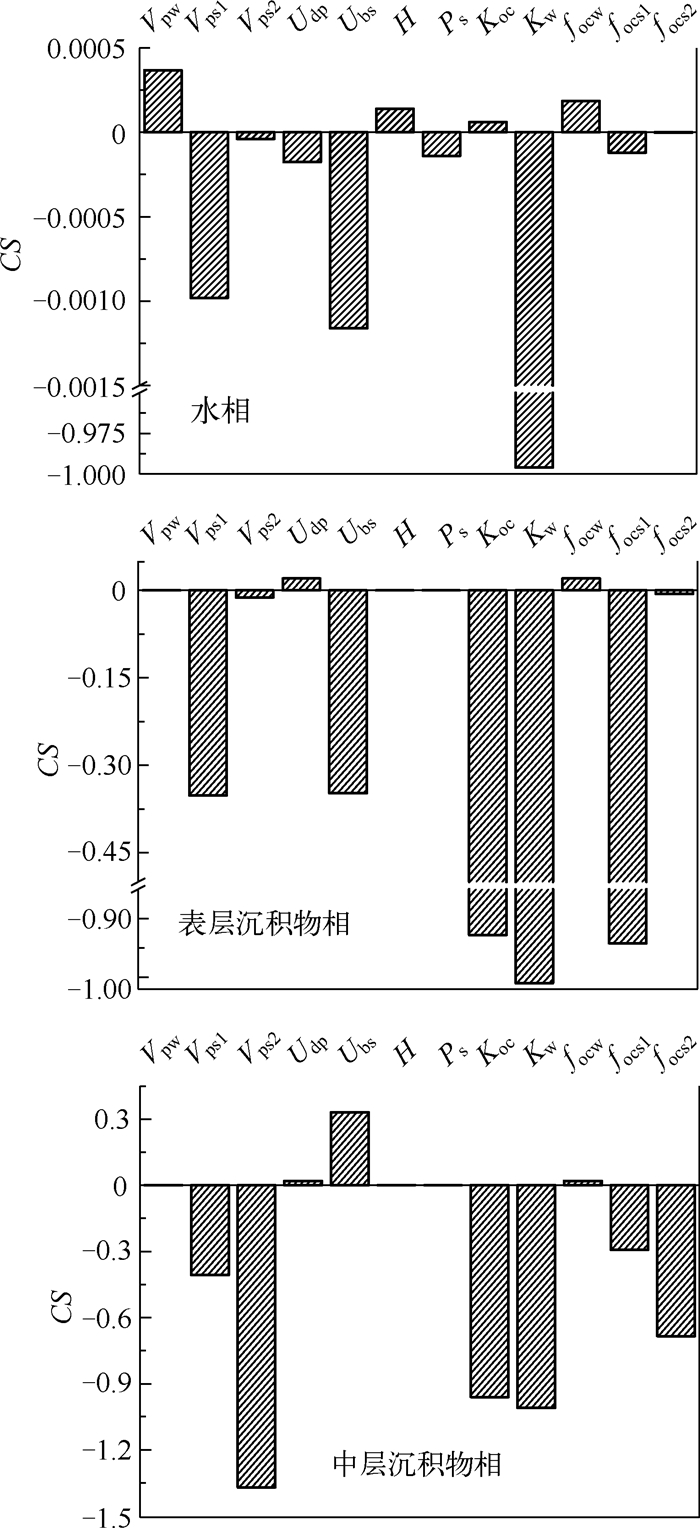
本研究主要选择以下参数进行灵敏度分析:Vpw、Vps1、Vps2、Kw、沉积物相中BPA的埋葬速率(Udp)、水相中固相的沉降速率(Ubs)、H、PS、Koc、focw、focs1、focs2.图 6为BPA在各相中的灵敏度系数分数,值的正负代表相应参数对某相浓度的增大或减小作用.
|
图 6 滇池不同环境相中关键参数灵敏度 Fig.6 The values of CS in different compartments of Lake Dianchi |
水相中,除Kw灵敏度值较大为-1.0,其余参数对BPA在水相的浓度影响很小(图 6),说明水相中BPA降解速率变化会引起BPA在水相的浓度呈相同比例变化,这与入滇BPA主要依靠水体降解这一途径去除相一致.对所选择参数,Vpw、H、Koc、focw的增大会引起BPA在水相中浓度的增大;相反,其余8个参数值的增大会引起BPA在水相中浓度的降低.表层沉积物中各参数灵敏度系数绝对值之和大于水相中对应值,说明表层沉积物相BPA浓度受各参数整体影响大于水相所受影响.表层沉积物相中,除Udp和focw外,其余参数的增大对污染物都表现出降低作用.Kw、focs1、Koc灵敏度值较大,分别为-1.10、-0.95、-0.90,这说明水相中BPA降解速率变化会引起BPA在水相的浓度进而影响表层沉积物相中浓度,由于BPA的有机碳分配系数相对较大,因而focs1、Koc变化对模型的计算有较大影响.其次为参数Vps1、Ubs,其余参数变化对表层沉积物相BPA浓度影响较低,可忽略.3个环境相中,中层沉积物相BPA浓度受各参数整体影响最大.中层沉积物相中,参数Udp、Ubs、H、focw的增大会引起BPA浓度的增大,余下参数的增大则会引起浓度降低.这一结果意味着如果同比例增大所选参数值,中层沉积物相中BPA浓度的降低值会远高于增大值.
3 结论1) 本研究模拟滇池区域BPA在各环境介质中的浓度水平、相间迁移和环境归趋行为.模拟结果表明:入滇总量98%的BPA主要通过水体降解去除,滇池出水去除量和水体残留量共约占1%,余下部分进入沉积物相.沉积物相是残留BPA最主要的汇,其中,表层沉积物相中BPA浓度最高,3相中浓度变化趋势受外界输入影响较大.
2) 不同相间的迁移过程中,水相→表层沉积物相的迁移是主要迁移过程,其次是表层沉积物相→中层沉积物相、水相→出水去除两个迁移过程,迁移通量分别为4.41×10-2、2.27×10-2、2.14×10-2 mol/h.
3) 灵敏度分析结果指出,BPA在水相中的降解速率、有机碳分配系数、有机碳含量、固相体积比等参数灵敏度系数较大,对模型影响比较显著.模型验证结果指出,模拟浓度与实测浓度吻合较好,表明建立的四级多介质逸度模型适用于滇池流域BPA的环境多介质迁移及归趋行为模拟.
| [1] |
Vandenberg LN, Maffini MV, Sonnenschein C et al. Bisphenol A and the great divide: a review of controversies in the field of endocrine disruption. Endocrine Reviews, 2009, 30: 75-95. DOI:10.1210/er.2008-0021 |
| [2] |
Van Waeleghem K, De Clercq N, Vermeulen L et al. Deterioration of sperm quality in young healthy Belgian men. Human Reproduction, 1996, 11: 325-329. DOI:10.1093/HUMREP/11.2.325 |
| [3] |
Grasselli F, Baratta L, Baioni L et al. Bisphenol A disrupts granulosa cell function. Domestic Animal Endocrinology, 2010, 39(1): 34-39. DOI:10.1016/j.domaniend.2010.01.004 |
| [4] |
Wang J, Liu X, Wang H et al. Expression of two cytochrome P450 aromatase genes isregulated by endocrine disrupting chemicals in rare minnow Gobiocypris rarus juveniles. Comparative Biochemistry and Physiology C: Pharmacology Toxicology and Endocrinology, 2010, 152(3): 313-320. DOI:10.1016/j.cbpc.2010.05.007 |
| [5] |
Wang XC, Dong QX, Chen YH et al. Bisphenol A affects axonal growth, musculature and motor behavior in developing zebrafish. Aquatic Toxicology, 2013, 142: 104-113. |
| [6] |
Durmaz E, Asci A, Erkekoglu P et al. Urinary bisphenol a levels in girls with idiopathic central precocious puberty. Journal of Clinical Research in Pediatric Endocrinology, 2014, 6: 16-21. DOI:10.4274/Jcrpe |
| [7] |
Calafat AM, Ye X, Wong LY et al. Exposure of the U. S. population to bisphenol A and 4-tertiary-octylphenol: 2003-2004. Environmental Health Perspectives, 2008, 116: 39-44. |
| [8] |
Zhang Z, Alomirah H, Cho HS et al. Urinary bisphenol A concentrations and their implications for human exposure in several Asian countries. Environmental Science & Technology, 2011, 45: 7044-7050. |
| [9] |
Mackay(加)著. 黄国兰, 陈春江, 孙庆宁等译. 环境多介质模型: 逸度方法. 北京: 化学工业出版社, 2007.
|
| [10] |
董继元, 王世功, 高宏等. 兰州地区DDT的环境多介质迁移和归趋模拟. 生态环境学报, 2009, 18(2): 519-522. |
| [11] |
董继元, 王金玉, 张本忠等. 兰州城区多环芳烃的多介质归趋模拟研究. 环境科学学报, 2013, 33(2): 570-578. |
| [12] |
田慧, 郭强, 方利江等. 半干旱地区典型POPs硫丹环境多介质迁移归趋模拟研究——以兰州河谷盆地为例. 环境科学学报, 2013, 33(4): 1110-1117. |
| [13] |
李静, 吕永龙, 王铁宇等. 苯并(a)芘的环境多介质迁移和归趋模拟. 环境工程学报, 2008(2): 279-285. |
| [14] |
Wang B, Huang B, Jin W et al. Seasonal distribution, source investigation and vertical profile of phenolic endocrine disrupting compounds in Lake Dianchi, China. Journal of Environmental Monitoring, 2012, 14: 1275-1282. DOI:10.1039/c2em10856a |
| [15] |
齐丽, 周志广, 许鹏军等. 北京地区二噁英类的环境多介质迁移和归趋模拟. 环境科学研究, 2012, 25(5): 543-548. |
| [16] |
杨一光, 杨桂华. 滇池生态环境的变迁及其演化趋势. 云南大学学报, 1985, 7: 45-52. |
| [17] |
Liu JL, Wang RM, Huang B et al. Distribution and bioaccumulation of steroidal and phenolic endocrine disrupting chemicals in wild fish species from Lake Dianchi, China. Environmental Pollution, 2011, 159: 2815-2822. DOI:10.1016/j.envpol.2011.05.013 |
| [18] |
高洪波. 国内外双酚A的生产现状及发展趋势. 化学工程师, 2003, 97: 35-37. |
| [19] |
孙慧超. 大连市区部分多环芳烃(PAHs)的来源和多介质环境行为[学位论文]. 大连: 大连理工大学, 2005. http://cdmd.cnki.com.cn/article/cdmd-10141-2005051608.htm
|
| [20] |
于晓菲. 应用多介质环境模型评价典型有机污染物的环境行为[学位论文]. 大连: 大连理工大学, 2006. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1029632
|
| [21] |
敖江婷. Ⅳ级逸度模型对典型有机污染物环境行为的动态模拟[学位论文]. 大连: 大连理工大学, 2008. http://cdmd.cnki.com.cn/article/cdmd-10141-2009041692.htm
|
| [22] |
李小平. 国内苯酚市场状况及发展前景. 石化技术, 2006, 13: 53-56. |
| [23] |
Kang JH, Kondo F. Effects of bacterial counts and temperature on the biodegradation of bisphenol A in river water. Chemosphere, 2002, 49: 493-498. DOI:10.1016/S0045-6535(02)00315-6 |
| [24] |
Klecka GM, Gonsior SJ, West RJ et al. Biodegradation of bisphenol A in aquatic environments: River die-away. Environmental Toxicology Chemistry, 2001, 20: 2725-2735. DOI:10.1002/etc.v20:12 |
| [25] |
Staples CA, Dorn PB, Klecka GM et al. A review of the environmental fate, effects, and exposures of bisphenol A. Chemosphere, 1998, 36: 2149-2173. DOI:10.1016/S0045-6535(97)10133-3 |
| [26] |
李发荣. 昆明市空气污染趋势与防治. 云南环境科学, 2000, 19: 50-53. |
| [27] |
杨常亮. 昆明市空气污染特征及成因研究. 云南环境科学, 1999, 18: 44-46. |
| [28] |
陈红书. 昆明市中心区"九五"期间空气污染情况分析. 云南环境科学, 2002, 21: 59-62. |
| [29] |
施坤, 李云梅, 朱利等. 滇池水体总悬浮物散射系数参数化模型. 环境科学学报, 2010, 30: 1479-1485. |
| [30] |
卢少勇, 金相灿, 张烨等. 滇池内湖滨带底泥的有机质分布规律. 湿地科学, 2009, 7: 135-139. |
| [31] |
彭丹, 金峰, 吕俊杰等. 滇池底泥中有机质的分布状况研究. 土壤, 2004, 36: 568-572. DOI:10.3321/j.issn:0253-9829.2004.05.020 |
| [32] |
Diamond M, Ganapathy M, Peterson S et al. Mercury dynamics in the Lahontan Reservoir, Nevada: Application of the QWASI fugacity/Equivalence multispecies model. Water, Air, and Soil Pollution, 2000, 117: 133-156. DOI:10.1023/A:1005126704309 |
| [33] |
Cousins IT, Staples CA, Klecka GM et al. A multimedia assessment of the environmental fate of bisphenol A. Human and Ecological Risk Assessment, 2002, 8: 1107-1135. DOI:10.1080/1080-700291905846 |
| [34] |
Cao HY, Tao S, Xu FL et al. Multimedia fate model for hexachlorocyclohexane in Tianjin, China. Environmental Science & Technology, 2004, 38: 2126-2132. |
 2015, Vol. 27
2015, Vol. 27 


