(2: 江苏省渔业生态环境监测站, 南京 210036)
(3: 中国农业科学院农业质量标准与检测技术研究所, 北京 100081)
(2: Jiangsu Fishery Environment Monitoring Center, Nanjing 210036, P. R. China)
(3: Institute of Quality Standards and Testing Technology for Agro-Products, Chinese Academy of Agricultural Sciences, Beijing 100081, P. R. China)
湖泊是地表生态系统中人类赖以生存的自然单元之一,在供水、防洪、养殖、旅游、航运和维持生态平衡等方面发挥着巨大的作用.数十年来,随着我国人口增加和工农业生产的发展,加之湖泊水资源的过度开发,使得湖泊水资源短缺、水环境恶化和生态系统退化等问题日益凸显,已严重威胁到社会经济的可持续发展和人类健康[1].
水环境是一个开放和动态的体系,其中生物与非生物环境是相互关联和相互作用的[2].随着现代物质文明的飞速发展,人类活动向水环境中排放的污染物中包含的重金属也日益增多.重金属元素在水环境中的累积,对水生动物的生长发育、种族繁衍等一系列生命活动造成了极大的威胁.如重金属汞(Hg)、镉(Cd)、铜(Cu)等,其污染特点是来源广、残留时间长、具有累积性、能沿食物链转移、污染后不易被发现和难以恢复等,严重地危害着渔业水环境和水生生物,也对人类健康造成潜在威胁.
江苏是我国淡水湖泊分布集中的省(区)之一.现有太湖、滆湖、洪泽湖、高宝邵伯湖和骆马湖5个省管湖泊,其中对于太湖和洪泽湖的研究是国内研究的热点[3-9].多年来,主管部门虽然对这五大湖泊的增殖区、保护区、网围养殖区和进出湖河道等功能区开展渔业环境监测,但对这5个湖泊大量的渔业水质监测数据还缺乏系统分析.因此,采用现代统计分析技术从这些监测数据中挖掘出该地区湖泊水质的变化规律,不但可以为当地渔业生产服务,还可以为该地区行业发展政策制定提供技术支撑.
多指标综合评价法(Technique for Order Preference by Similarity to Ideal Solution, TOPSIS)也叫逼近于理想解的技术,由Hwang和Yoon于1981年首次提出,是系统工程中有限方案多目标决策分析常用的决策方法,其方法的核心思想是通过先定义决策问题的理想解与负理想解,然后比较评价方案与理想解和负理想解的距离远近,最后计算各个方案与理想解的相对贴近度,进行方案的优劣排序. TOPSIS法对数据分布及样本量、指标多少无严格限制,数学计算亦不复杂,既适用于少样本资料,又适用于多样本的大系统,已在医疗、经济、农业等领域中得到广泛应用[10-11].以往的渔业水质监测数据仅以简单的柱形图描述各监测指标是否超标,无统计学证据支撑.目前,基于长期定位监测数据的江苏省主要湖泊水质重金属的比较分析与综合评价,亦未见相关文献报道.
本文首次利用系统分组资料方差分析方法对江苏多年定位监测的5个湖泊水体的重金属数据进行统计分析,以鉴别湖泊间、湖泊内站位间和站位内年份间的差异显著性,在此基础上应用TOPSIS法对5个湖泊水体重金属进行综合对比分析,并对它们的变化规律进行总结.
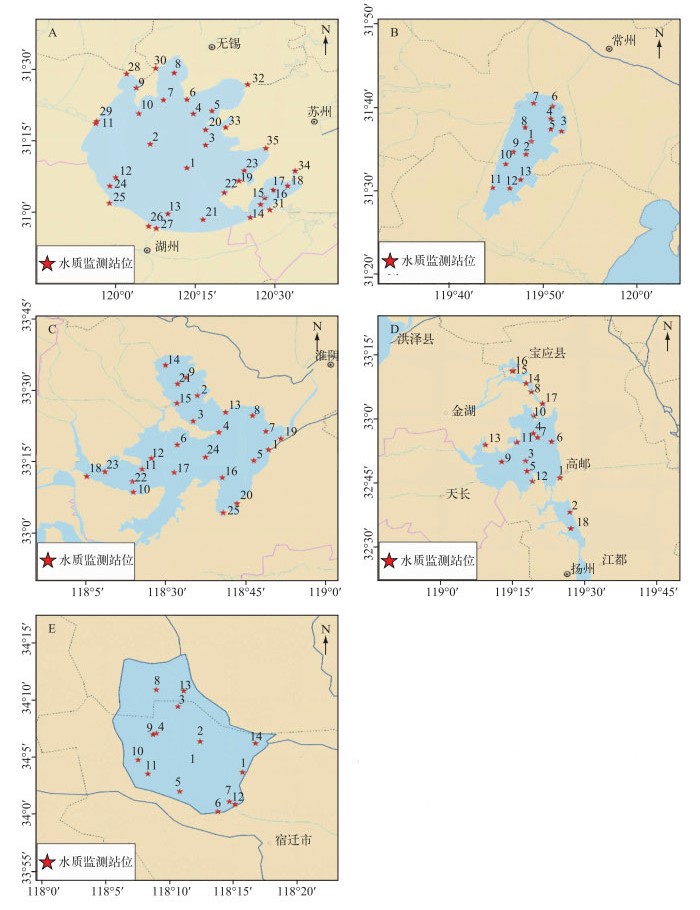
1 材料与方法 1.1 数据来源2001-2011年(不含2004年)间,由江苏省渔业生态环境监测站统一采集水样.采样时间上半年在4月份,下半年在10月份,5个湖泊采样时间基本一致.取重金属水样500 ml放于洁净的聚乙烯瓶中,之后加入适量硝酸保存,同时用采集的空白样品和10 %以上的平行样进行质量控制(QC控制).其中,太湖共监测413站次,滆湖共监测183站次,洪泽湖共监测205站次,高宝邵伯湖共监测221站次,骆马湖共监测142站次.其监测站位见图 1.
|
图 1 太湖(A)、滆湖(B)、洪泽湖(C)、高宝邵伯湖(D)和骆马湖(E)监测站位示意 Fig.1 Sketch maps showing the location of sampling points in Lake Taihu (A), Lake Gehu (B), Lake Hongze (C), Lake Gaobaoshaobo (D) and Lake Luoma (E) |
样品在硫酸-过硫酸钾体系中消解后,测定Hg浓度,加入抗坏血酸-硫脲后测定As浓度,两者均采用AFS-230a原子荧光光度计测定.采用SpectrAA220原子吸收分光光度计测定Cu、Pb和Cd浓度.分析质量使用试剂空白及平行样进行控制,加标回收来控制样品测定的准确性,结果均符合质控要求.
1.3 统计分析方法 1.3.1 系统分组资料方差分析以湖泊作为组,湖泊内监测站位作为组内亚组,站位内年份作为小亚组,进行三级系统分组资料方差分析以比较各重金属指标在不同湖泊间的差异显著性.
1.3.2 TOPSIS法进行水质综合评价主要分析步骤:(1)建立同趋势化的原始数据矩阵,以消除不同指标不同量纲及其数量级的差异对评价结果的影响;(2)对同趋势化的原始数据矩阵进行归一化处理,并建立归一化数据矩阵,其计算公式为:u=(x-xmin)/(xmax-xmin);(3)根据归一化矩阵得到最优值向量A+和最劣值向量A-;(4)分别计算各方案的评价指标值与最优方案和最劣方案的距离Di+和Di-,计算公式分别为:
10年内,江苏省五大湖泊Cu浓度的平均数为4.54 μg/L,中位数为2.86 μg/L,众数为2.00 μg/L;Pb浓度平均数为4.03 μg/L,中位数为2.50 μg/L,众数为0.50 μg/L;Cd浓度平均数为1.02 μg/L,中位数为0.50 μg/L,众数为0.005μg/L;Hg浓度平均数为0.118 μg/L,中位数为0.075 μg/L,众数为0.062 μg/L;砷浓度平均数为2.84 μg/L,中位数为2.66 μg/L,众数为2.03 μg/L.汇总五大湖泊水体重金属的数据,其中均是众数 < 中位数 < 平均数,可知5种重金属浓度呈右偏态分布(图 2).

|
图 2 江苏省五大湖泊水体中重金属Cu、Pb、Cd、Hg和As浓度分布直方图 Fig.2 The histogram of Cu, Pb, Cd, Hg and As concentrations in water of the five lakes in Jiangsu Province |
分别对不同湖泊水体重金属监测数据进行描述性统计分析,可以得到其指标特征(表 1).
| 表 1 2001-2011年江苏省五大湖泊水体中重金属浓度基本统计量 Tab.1 Basic statistics of heavy metal concentrations in water of the five lakes in Jiangsu Province from 2001 to 2011 |
由表 1可知,江苏省五大湖泊10年间水体重金属Cu、Pb、Cd、Hg、As的平均浓度均符合《渔业水质标准》[12],但是相对变异均较大,尤其是Cu浓度的最大值已超过《渔业水质标准》[12].说明重金属监测过程中个别年份个别站位重金属污染较重,存在极端大值的影响.
2.3 五大湖泊水体重金属指标差异显著性比较采用系统分组资料方差分析方法对上述重金属指标进行方差分析,结果表明:湖泊水体中除Cu浓度外,其他4种重金属浓度5个湖泊间均差异极显著,这可能与湖泊周围环境条件的差异、入湖污染物的排放以及农田农药化肥的施用有关.另外,湖泊内站位间各重金属浓度的差异均不显著. Pb、Cd、Hg浓度站位内年份间差异显著或极显著,说明它们年际变化均不稳定,Cu和As浓度站位内年份间差异不显著(表 2).
| 表 2 江苏省五大湖泊水体中重金属浓度方差分析结果1) Tab.2 The ANOVA of heavy metal concentrations in water of the five lakes in Jiangsu Province |
进一步对湖泊间差异显著或极显著的重金属浓度进行多重比较,结果见表 3.
| 表 3 江苏省五大湖泊渔业水质重金属浓度多重比较结果 Tab.3 The multiple comparisons of heavy metal concentrations in fishery water of the five lakes in Jiangsu Province |
多重比较结果表明:骆马湖水体Pb浓度最高,为8.54 μg/L,与其他4个湖泊间差异显著.洪泽湖Cd浓度最高为1.44 μg/L,与太湖和高宝邵伯湖差异不显著,与滆湖和骆马湖差异显著.骆马湖Hg浓度最高为0.19 μg/L,与洪泽湖差异不显著,与其他3个湖泊差异显著.太湖As浓度最高为10.40 μg/L,与其他4个湖泊差异显著,其他4个湖泊间差异不显著.
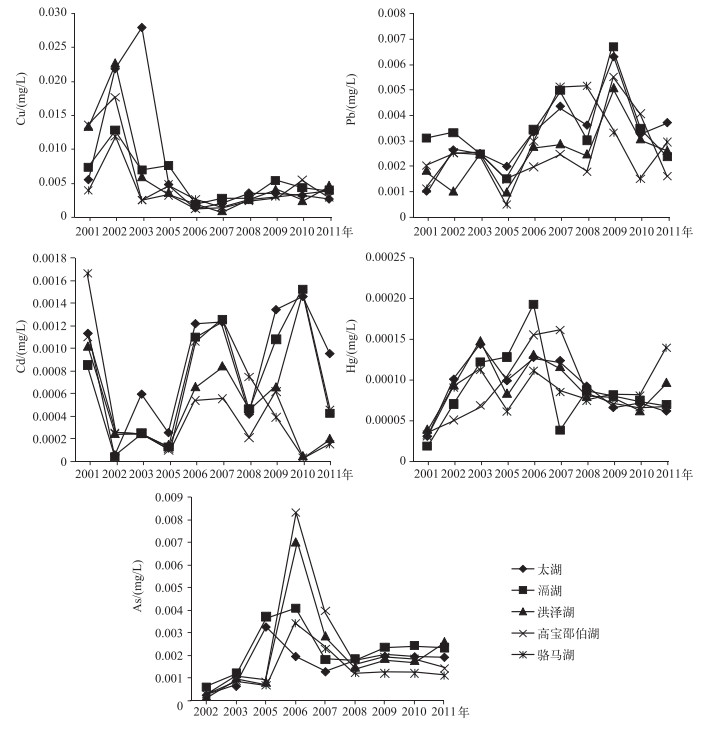
2.4 10年内五大湖泊重金属变化趋势10年间,Cu浓度在江苏省五大湖泊间具有相同的变化趋势,5个湖泊基本上在2002年前后出现最大值,近几年Cu浓度有所下降,说明可能2002年前后5个湖泊均有含Cu污染物的排入,导致Cu浓度的增高. As浓度在5个湖泊间也具有相同的变化趋势,5个湖泊基本上在2006年前后出现最大值,近几年As浓度有所下降,说明在2006年前后5个湖泊可能均有含As污染物的排入,随着水体的流动和更替,As浓度近几年来有所下降.而5个湖泊Pb浓度2007年以来相对较高,其平均浓度明显高于2006年之前. 5个湖泊2003-2006/2007年Hg浓度也高于其他年份. 10年内5个湖泊Cd浓度变化趋势无明显规律(表 3).
2.5 五大湖泊水质重金属综合评价采用TOPSIS法进行分析时,将同趋势化后的数据进行归一化处理,并建立相应的归一化数据矩阵(表 4).
| 表 4 江苏省五大湖泊水体中重金属指标归一化结果 Tab.4 The uniformization of heavy metal in water of the five lakes in Jiangsu Province |
由表 4可知最优值向量A+和最劣值向量A-分别为A+=min(0, 0, 0, 0, 0)和A-=max(1, 1, 1, 1, 1).
计算各重金属指标值与最优方案和最劣方案的距离,以及与最优方案的相对接近程度(Ci),并按Ci值大小对各水体进行排序. Ci值越小,说明重金属污染越轻;反之,污染越重.由表 5可知:高宝邵伯湖Ci值(0.5091)最小,骆马湖Ci值(0.5858)最大,说明总体而言高宝邵伯湖水体重金属污染程度最小,骆马湖水体重金属污染程度最大.洪泽湖Ci值(0.5226)、太湖Ci值(0.5397)和滆湖Ci值(0.5499)相差不多,说明这3个湖泊重金属污染综合评价优劣相当.
| 表 5 江苏省五大湖泊水体中重金属综合评价结果 Tab.5 Evaluation results of heavy metal in water of the five lakes in Jiangsu Province |
在水资源的污染中,重金属污染影响大,可恢复难度大,给江苏省的水环境带来很大的破坏.重金属污染物进入水中后通过一系列化学作用迁移转化,参与和干扰各种环境化学过程和物质循环,最终以一种或多种形态长期存留在环境中,造成永久性的潜在危害[13]. 10年内骆马湖水体Pb和Hg浓度最高,洪泽湖水体Cd浓度最高,太湖水体As浓度最高.对湖泊沉积物重金属的已有研究结果表明,骆马湖受人为污染影响严重的主要是重金属中的Pb与Cd[14],洪泽湖底质污染为Cd污染[15],危害太湖生态安全的主要重金属元素为As、Cr和Hg[16].结合本研究结果证实,沉积物与水体中重金属均可能与外源输入有关.而且,五大湖泊水体中Cu和As浓度变化趋势大致相同(图 3).已有研究资料表明,太湖不同湖区/入湖河流水体重金属浓度存在一定的差异[17],但是本研究在方差分析的基础上,综合五大湖泊的信息,统计推断出5种重金属浓度在湖泊内站位间均差异不显著.然而,江苏省五大湖泊重金属污染并未随着经济发展水平的差异呈现由北到南越来越重的趋势,这可能是由于各湖泊的利用方式不同,湖泊周围环境条件不同,以及湖泊监管治理的不同,造成了江苏省五大湖泊水体中重金属浓度的差异.但目前由于缺乏诸如湖泊周围的工业废物排放、农用化肥使用等一些关联数据,因此有关湖泊之间重金属污染存在差异的原因有待于进一步探讨.
|
图 3 江苏省五大湖泊重金属浓度年度均值变化趋势 Fig.3 Annual average concentrations of heavy metals in water of the five lakes in Jiangsu Province |
水体中的重金属污染主要来自两部分:自然源和人为源.自然源主要是岩石风化的碎屑产物,通过自然途径进入水体中的重金属一般不会对水体造成污染;人为污染源主要包括采矿和冶炼、金属加工、化工、废电池处理、电子、造革和染料、农药和化肥的使用等,是造成水体重金属污染的主要原因[18].由于工农业生产的迅猛发展,排放到水体中的重金属元素日益增多,水环境中的污染问题亦日益凸显.因此,控制重金属污染物的排放,改善江苏湖泊的水环境现状,是摆在我们面前无法回避的一项十分迫切和艰巨的任务.总体而言,10年来江苏省五大湖泊水体重金属平均浓度均符合《渔业水质标准》,但本文发现湖泊间、站位内的年份间重金属浓度存在一些差异,有的差异已经达到统计学上显著的程度,这些结果可为检测管理部门以及政府决策提供一些参考信息.
4 结论经过2001-2011年对江苏省五大湖泊1164站次长期的定位监测,表明五大湖泊水体中Cu、Pb、Cd、Hg和As浓度均符合《渔业水质标准》,除Cu浓度外,其他4种重金属浓度5个湖泊间均差异极显著,湖泊内站位间各重金属浓度均差异不显著.综合分析结果表明,高宝邵伯湖水体重金属污染程度最小,骆马湖水体重金属污染程度最大,洪泽湖、太湖和滆湖水体重金属污染综合评价优劣相当.
| [1] |
濮培民, 王国祥, 李正魁等. 健康水生态系统的退化及其修复-理论、技术及应用. 湖泊科学, 2001, 13(3): 193-203. DOI:10.18307/20010301 |
| [2] |
孟紫强. 环境毒理学基础. 北京: 高等教育出版社, 2005.
|
| [3] |
成芳, 凌去非, 徐海军等. 太湖水质现状与主要污染物分析. 上海海洋大学学报, 2010, 19(1): 105-110. |
| [4] |
李波, 濮培民, 韩爱民. 洪泽湖水质的时空相关性分析. 湖泊科学, 2002, 14(3): 259-266. DOI:10.18307/2002.0311 |
| [5] |
高永年, 高俊峰, 陈坰烽等. 太湖流域水生态功能三级分区. 地理研究, 2012, 31(11): 1941-1951. |
| [6] |
袁和忠, 沈吉, 刘恩峰. 太湖重金属和营养盐污染特征分析. 环境科学, 2011, 32(3): 649-657. |
| [7] |
刘瑞民, 王学军, 郑一等. 太湖水质参数中小尺度空间结构特征. 长江流域资源与环境, 2002, 11(1): 32-35. |
| [8] |
张少威, 刘茂松, 徐驰等. 洪泽湖7条入湖河流的水质动态及其关联分析. 南京林业大学学报:自然科学版, 2012, 36(4): 36-40. |
| [9] |
李波, 濮培民. 淮河流域及洪泽湖水质的演变趋势分析. 长江流域资源与环境, 2003, 12(1): 67-73. |
| [10] |
刘玉秀, 徐少青. TOPSIS法用于医院工作质量的多指标综合评价. 中国卫生统计, 1993, 10(2): 12-15. |
| [11] |
雷战波, 朱正威, 王雷. 基于熵权夹角和TOPSIS的企业经济效益诊断模型. 运筹与管理, 2005, 14(2): 142-148. |
| [12] |
GB 11607-1989. 渔业水质标准.
|
| [13] |
戴树桂. 环境化学. 北京: 高等教育出版社, 1996.
|
| [14] |
王永平, 洪大林, 申霞等. 骆马湖沉积物重金属及营养盐污染研究. 南水北调与水利科技, 2013, 11(6): 45-49. |
| [15] |
刘振坤, 张书海. 洪泽湖底质重金属污染变化趋势分析. 江苏环境科技, 2005, 18(4): 41-43. |
| [16] |
石志芳. 太湖沉积物中重金属污染特征及生态风险评价[学位论文]. 杨凌: 西北农林科技大学, 2010.
|
| [17] |
Zeng J, Yang LY, Chen XF et al. Spatial distribution and seasonal variation of heavy metals in water and sediments of Taihu lake. Polish Journal of Environmental Studies, 2012, 21(5): 1489-1496. |
| [18] |
王海东, 方凤满, 谢宏芳. 中国水体重金属污染研究现状与展望. 广东微量元素科学, 2010, 17(1): 14-18. |
 2016, Vol. 28
2016, Vol. 28 

