(2: 浙南水科学研究院, 温州 325035)
(2: Southern Zhejiang Water Research Institute, Wenzhou 325035, P.R.China)
平原河网地区由于其特殊的地理位置和自然条件,通常人口稠密,近年来随着社会经济的快速发展和城市化进程的加快,河网水体纳污量不断增加,使得大量的氮素进入水体,从而破坏了原有的氮平衡体系,导致水体的氮污染加剧,尤其是氨氮,已成为引起平原河网水体水质超标的主要污染物.在水生态系统中广泛分布着个体微小、营养类型多样、种类繁多、代谢极为活跃的各类微生物[1].相关研究表明,微生物数量或生物量随水环境中营养程度的递增而增加[2].因此,在平原河网这种严重富营养化、大型水生生物消亡的水环境中,微生物所扮演的角色及发挥的生态效应将会显得尤为重要.作为水生态系统中重要的组成部分[3-4],微生物在有机物的降解、生源要素的形态转化和地球化学循环等方面发挥着举足轻重的作用[5],其中,自然界中氮的生物地球化学循环主要由微生物驱动.在富营养水生生态系统中,氮循环菌对氮素的迁移和转化起着至关重要的作用,其相应的理论研究与实际应用均极为重要.因此,对平原河网氮污染水体中的氮循环菌开展相关研究,不仅可以深化对平原河网中氮转化机理及转化效应的认识,而且可为河道氮污染的控制、修复及管理提供支撑.
温瑞塘河是温州市人口、经济和污染的聚集地,为典型的南方平原河网,河床比降小,流速缓慢,其水系河道贯穿温州地区的鹿城、瓯海、龙湾、瑞安“三区一市”,其河道总长度为1178.4 km,其中主河道长33.8 km,随着当地社会经济和城市建设的快速发展,各种生活污水和工业废水不断进入河网,导致其水环境污染问题日益突出[6-9].同时,由于温瑞塘河相对静止的状态,在其水系内创造了许多独特且相对稳定的生境,为相关水环境的原位实验提供了良好条件.因此,本研究以温瑞塘河不同氮污染程度的河道为研究对象,对其中浮游、颗粒附着及底泥中的氮循环菌开展研究,揭示平原河网水体氮污染程度对氮循环菌的影响效应,探讨氮污染水体中氮的迁移、转化规律,为平原河网地区氮污染水体的生态修复和可持续管理提供理论参考.
1 材料与方法 1.1 实验设计实验区域(27°55′N, 120°42′E)设立在浙江省温州市温瑞塘河茶山段舜岙河和横江河上,位于温州医科大学茶山校区附近依据河道不同氮污染程度及水质状况,筛选3条河道设置研究点位,分别标记为A1、A2和A3(图 1).实验期间,不同实验区域的水质情况见表 1,水质指标的测定方法参照《湖泊富营养化调查规范》进行[10].分别于2014年10月14日、11月8日、12月2日及12月22日,用采水器和彼得森采泥器(开口面积为0.0625 m2)分别采集表层水样和表层底泥样品,用保温箱冷藏带回实验室做后续处理.整个实验参照随机区组设计,以河道中不同氮污染程度为处理因素、以采样时间作为区组,对水体中不同生活方式的氮循环菌影响效应进行研究.
|
图 1 研究点位示意 Fig.1 Location of study sites |
| 表 1 实验期间研究点位的水环境状况 Tab.1 Differences in the physical and chemical parameters at different study sites during the experiment |
采用最大可能数法(most probable number, MPN)对不同河道水体中的浮游、颗粒附着及底泥中氮循环菌进行测定.参照文献[11-12]的膜过滤方法,经孔径为5 μm聚碳酸酯膜过滤,截留在滤膜上的微生物为颗粒附着微生物,并用与过滤体积相同的灭菌水对截留的颗粒物进行振荡悬浮混匀,用于颗粒附着氮循环菌的测定;而孔径为5 μm聚碳酸酯膜过滤后的滤液用于浮游氮循环菌的测定;取底泥10 g,置于含90 ml灭菌水的锥形瓶中,振荡混匀,即得稀释10倍的底泥样品,用于底泥中氮循环菌的测定,在将底泥样品与其他样品进行比较时,视1 g为1 ml.
同时,分别配置氨化、亚硝化、硝化及反硝化菌培养液[13],分装于试管中,每支9 ml,并在反硝化培养液中倒置小玻璃管,加塞,在121℃下灭菌30 min.每个样品作5~7个10倍系列稀释,每支试管各接种样品和稀释样品1 ml,每个稀释梯度做3个平行.在28±1℃下暗处进行培养,氨化细菌培养7 d,反硝化细菌培养15 d,亚硝化和硝化细菌均培养30 d.以纳氏试剂、格利斯试剂、二苯胺试剂等对各种形态氮的产生和消失情况进行检测,并定期观察倒置小玻璃管中的产气情况.通过查MPN表及相应的稀释倍数计算样品中各种氮循环菌的数量.
1.3 数据分析实验数据采用SPSS 16.0统计软件进行方差分析和Duncan多重对比,采用Sigmaplot 12.0软件进行作图,采用PAST软件的相似性分析(Analysis of similarity, ANOSIM)模块对不同氮污染程度下氮循环菌种群结构的差异进行定量比较. ANOSIM是一种比较不同群落差异显著性的非参数检验方法[14],在本实验中,将数据经过百分数转换后,以Bray-Curtis指数为相似性度量参数,显著性以10000次重复取样的排列群组算法进行计算.通过比较ANOSIM产生的R值(R值的大小表示不同群落的分离程度,1表示完全分离,即两个群落没有任何相似性,0表示两个群落完全相同,没有分离)对氮循环菌组成结构的相似性进行比较.
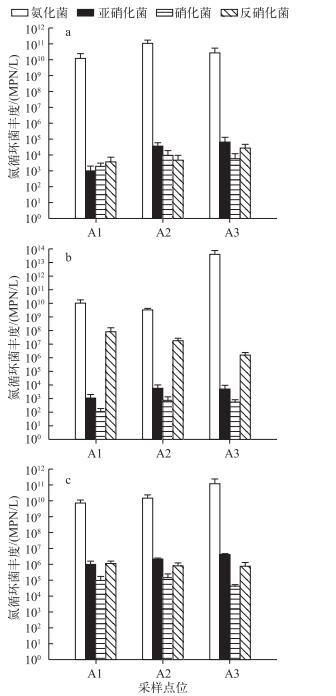
2 结果与分析 2.1 水体氮污染程度对浮游氮循环菌的影响由不同氮污染程度下浮游氮循环菌的丰度变化可知,在氮污染情况下,氮循环菌中的氨化菌丰度显著高于其他氮循环菌多个数量级.浮游态亚硝化菌和反硝化菌的丰度随水体氮污染程度的增加而升高;而硝化菌的丰度出现先升高后下降的趋势,其丰度与亚硝化菌相比,差距逐渐增大(图 2a).
|
图 2 不同氮污染程度对浮游氮循环菌(a)、颗粒附着氮循环菌(b)和底泥中氮循环菌(c)丰度的影响 Fig.2 Effects of aquatic nitrogen pollution on the planktonic nitrogen cycling bacteria(a), particle-attached nitrogen cycling bacteria(b)and benthic nitrogen cycling bacteria(c) |
由不同氮污染程度下颗粒附着氮循环菌的丰度变化可知(图 2b),在氮污染情况下,颗粒附着氮循环菌中的氨化菌在丰度上依旧具有明显优势,与浮游态相比,颗粒附着氮循环菌中的反硝化菌具有相对较高的丰度.另外,随着氮污染程度的升高,亚硝化菌和硝化菌丰度逐渐升高,而反硝化菌丰度则逐渐降低.
2.3 水体氮污染程度对底泥中氮循环菌的影响由不同氮污染程度下底泥中氮循环菌的丰度变化(图 2c)可知,在不同的氮污染区域,氮循环菌中的氨化菌丰度都最高,显著高出其他氮循环菌多个数量级.随着氮污染程度的增加,底泥氮循环菌中的氨化菌和亚硝化菌丰度有所增加,但4类氮循环菌的组成比例情况变化不大,均呈现出高丰度的氨化菌和低丰度的硝化菌的组成情况,并随氮污染程度的升高亚硝化菌与硝化菌丰度之间的差距逐渐增大.
2.4 不同氮污染程度、不同生活类型氮循环菌组成结构的相似性分析为了能够更好地判断不同氮污染程度、不同生活类型氮循环菌在组成结构上出现的变化,对氮循环菌的组成结构进行相似性分析(ANOSIM),结果可知,氮循环菌组成结构在不同氮污染程度之间的差异不显著. A1与A2点位、A1与A3点位以及A2与A3点位R值分别为-0.01678、-0.02499以及-0.02331(P>0.05).而在不同生活类型之间差异相对较大,浮游与颗粒附着氮循环菌之间(R=0.1099, P < 0.05)、底泥与颗粒附着氮循环菌之间(R=0.1138, P < 0.05)统计分析均达显著水平,而浮游与底泥氮循环菌之间(R=0.2028, P < 0.01)统计分析达极显著水平.通过对各生活类型之间分别进行比较可以看出,浮游与底泥中氮循环菌之间的R值大于底泥与颗粒附着氮循环菌之间的R值,而浮游与颗粒附着氮循环菌之间的R值相对最小,说明氮循环菌组成结构在浮游与底泥之间差异最大.
3 讨论随着我国经济的快速发展和城市化进程的加快,生活生产污水中大量的含氮物质被排入城市河道,造成平原河网地区水环境的严重污染.受污染的河水不仅会失去资源功能和使用价值,而且会严重破坏周围景观,甚至危害人类的身体健康.水体中不同形态氮之间的转化主要依赖于水生态中大量的氮循环微生物.这些在水环境中广泛分布、代谢活跃的氮循环微生物,对平原河网水生态的平衡、过量氮素的迁移转化发挥着积极地作用.然而,作为氮循环的直接参与者,这些氮循环微生物的群落特征和功能作用也会受到包括氮素形态、浓度在内的多种环境因子的影响[15].本文研究结果显示,高氮污染的河流水环境中氮循环菌呈现出一些与其他环境不一样的分布特征.首先,氨化菌的丰度显著高于其他氮循环菌,而亚硝化菌和硝化菌丰度相对较低,组成比例失衡(图 2).这应该是由于氨化菌以有机氮为底物,通常在有机物较多的环境中生长较好[16-18].而平原河网水体受到沿岸生活、餐厨污物的影响较大,有机物汇入较多,水体氮浓度高,溶解氧浓度普遍偏低,在研究中总氮浓度最低的A1点,实验期间其平均总氮浓度也在21.00±4.15 mg/L(表 1),这为氨化菌的生存提供了充足的底物和适宜的生存环境,这可能是本研究结果中氨化菌丰度相对较高的原因.而亚硝化菌和硝化菌为化能自养菌,当氨化菌等异养菌利用有机物快速增殖时,对亚硝化菌和硝化菌会产生竞争优势,使其生长受到限制[19-20],这可能是亚硝化菌和硝化菌丰度较低的原因之一,也有可能正是因为亚硝化菌和硝化菌丰度显著低于氨化菌进而导致水体中氨态氮得不到有效转化,使研究水域出现高氨态氮浓度的情况.
另外,对比亚硝化菌与硝化菌,发现亚硝化菌丰度普遍高于硝化菌(图 2).相关研究表明在自然水体中游离氨对亚硝化菌、硝化菌存在抑制作用,作用浓度范围分别为10~150 mg/L和0.1~1.0 mg/L,可见硝化菌对游离氨更为敏感[21].同时,据文献报道,亚硝化菌的溶解氧饱和常数一般为0.2~0.4 mg/L,而硝化菌的溶解氧饱和常数一般为1.2~1.5 mg/L,在低溶解氧条件下亚硝化菌对溶解氧的亲和力大于硝化菌[22].相应的,在杨旭楠等的研究结果中便出现在低氧的河流沉积物中亚硝化菌丰度高于硝化菌的情况[23].因此,在高氮污染的水体中游离氨的存在及低浓度的溶解氧可能是导致亚硝化菌丰度普遍高于硝化菌的原因.而随着水体氮污染程度的增加,溶解氧浓度的降低,相应的会更有利于亚硝化菌而不利于硝化菌的生长,这可能是实验中随着氮污染程度的增加亚硝化菌和硝化菌丰度差异逐渐增大的原因.
通过对不同氮污染程度、不同生活类型氮循环菌组成结构进行相似性分析,发现不同氮污染程度之间氮循环菌在组成结构上均较为相似,而不同生活类型之间差别相对较大,并均达到显著性水平.水体中微生物生理类群的数量往往与相应化合物的浓度密切相关,但在本研究中不同污染程度区域之间氮浓度虽然存在显著差异,但这种差异可能不及不同生活类型的氮循环菌所处的微环境差别之大,即使在氮浓度如此之高的水环境中,底泥与水体之间的差异依旧是不同研究区域之间所不能比拟的,这可能是导致不同生活类型氮循环菌组成结构差异相对较大的原因.另外,与其他生活类型相比,在颗粒附着态中明显出现了较高丰度的反硝化菌,这可能与颗粒微界面这一特殊环境存在联系;而随着氮污染程度的增加,颗粒附着反硝化菌的丰度出现下降,这可能与反硝化菌的底物硝态氮在研究水域中随着总氮、氨态氮浓度的增加而出现降低存在联系(表 1).
不同生活类型的氮循环菌种群结构组成存在较大差异,在悬浮颗粒物上反硝化菌存在相对较高的丰度.而纵观平原河网氮污染水体中氮循环菌丰度的分布可以发现,在氮循环菌中氨化菌为优势种群,而亚硝化菌和硝化菌丰度相对较低,不同生理类群氮循环菌组成比例失衡.
致谢: 感谢洪宇轩、蔡芬芬、杨李君、严璐在实验中给予的帮助.| [1] |
Hahn MW. The microbial diversity of inland waters. Current Opinion in Biotechnology, 2006, 17(3): 256-261. DOI:10.1016/j.copbio.2006.05.006 |
| [2] |
Zhou WH, Li T, Cai CH et al. Spatial and temporal dynamics of phytoplankton and bacterioplankton biomass in Sanya Bay, northern South China Sea. Journal of Environmental Sciences, 2009, 21(5): 595-603. DOI:10.1016/S1001-0742(08)62313-X |
| [3] |
Azam F, Worden AZ. Microbes, molecules, and marine ecosystems. Science, 2004, 303: 1622-1624. DOI:10.1126/science.1093892 |
| [4] |
Psenner R, Alfreider A, Schwarz A. Aquatic microbial ecology: Water desert, microcosm, ecosystem. What's Next? International Review of Hydrobiology, 2008, 93: 606-623. DOI:10.1002/iroh.v93:4/5 |
| [5] |
Fuhrman JA. Microbial community structure and its functional implications. Nature, 2009, 459: 193-199. DOI:10.1038/nature08058 |
| [6] |
Lu P, Mei K, Zhang YJ et al. Spatial and temporal variations of nitrogen pollution in Wen-Rui Tang River watershed, Zhejiang, China. Environmental Monitoring and Assessment, 2011, 180(1): 501-520. |
| [7] |
Shi HH, Yang B, Huang MS et al. The toxicity of sediments from the black-odors river of Wenzhou, China to the embryos of Xenopus tropicalis. Fresenius Environmental Bulletin, 2012, 21: 3952-3958. |
| [8] |
Yang LP, Mei K, Liu XM et al. Spatial distribution and source apportionment of water pollution in different administrative zones of Wen-Rui-Tang (WRT) river watershed, China. Environmental Science and Pollution Research, 2013, 20(8): 5341-5352. DOI:10.1007/s11356-013-1536-x |
| [9] |
Ji Xiaoliang, Shang Xu, Zhu Yuanli et al. Spatial and temporal distribution of organic contamination and nutrient in Wenruitang River network. Environmental Chemistry, 2013, 32(4): 702-703. [纪晓亮, 商栩, 朱元励等. 温瑞塘河河网水体中有机物和营养盐的时空分布特征. 环境化学, 2013, 32(4): 702-703. DOI:10.7524/j.issn.0254-6108.2013.04.026] |
| [10] |
Jin Xiangcan, Tu Qingying. Investigation handbook of lake eutrophication (2nd ed). Beijing: China Environmental Science Press, 1990, 138-207. [金相灿, 屠清瑛. 湖泊富营养化调查规范(第二版). 北京: 中国环境科学出版社, 1990, 138-207.]
|
| [11] |
Kellogg C, Deming J. Comparison of free-living, suspended particle, and aggregate-associated bacterial and archaeal communities in the Laptev Sea. Aquatic Microbial Ecology, 2009, 57(1): 1-18. DOI:10.1007/s00248-008-9465-9 |
| [12] |
Hugoni M, Etien S, Bourges A et al. Dynamics of ammonia-oxidizing Archaea and Bacteria in contrasted freshwater ecosystems. Research In Microbiology, 2013, 164(4): 360-370. DOI:10.1016/j.resmic.2013.01.004 |
| [13] |
Li Zhengao, Luo Yongming, Teng Ying. Research methods of soil and environmental microorganism. Beijing: Science Press, 2008, 100-103. [李振高, 骆永明, 滕应. 土壤与环境微生物研究法. 北京: 科学出版社, 2008, 100-103.]
|
| [14] |
Clarke KR. Non-parametric multivariate analyses of changes in community structure. Australian Journal of Ecology, 1993, 18(1): 117-143. DOI:10.1111/aec.1993.18.issue-1 |
| [15] |
Abell GCJ, Ross DJ, Keane JP et al. Nitrifying and denitrifying microbial communities and their relationship tonutrient fluxes and sediment geochemistry in the Derwent Estuary, Tasmania. Aquatic Microbial Ecology, 2013, 70(1): 63-75. DOI:10.3354/ame01642 |
| [16] |
Liu Dongshan, Luo Qifang. Distribution and role of denitrifying, nitrifying, nitrosation and ammonifying bacteria in East Lake. Environmental Science, 2002, 23(3): 29-35. [刘东山, 罗启芳. 东湖氮循环细菌分布及其作用. 环境科学, 2002, 23(3): 29-35.] |
| [17] |
Liu Huihui, Xue Chaobo. The bacteria distribution on the culture environment of interdial shellfish. Acta Ecologica Sinica, 2008, 28(1): 436-444. [刘慧慧, 薛超波. 滩涂贝类养殖环境的细菌分布. 生态学报, 2008, 28(1): 436-444.] |
| [18] |
Du Ping, Liu Jingjing, Zeng Jiangning et al. Spatial distribution patterns of heterotrophic, nitrogen, and phosphate bacteria in hypoxic zone of Yangtze River Estuary. Chinese Journal of Applied Ecology, 2011, 22(5): 1316-1324. [杜萍, 刘晶晶, 曾江宁等. 长江口低氧区异养细菌及氮磷细菌分布. 应用生态学报, 2011, 22(5): 1316-1324.] |
| [19] |
Wang Haili, Yang Jifang, Chen Jigang et al. Spatio-temporal distribution of nitrifying and denitrifying bacteria with related to environmental factors in Xiangshan Bay. Chinese Journal of Ecology, 2011, 30(4): 752-762. [王海丽, 杨季芳, 陈吉刚等. 象山港海域硝化细菌与反硝化细菌的时空分布特征及其与环境因子的关系. 生态学杂志, 2011, 30(4): 752-762.] |
| [20] |
Wang Junan, Li Dong, Zhang Jie et al. Partial nitrosification in biofilter for sewage with low ammonia at room temperature. Journal of Beijing University of Technology, 2012, 38(1): 121-125. [王俊安, 李冬, 张杰等. 常温低氨氮污水生物滤池部分亚硝化的实现. 北京工业大学学报, 2012, 38(1): 121-125.] |
| [21] |
Li Yafeng, Ma Chenxi, Zhang Chi. SBR nitrosation realization of different aeration modes and NO2--N accumulation. Chinese Journal of Environmental Engineering, 2014, 8(11): 4561-4567. [李亚峰, 马晨曦, 张驰. 不同曝气方式下SBR亚硝化的实现及NO2--N积累效果. 环境工程学报, 2014, 8(11): 4561-4567.] |
| [22] |
Laanbroek HJ, Bodelier PLE, Gerard S. Oxygen consumption kinetics of nitrosomonas europaea and nitrobacter hamburgensis grown in mixed continuous cultures at different oxygen concentrations. Archives of Microbiology, 1994, 161(2): 156-162. DOI:10.1007/BF00276477 |
| [23] |
Yang Xunan, Lin Xingrui, Fu Shiyu et al. Effect of dissolved oxygen on the vertical distribution of nitrifying bacteria in tidal river sediment. Acta Scientiarum Naturalium Universitatis Sunyatseni, 2013, 52(5): 91-96. [杨旭楠, 林兴锐, 符诗雨等. 感潮河流沉积物中溶解氧对硝化细菌垂向分布的影响. 中山大学学报:自然科学版, 2013, 52(5): 91-96.] |
 2016, Vol. 28
2016, Vol. 28 

