(2: 中国科学院大学, 北京 100049)
(3: 中国科学院大学中丹学院, 北京 100190)
(4: 苏州科技大学环境科学与工程学院, 苏州 215011)
(2: University of Chinese Academy of Sciences, Beijing 100049, P. R. China)
(3: Sino-Danish Center for Education and Research, Beijing 100190, P. R. China)
(4: School of Environmental Science and Engineering, Suzhou University of Science and Technology, Suzhou 215011, P. R. China)
磷循环属于典型的沉积型循环[1].沉积物作为湖泊磷的蓄积库,汇集了各种类型的陆源磷,但在一定条件下,沉积物又由磷的“汇”转变为“源”,不断地释放到上覆水中[2-3].因此,探究沉积物中磷的来源,对控制和治理湖泊富营养化具有重要的指导意义.
目前发现的磷同位素有23种(24P~46P),但只有31P是稳定同位素,其余均为放射性同位素,含量低、半衰期短,限制了它们在磷源示踪和磷循环方面的应用[4].在自然界中,磷主要以磷酸盐的形式存在,且PO43-中的P与O的结合比较稳定(键能为359.8 kJ/mol);在地表温度和pH范围内,若没有生物的作用P-O键不易断裂.基于此,磷酸盐的氧同位素(δ18OP)作为一种示踪剂广泛地应用于磷的生物地球化学循环研究[5-8].
通常,样品中的PO43-要转化成Ag3PO4,然后采用同位素比值质谱法(IRMS)进行磷酸盐氧同位素测定.然而自然界中的样品成分复杂,尤其是有机质的存在,既影响Ag3PO4生成,又干扰δ18OP测定,因此测定之前需要对样品进行提取和纯化处理.首先,提取PO43-之前对样品进行除碳处理,可以有效地提高后续纯化效果. Stephan和O'Neil等针对有机质含量较高的生物性磷酸盐样品(如动物骨骼、牙齿等),分别提出了用2.5% NaClO + NaOH和30% H2O2进行预处理的方法[9-10]. NaClO处理后Ag3PO4产物颜色呈亮黄绿色,且结晶较大. H2O2处理可以去除有机碳,缩短了磷酸盐的提取时间,并且可生成较纯净的Ag3PO4产物.其次,前处理中最为关键的步骤是纯化提取的PO43-,Blake教授和McLaughlin教授分别提出了不同的纯化方法[11-12]. Blake方法首先将矿石提取液稀释至海水浓度,用2次氢氧化镁共沉淀(magnesium-induced co-precipitation,简称MAGIC)进行富集,同时去除部分杂质;接着用PO43-的特征沉淀磷钼酸铵(APM)和磷酸铵镁(MAP)进一步纯化PO43-;然后依次用阳离子交换树脂除去金属离子、阴离子交换树脂除去有机质、阳离子交换树脂除去HCO3-. McLaughlin方法是用一次MAGIC富集海水中的溶解态磷酸盐,然后用PO43-的特征沉淀CePO4进一步纯化PO43-,再用阳离子交换树脂除去Ce3+,最后将PO43-转化成Ag3PO4.卢阳阳等[13]改进了McLaughlin法,在除去Ce3+后用阴离子交换树脂除有机质. Blake法的优点是APM和MAP沉淀对pH要求较低,容易生成,且沉淀量小,对有机质的吸附作用小;缺点是操作繁琐、耗时. McLaughlin法的优点是CePO4对Cl-等杂质离子有较好的去除效果;缺点是CePO4受pH影响较大,Fe、Al、Ca等金属离子会干扰沉淀的生成.已有的预处理方法主要是针对海水、矿石、土壤、动物骨骼、牙齿等,而对湖泊沉积物的研究相对较少[6, 9-10, 12, 14-15].湖泊沉积物组成相对其余样品更加复杂,含有大量腐殖质、蛋白质、糖、脂质等非磷酸根的含氧杂质,因此建立一种适用于湖泊沉积物的磷酸盐氧同位素前处理方法尤为重要.
为了探明NaClO处理和H2O2处理等除有机碳方法,Blake法和McLaughlin法等纯化方法在湖泊沉积物磷酸盐氧同位素前处理中的效果,本文对这几种方法进行了对比研究.首先,采用2.5% NaClO和30% H2O2对有机质含量较高的湖泊沉积物样品进行预处理,并比较2种预处理对无机磷提取效率、提取液中溶解性有机碳(DOC)含量以及沉积物磷形态的影响.其次,运用Blake法和McLaughlin法对沉积物提取液中磷酸盐进行纯化,比较2种方法中DOC的去除效率和磷酸盐的回收率.本文结合预处理除碳方法和2种纯化方法的优点,并对一些操作步骤进行筛选优化,建立一种适用于湖泊沉积物磷酸盐氧同位素的前处理方法.
1 材料与方法 1.1 试剂与仪器试剂:NaClO(Aladdin)、H2O2(AR)、HCl(GR)、Mg(NO3)2·6H2O(AR)、NaOH(GR)、HNO3(GR)、(NH4)6Mo7O24·4H2O(AR)、CeNO3(Aladdin)、阳离子交换树脂(BioRad AG-50X8,H+型,100~200目)、阴离子交换树脂(BioRad AG1-X8,OH-型,200~400目)、NaHCO3(Aladdin)、MgCl2(AR)、BD试剂、CH3COOK·3H2O(GR)、CH3COOH(AR).
器皿及仪器:聚四氟乙烯(PTFE)离心管、100 ml烧杯、1 L烧杯、10 ml玻璃离心管、恒温振荡器(HZ-9511K)、冷冻干燥机(7948030,Labconco)、离心机(TGL-16M,湘仪)、马弗炉(KBF1700)、带砂芯的层析柱、总有机碳分析仪(Torch,Teledyne Tekmar)、元素分析仪(EA3000,EuroVector).
1.2 样品采集丹麦富营养化湖泊Nordborg湖平均水深5 m,湖面面积0.546 km2,换水周期为0.82 a[16].流域面积63%为农田,25%为城镇用地,其他区域被森林覆盖.湖北岸设有两个前置库,拦截净化农田来水.于2014年3月12日用彼得森采泥器进行表层沉积物样品采集. 4个样品分别位于Nordborg湖最深处(8.5 m)、1/2水深处(4.2 m)、前置库KS1和前置库KS2,记为样品1、样品2、样品3和样品4. 4个沉积物样品的碳、氮、磷含量如表 1所示.
| 表 1 丹麦Nordborg湖沉积物样品的碳、氮、磷含量 Tab.1 The contents of C, N, P of four samples in Nordborg Lake |
将沉积物样品冻干后研磨过200目筛.分别取0.5 g左右样品于PTFE离心管中,设置3个实验组:对照组、NaClO处理组和H2O2处理组.每组处理3个平行.具体步骤如下:
对照组:不进行任何预处理.
NaClO处理组:加入10 ml 2.5% NaClO溶液震荡24 h后离心(7000转/min, 10 min),弃去上清液,剩余残渣用纯水洗涤4~5次至中性.
H2O2处理组:加入10 ml 30% H2O2溶液浸泡24 h后,待无明显气泡生成后离心(7000转/min, 10 min),弃去上清液,剩余残渣用纯水洗涤4~5次至中性.
选取部分预处理后样品残渣,用1 mol/L HCl提取无机磷,其余样品残渣按照连续萃取法(SEDEX)提取5种形态磷(即弱交换态磷Ex-P、铁铝结合态磷Fe-P、自生磷灰石CFAP、碎屑磷灰石CAP、闭蓄态磷Org-P)[17].按照钼锑抗分光光度法测定各提取液中PO43--P含量[18],并且用总有机碳分析仪测定无机磷提取液中的DOC浓度.
1.3.2 纯化方法以样品3为例,分别按照Blake法和McLaughlin法对沉积物提取液进行纯化处理,并测定每一步的DOC浓度和磷含量,最后测定产物Ag3PO4的C、N含量.每组处理7个平行.
Blake方法[19]:依次经过2次氢氧化镁共沉淀(MAGIC)、磷钼酸铵沉淀、磷酸铵镁沉淀、阳离子交换树脂吸附金属离子、阴离子交换树脂除去有机质、阳离子交换树脂除HCO3-、微沉淀生成Ag3PO4,60℃烘干待测.
McLaughlin方法:参照McLaughlin方法[12],并结合卢阳阳等的方法进行改进[13].依次经过阳离子交换树脂除去Fe、Al、Ca等金属离子、1次MAGIC操作、CePO4沉淀、阳离子交换树脂除去Ce3+、阴离子交换树脂除去有机质、加酸除去HCO3-,快速沉淀生成Ag3PO4,60℃烘干待测.
1.4 数据统计与分析采用Origin 9.0软件进行图形绘制,并用SPSS 20.0软件对数据进行统计分析.
2 结果与讨论 2.1 不同预处理方法的比较 2.1.1 不同预处理方法对DOC去除效果的影响经NaClO处理后无机磷提取液中DOC浓度减少了32%~74%;H2O2对DOC的去除效果不稳定,经H2O2处理后样品1和样品4的无机磷提取液中DOC浓度分别减少了10%和55%,但是样品2和样品3的DOC浓度却分别增加了21%和70%.对比2种预处理方法对样品DOC的去除结果发现,两者差异显著(P=0.01),且NaClO处理对DOC去除效果优于H2O2(图 1a).这与土壤方面的相关研究结果一致,在去除土壤有机质时NaClO比H2O2更有效[20-23].

|
图 1 2.5% NaClO和30% H2O2预处理后沉积物提取液中DOC浓度(a)和无机磷含量(b)的变化 Fig.1 Variation of DOC concentration(a) and inorganic phosphate content(b) in sediments extracts after 2.5% NaClO and 30% H2O2 pretreatments |
NaClO去除天然有机质时,ClO-直接与腐殖酸、富里酸、芳香族化合物等发生氯化反应,生成CHCl3、氯代乙酸等[24-26].而且NaClO溶液呈碱性,可将部分腐殖酸和富里酸洗脱出来,从而减少无机磷提取液中DOC浓度.
H2O2稳定性较差,可被沉积物中的Fe3+和锰氧化物催化分解[27],从而减弱对有机质的降解作用[28].腐殖质、木质素以及一些简单的碳水化合物与H2O2反应会生成大量小分子有机酸(如蚁酸、乙酸、乙二酸、丙二酸)、苯酚、苯甲酸[29].样品2和样品3的无机磷提取液中DOC浓度升高可能是因为H2O2将沉积物样品中部分难降解有机质转化成水溶性有机酸.
2.1.2 不同预处理方法对沉积物磷形态的影响NaClO对沉积物磷形态的影响小于H2O2.经NaClO处理后,无机磷提取率维持在93%~98%(图 1b),但沉积物的总磷减少14%~29%(图 2),表明NaClO对有机磷有明显的去除效果而对无机磷几乎无影响.经H2O2处理后,除样品1总磷减少30%外,其他3种样品的总磷与对照组几乎没有差异(图 2),但无机磷的提取率提高了35%~64%(图 1b),表明H2O2将有机磷转化为无机磷.

|
图 2 2.5% NaClO和30% H2O2预处理后沉积物磷形态的变化 Fig.2 Variations of sediments phosphates species after 2.5% NaClO and 30% H2O2 pretreatments |
比较NaClO和H2O2处理后沉积物磷赋存形态的变化可得,NaClO和H2O2处理组的Ex-P分别减少了29%~86%和86%~90%,说明Ex-P更易受H2O2破坏(P=0.039). Ex-P一般通过物理吸附作用或者磷酸盐与沉积相胶体、矿物通过配位交换的方式吸附在沉积物表面[30],极易因环境的改变而释放.实验过程中,NaClO与沉积物反应缓和,而H2O2与沉积物反应时却有大量气泡冒出,激烈的气泡涌动可能促进了Ex-P的释放.但由于Ex-P仅占总磷的1%~3%,因此Ex-P的变化对无机磷提取率的影响可忽略.
除样品4外,NaClO处理组和H2O2处理组的Fe-P含量变化几乎无差异(P=0.666),分别减少了43%~61%和37%~65%. Fe-P是指铁铝氧化物表面及氧化物晶格包裹的磷,包括无定型氧化铁(FeOOH)-P胶体. FeOOH-P最稳定的pH范围为6.5~8.0,在高pH或低pH条件下,都易将PO43-释放出来[31]. NaClO水解产生OH-,可促进Fe-P的释放.考虑到pH值较高的NaClO溶液对含铝氧化物的溶解作用,Siregar等[22]建议将pH下调至8左右以减少对晶体矿物结构的破坏. 30%H2O2呈弱酸性(pH为5~6),对FeOOH-P有一定的溶解作用,使Fe-P转化成其他形态的磷. H2O2处理组中样品4的Fe-P含量升高可能是因为其他形态的磷转化成了Fe-P,且此转化量大于H2O2对FeOOH-P的溶解量.
NaClO对CFAP和CAP影响不大,含量波动范围分别为-9%~6%和-4%~3%. CFAP和CAP主要是CaCO3结合态的磷,稳定性较强,不易释放[3]. H2O2使这2种磷形态的磷含量明显增加,其中CFAP增加了21%~65%;CAP除样品3变化较小,仅减少了4%外,其它样品增加了32%~182%,其原因可能是H2O2在氧化有机质的过程中将有机磷转化为无机磷.
与对照组相比,经过NaClO和H2O2处理后Org-P含量分别减少了47%~69%和82%~96%.这表明NaClO和H2O2均对Org-P有明显影响,且H2O2处理对Org-P影响更明显(P=0.020).
2.2 两种经典方法的纯化效率对比 2.2.1 有机质去除率比较Blake法和McLaughlin法对PO43-提取液的纯化效果可得,两种方法均使有机质含量降低,但是趋势不同(图 3).按照Blake法处理后DOC浓度呈逐步降低的趋势,而McLaughlin法中DOC浓度却波动较大.

|
图 3 Blake法和McLaughlin法对有机质去除效率对比 Fig.3 Comparison of organic matter removal efficiency between Blake and McLaughlin methods |
Blake法和McLaughlin法分别采用2次MAGIC和1次MAGIC操作,DOC浓度分别减少了42.03%和33.98%,二者相差8.04%,表明第2次MAGIC操作对DOC的去除作用有限.这可能与Mg(OH)2沉淀对有机质的吸附作用有关,在2次MAGIC操作中Mg(OH)2沉淀量基本不变,故吸附的有机质含量变化不大,减少的部分可能是被NaOH清洗掉的碱溶性有机质.由于MAGIC操作复杂,且耗时长,因此,建议只采用1次MAGIC.
在利用特征沉淀对样品进行纯化的步骤中,Blake法与McLaughlin法分别采用了APM+MAP沉淀和CePO4沉淀,但是二者对有机质的去除效果有显著差异(P=0.007).经APM+MAP沉淀处理后,样品中DOC浓度减少至7.74±1.13 mg/L,约为提取液DOC浓度的12.70%;而CePO4沉淀却使DOC浓度升高至提取液的2倍. Blake法中APM和MAP沉淀分别选用5% NH4NO3和1 :20氨水进行洗涤,2种试剂可分别去除酸溶性有机质和碱溶性有机质,从而使DOC浓度下降. McLaughlin法中DOC浓度升高的原因可能是在第一步中阳离子交换树脂用量不足,导致金属离子无法完全去除,在CePO4沉淀的过程中,生成金属氢氧化物.在洗涤沉淀的过程中,大量CH3COOK会吸附于沉淀,且固液分离时有少量CH3COOK溶液仍滞留在离心管内,导致DOC浓度升高.
经过阴离子交换树脂处理后,Blake法处理的样品中DOC浓度几乎没有变化,表明在DOC浓度较低的情况下,阴离子树脂对有机质的去除效果不明显.因此,建议省略阴离子交换树脂处理. McLaughlin法处理的样品中DOC浓度减少至22.63±7.98 mg/L,约为提取液中DOC浓度的1/3,但仍明显高于Blake法的处理结果. CH3COOH和PO43-对阴离子交换树脂的相对选择性十分接近,分别为5.0和3.2(BIO-RAD公司),部分CH3COOH会随PO43-一同发生吸附解吸而无法去除,从而导致DOC浓度较高.
2.2.2 不同方法的磷回收率比较Blake法和McLaughlin法对磷的总回收率接近,但Blake法稳定性较好(表 2). MAGIC法几乎不造成磷损失,且1次操作与2次操作结果没有显著性差异(P=0.126). CePO4沉淀与APM+MAP沉淀的回收率基本一致,但CePO4沉淀操作相对复杂,因CePO4沉淀受pH影响较大,McLaughlin研究得出pH=5.5时效果最好[12].通常,沉积物提取液中含有大量的Fe、Al、Ca等金属离子,在pH调节过程中极易产生金属离子的氢氧化物沉淀,从而干扰CePO4沉淀的生成.在本实验中,为了降低金属离子的干扰作用,在MAGIC操作前增加了阳离子树脂除去杂质金属离子,以便更好地生成CePO4.阳离子树脂对回收率的影响较小,少量的PO43-会残留在树脂表面,纯水多次冲洗即可提高回收率.阴离子树脂对回收率的影响较大,按照阴离子树脂对抗衡离子的选择性顺序,HSO4-、NO3-等杂质离子会优先吸附到树脂上,减少了PO43-与树脂结合的机会,未能吸附到阴离子树脂上的PO43-将随废液损失掉;此外,阴离子树脂操作复杂,耗时长,且对树脂的用量要求较高,树脂不足会增加磷损失的机率.
| 表 2 各步骤磷回收率比较 Tab.2 Overall phosphate throughput during purification |
按照Blake法,将纯化后的溶液蒸发浓缩,加入银氨溶液后加热使氨水挥发析出Ag3PO4,亮黄色的结晶浮于溶液表面.按照McLaughlin法,调节pH至7~8,加入AgNO3溶液,迅速生成黄白色的Ag3PO4沉淀,沉淀随时间慢慢变暗.
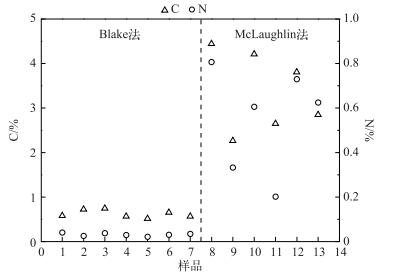
为了比较Ag3PO4纯度,分别对2种方法得到的Ag3PO4进行C、N含量测定(图 4).其中1~7和8~13分别代表用Blake法和McLaughlin法纯化样品3得到的Ag3PO4平行样.经Blake法纯化获得的Ag3PO4的C、N含量分别为0.622%±0.081%和0.032%±0.006%;经McLaughlin法纯化获得的Ag3PO4的C、N含量分别为3.37%±0.82%和0.55%±0.21%,分别是Blake法的5.4和17.2倍,说明Blake法的纯化效果更好,重现性高,效果稳定.这与Tamburini等[15]的研究结果一致. Tamburini等在分析不同有机质含量的土壤样品的δ18OP时发现,通过McLaughlin法纯化获得的Ag3PO4中含有有机质,且对后续的氧同位素测定有干扰;慢沉淀可以减少有机质的混入和对δ18OP测定的影响[15].
|
图 4 经Blake法和McLaughlin法获得的Ag3PO4的C、N含量对比 Fig.4 Comparison of C and N contents of Ag3PO4 through Blake and McLaughlin methods |
1) NaClO处理可以保证较高的无机磷提取效率,同时能有效地减少无机磷提取液中有机质含量,且对不同形态磷的破坏较小;H2O2对有机质的去除效果不稳定,处理后沉积物的磷形态之间发生转化.因此,NaClO法更适用于湖泊沉积物样品的预处理.
2) Blake法对有机质的去除率高于McLaughlin法;2种方法的磷回收率差异不大,但Blake法稳定性较好. Blake法和McLaughlin法得到的Ag3PO4中C、N含量的对比分析表明, Blake法的纯化效果更好且更稳定.
3) 结合NaClO法与Blake法的优点,建立了一种适合湖泊沉积物的磷酸盐氧同位素前处理方法(图 5).首先用2.5% NaClO对沉积物样品进行除碳预处理,然后对磷酸盐提取液依次通过氢氧化镁共沉淀(MAGIC)、APM+MAP沉淀、阳离子交换树脂处理,最后生成Ag3PO4.

|
图 5 湖泊沉积物磷酸盐氧同位素前处理流程图 Fig.5 Procedure for pretreatment of oxygen isotope composition of phosphate in lake sediments |
| [1] |
Li Bo. Ecology. Beijing: Higher Education Press, 2000, 251-252. [李博. 生态学. 北京: 高等教育出版社, 2000, 251-252.]
|
| [2] |
Fan Chengxin. Physiochemical characteristics of sedimets in Gehu Lake and simulation of its phosphorus release. J Lake Sci, 1995, 7(4): 341-349. [范成新. 滆湖沉积物理化特征及磷释放模拟. 湖泊科学, 1995, 7(4): 341-349. DOI:10.18307/1995.0408] |
| [3] |
Song Yuanyuan, Feng Muhua, Su Zhengguang et al. Vertical distribution of chemical speciation of phosphorus in sediments from different sources of Fuxian Lake. Acta Scientiae Circumstantiae, 2013, 33(9): 2579-2589. [宋媛媛, 冯慕华, 苏争光等. 抚仙湖不同来源沉积物磷形态垂向分布特征. 环境科学学报, 2013, 33(9): 2579-2589.] |
| [4] |
Davies CL, Surridge BW, Gooddy DC. Phosphate oxygen isotopes within aquatic ecosystems:Global data synthesis and future research priorities. Science of the Total Environment, 2014, 496: 563-575. DOI:10.1016/j.scitotenv.2014.07.057 |
| [5] |
Liang Y, Blake R. Oxygen isotope signature of Pi regeneration from organic compounds by phosphomonoesterases and photooxidation. Geochimica et Cosmochimica Acta, 2006, 70(15): 3957-3969. DOI:10.1016/j.gca.2006.04.036 |
| [6] |
Mclaughlin K, Paytan A, Kendall C et al. Phosphate oxygen isotopes as a tracer for sources and cycling of phosphate in San Francisco Bay. Journal of Geophysical Research, 2006, 111: G03003. |
| [7] |
Jaisi DP, Blake RE. Tracing sources and cycling of phosphorus in Peru Margin sediments using oxygen isotopes in authigenic and detrital phosphates. Geochimica et Cosmochimica Acta, 2010, 74(11): 3199-3212. DOI:10.1016/j.gca.2010.02.030 |
| [8] |
Goldhammer T, Brunner B, Bernasconi SM et al. Phosphate oxygen isotopes:Insights into sedimentary phosphorus cycling from the Benguela upwelling system. Geochimica et Cosmochimica Acta, 2011, 75(13): 3741-3756. DOI:10.1016/j.gca.2011.04.006 |
| [9] |
Stephan E. Oxygen isotope analysis of animal bone phosphate:Method refinement, influence of consolidants, and reconstruction of palaeotemperatures for holocene sites. Journal of Archaeological Science, 2000, 27: 523-535. DOI:10.1006/jasc.1999.0480 |
| [10] |
O'Neil JR, Roe LJ, Reinhard E et al. A rapid and precise method of oxygen isotope analysis of biogenic phosphate. Israel Journal of Earth Sciences, 1994, 43(3/4): 203-212. |
| [11] |
Blake RE, Chang SJ, Lepland A. Phosphate oxygen isotopic evidence for a temperate and biologically active Archaean ocean. Nature, 2010, 464(7291): 1029-1032. DOI:10.1038/nature08952 |
| [12] |
Mclaughlin K, Silva S, Kendall C et al. A precise method for the analysis of δ18O of dissolved inorganic phosphate in seawater. Limnology and Oceanography:Methods, 2004, 2(7): 202-212. DOI:10.4319/lom.2004.2.202 |
| [13] |
Lu Yangyang, Zheng Zhenzhen, Yin Xijie et al. The measurement of oxygen isotope composition of dissolved inorganic phosphate in seawater. Acta Geoscientica Sinica, 2012, 33(6): 961-966. [卢阳阳, 郑珍珍, 尹希杰等. 海水溶解磷酸盐氧同位素组成的测定. 地球学报, 2012, 33(6): 961-966. DOI:10.3975/cagsb.2012.06.16] |
| [14] |
Mclaughlin K, Cade-Menun BJ, Paytan A. The oxygen isotopic composition of phosphate in Elkhorn Slough, California:A tracer for phosphate sources. Estuarine, Coastal and Shelf Science, 2006, 70(3): 499-506. DOI:10.1016/j.ecss.2006.06.030 |
| [15] |
Tamburini F, Bernasconi S, Angert A et al. A method for the analysis of the δ18O of inorganic phosphate extracted from soils with HCl. European Journal of Soil Science, 2010, 61(6): 1025-1032. DOI:10.1111/ejs.2010.61.issue-6 |
| [16] |
Egemose S, De Vicente I, Reitzel K et al. Changed cycling of P, N, Si, and DOC in Danish Lake Nordborg after aluminum treatment. Canadian Journal of Fisheries and Aquatic Sciences, 2011, 68(5): 842-856. DOI:10.1139/f2011-016 |
| [17] |
Zhang JZ, Guo L, Fischer CJ. Abundance and chemical speciation of phosphorus in sediments of the Mackenzie River Delta, the Chukchi Sea and the Bering Sea:Importance of detrital apatite. Aquatic Geochemistry, 2010, 16(3): 353-371. DOI:10.1007/s10498-009-9081-4 |
| [18] |
Editorial Board of Water and Wastewater Monitoring and Analysis Methods, Ministry of Environmental Protection of the People's Republic of China. Water and wastewater monitoring and analysis methods:4th edition. Beijing: China Environmental Science Press, 2002. [国家环境保护总局《水和废水监测分析方法》编委会. 水和废水监测分析方法:第4版. 北京: 中国环境科学出版社, 2002.]
|
| [19] |
Blake RE, Chang SJ, Lepland A. Phosphate oxygen isotopic evidence for a temperate and biologically active Archaean ocean. Nature, 2010, 464(7291): 1029-1032. DOI:10.1038/nature08952 |
| [20] |
Lavkulich LM, Wiens JH. Comparison of organic matter destruction by hydrogen peroxide and sodium hypochlorite and its effects on selected mineral constituents. Soil Science Society of America Journal, 1970, 34: 755-758. DOI:10.2136/sssaj1970.03615995003400050025x |
| [21] |
Mikutta R, Kleber M, Kaiser K et al. Review:Organic matter removal from soil using hydrogen peroxide, sodium hypochlorite, and disodium peroxodisulfate. Soil Science Society of America Journal, 2005, 69: 121-135. |
| [22] |
Siregar A, Kleber M, Mikutta R et al. Sodium hypochlorite oxidation reduces soil organic matter concentrations without affecting inorganic soil constituents. European Journal of Soil Science, 2005, 56(4): 481-490. DOI:10.1111/ejs.2005.56.issue-4 |
| [23] |
Anderson J. An improved pretreatment for mineralogical analysis of samples containing organic matter. Clays and Clay Minerals, 1963, 10(3): 380-388. |
| [24] |
Jimenez MCS, Dominguez AP, Silverio JMC. Reaction kinetics of humic acid with sodium hypochlorite. Water Research, 1993, 27(5): 815-820. DOI:10.1016/0043-1354(93)90145-8 |
| [25] |
Li CW, Benjamin MM, Korshin GV. Use of UV spectroscopy to characterize the reaction between NOM and free chlorine. Environmental Science & Technology, 2000, 34(12): 2570-2575. |
| [26] |
Pomes ML, Larive CK, Thurman EM et al. Sources and haloacetic acid/trihalomethane formation potentials of aquatic humic substances in the Wakarusa River and Clinton Lake near Lawrence, Kansas. Environmental Science & Technology, 2000, 34(20): 4278-4286. |
| [27] |
Strukul G. Catalytic oxidations with hydrogen peroxide as oxidant. Dordrecht: Kluwer Academic Publisher, 1992, 97-98.
|
| [28] |
Wang GS, Liao CH, Wu FJ. Photodegradation of humic acids in the presence of hydrogen peroxide. Chemosphere, 2001, 42(4): 379-387. DOI:10.1016/S0045-6535(00)00153-3 |
| [29] |
Chakrabartty S, Kretschmer H, Cherwonka S. Hypohalite oxidation of humic acids. Soil Science, 1974, 117(6): 318-322. DOI:10.1097/00010694-197406000-00003 |
| [30] |
Yin Ran, Wang Fushun, Mei Hangyuan et al. Distribution of phosphorus forms in the sediments of cascade reservoirs with different trophic states in Wujiang catchment. Chinese Journal of Ecology, 2010, 29(1): 91-97. [尹然, 汪福顺, 梅航远等. 乌江流域不同营养水平的梯级水库沉积物中磷形态特征. 生态学杂志, 2010, 29(1): 91-97.] |
| [31] |
Pan B, Wu J, Pan B et al. Development of polymer-based nanosized hydrated ferric oxides (HFOs) for enhanced phosphate removal from waste effluents. Water Research, 2009, 43(17): 4421-4429. DOI:10.1016/j.watres.2009.06.055 |
 2017, Vol. 29
2017, Vol. 29 


