(2: 中国科学院重庆绿色智能技术研究院, 中国科学院水库水环境重点实验室, 重庆 400714)
(3: 重庆大学城市建设与环境工程学院, 重庆 400045)
(2: CAS Key Lab of Reservoir Environment, Chongqing Institute of Green and Intelligence Technology, Chinese Academy of Sciences, Chongqing 400714, P.R.China)
(3: College of Urban Construction and Environmental Engineering, Chongqing University, Chongqing 400045, P.R.China)
全球内陆水域面积约仅为陆地总面积的2%,但由于受到高强度的人类活动胁迫,其在全球碳循环中所占的比重不可忽略[1].河流作为连接陆地和海洋生态系统两大碳库的重要环节,成为全球碳循环研究的一个重要组成部分.一方面河流直接向海洋输送大量的含碳物质,据统计,河流每年以溶解态和颗粒态向海洋输人约1 Gt C,其中,有机碳40%、无机碳60%[1]; 另一方面河流通过水-气界面向大气释放或吸收CO2、CH4[2-5],其中释放的CO2估算至少能达到107 t/a的数量级[6].因此,正确评价河流水-气界面CO2与CH4的交换通量对于深入系统的理解河流在全球或区域碳循环中的角色,总体把握河流的碳收支状况是非常重要的.
通常,对水-气界面间气体交换通量的监测方法有涡度相关法、模型估算法、浮游箱法和遥感反演法等[7],其中,模型估算法因其简单、灵活、易操作等特点在野外现场监测中最为常用.在原理上,模型估算法根据空气和水体内气体浓度梯度差运用Fick定律来估算通量,气体在两介质中的浓度及其传质系数的确定是该方法的核心[8-10].
金沙江是长江的上游河段,流经云贵高原西北部、川西南山地,到四川盆地西南部的宜宾接纳岷江为止,全长2326 km,流域面积47.3×104 km2.水-气界面气体交换过程不仅受到风速、温度等的影响,且同所在水域的水深、水域面积等密切相关.在该水域实际运用模型估算法监测水-气界面温室气体(CO2、CH4)交换通量,需充分考虑前述因素的影响,但目前鲜有报道.本文以金沙江下游为研究对象,即攀枝花至宜宾段,2015年8月汛期对金沙江下游进行现场监测,获得表层水体CO2与CH4分压及各环境参数的实测资料,利用薄边界层模型估算夏季水-气界面CO2与CH4的交换通量,并初步分析了环境变量与分压及通量的相关性.当前,金沙江下游正在建设乌东德、白鹤滩水电站,已建成溪洛渡、向家坝水电站,随着水电站的建设运行,金沙江流域的碳循环可能将发生变化,故对金沙江下游流域展开水-气界面研究,对揭示该流域水电站建成后碳循环变化具有重要的意义.
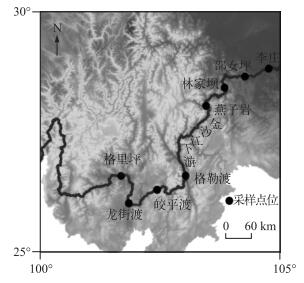
1 材料与方法 1.1 研究区域金沙江下游,即攀枝花至宜宾段,长约768 km,落差719 m,除小部分属攀枝花市、宜宾市和云南楚雄所辖外,大部分为川滇界河.河段两侧山地年降水量约为900~1300 mm,相应径流深为500~900 mm,特别是大凉山地区年降水量高达1500 mm以上,径流深达1200~1400 mm.采样点位从上游到下游分别为格里坪、龙街渡、皎平渡、格勒渡、燕子岩、林家坝、邵女坪、李庄. 2015年8月8-18日沿程利用当地小船采集水样.金沙江流域天然河段因水流湍急,故在水体样品采集中,选择在河道中心采样.采样期间,同步采集相关环境参量指标.金沙江下游采样点位示意图见图 1,每个采样点具体采样时间见表 1,邵女坪、格勒渡采样点实景照片见图 2.
|
图 1 金沙江下游采样点位示意 Fig.1 Sketch of the sampling sites in the downstream of Jinsha River |

|
图 2 金沙江下游邵女坪(a)、格勒渡(b)采样点实景照片 Fig.2 Photoes of the sampling sitess of Shaonvping(a) and Geledu(b) of the downstream of Jinsha River |
| 表 1 金沙江下游各采样点情况 Tab.1 The characteristics of sampling spots in the downstream of Jinsha River |
对于水-气界面温室气体监测,目前常用的有两种方法,一种为静态箱-气相色谱法,另一种为顶空平衡法-气相色谱法与薄边界层模型(TBL)估算法结合.但静态箱-气相色谱法在有风或流动水体的观测条件下,箱体与表层水体的摩擦引起的扰动,可能导致额外的温室气体排放,影响观测结果的准确性[11],且劳动强度大,不适宜开展大区域、长期的观测[12],因此静态箱法只适用于对静态水体的观测.考虑到金沙江水流湍急,采样点位之间距离远,且点位的地理与气候条件差,不适用静态箱法展开研究.故本研究采用顶空平衡法与TBL模型估算法对金沙江下游水-气界面温室气体展开监测研究.
1.3 顶空平衡法原理顶空平衡法的原理是在装有水样和初始惰性气体的密封玻璃瓶中,通过剧烈摇晃使水体内气体浓度与上方空气中气体浓度达到平衡,测量上方空气中气体的浓度值而得到平衡前水体待测气体的分压[13].其计算公式为[14]:
| $\begin{split} p\left(\text{Gas}\right)=\frac{p_{\text{final}}·K_{\text{equilibrium}}+(HS/S)\frac{p_{\text{final}}-p_{\text{initial}}}{V_\text{m}}}{K_{\text{sample}}} \end{split}$ | (1) |
式中, p(Gas)为待测水样中气体分压(μatm);pinitial和pfinal分别为平衡前后瓶内上方空气中待测气体分压,(μatm);HS/S为瓶内气体与水体体积比;Vm为气体的摩尔体积(mol/L); Ksample和Kequilibrium分别为采样时和样品分析前瓶内水温条件下对应的待测气体溶解度(mol/(L·atm)),不同气体其亨利系数可通过下式计算[15-16]:
| $\begin{split} \text{ln}K_0(\text{CO}_2)=-58.0931+90.5069\frac{100}{T_\text{K}}+22.294 \text{ln}\left(\frac{T_\text{K}}{100}\right)+\\ s\left(0.027766-0.02588\frac{T_\text{K}}{100}+0.0050578\frac{T_\text{K}}{100}^2\right) \end{split}$ | (2) |
| $\begin{split} \text{ln}K_0(\text{CH}_4)=-115.6477+\frac{155.5756}{T_\text{K}/100}+65.2553 \text{ln}\left(\frac{T_\text{K}}{100}\right)-6.1698\frac{T_\text{K}}{100} \end{split}$ | (3) |
式中,TK为水体绝对温度(K);s为盐度(ng/L),在淡水系数中该值可为0;对于CH4来说,上式得到的结果再乘以系数1000 g/L/18.0 g/mol便可转换成mol/(L·atm)的单位.
其中Vm可由下式进行换算[17]:
| $\begin{split} V_\text{m}=1×0.082057×(273.15+T)\frac{101.325}{P} \end{split}$ | (4) |
式中,T为采样时的水温(℃);p为采样时的大气压力(kPa).
1.4 水-气界面通量估算原理水-气界面气体交换通量主要受以下几个因素的影响:1)表层水体气体的分压;2)气体传质系数,而气体传质系数又受流速、风速、温度等因素的影响.根据Fick定律,对于淡水水体,水-气界面气体交换通量(正为释放、负为吸收)可由式(5)计算得出[12]:
| $\begin{split} Flux=k_\text{x}\left(C_{\text{water}}-C_{\text{air}}\right) \end{split}$ | (5) |
式中, Flux为温室气体(CO2、CH4)扩散通量(mmol/(m2·h));kx为气体交换系数(cm/h);Cwater为气体在水中的浓度(mmol/L);Cair为现场温度及压力下大气中温室气体的饱和浓度(mmol/L).
对于交换系数kx的估算,目前通用的2种模型分别是薄边界层模型(TBL)和表面更新模型(SRM). TBL模型是假定气体转移是由水表面的薄边界层控制的水-气界面的浓度与大气中气体浓度形成溶解平衡;而SRM模型是假定水面漩涡可取代水表面薄层,且取代速度决定于水的被搅动程度.目前世界范围内对kx系数的确定绝大多数采用的是1989年Jähne B等建立的数学经验公式[18]:
| $\begin{split} k_\text{x}=k_{600}{\left(\frac{600}{Sc}\right)^{0.67}} \end{split}$ | (6) |
式中, k600为六氟化硫(SF6)气体的交换系数(cm/h);考虑采样点位均属于已建或在建水电站的库区范围,故本研究采用对于湖泊、水库生态系统的交换系数,其中CO2选用Cole等在1998年建立的经验公式[19]:
| $\begin{split} k_{600}=2.07+0.215U^{1.7}_{10} \end{split}$ | (7) |
CH4选用Macintyre等建立的经验公式[20]:
| $\begin{split} k_{600}=0.45U^{1.64}_{10} \end{split}$ | (8) |
Sc为t℃下CO2、CH4的Schmidt常数,对淡水而言,可按下式进行计算[21-22]:
| $\begin{split} Sc\left(\text{CO}_2\right)=1911.1-118.11t+3.4527t^2-0.04132t^3 \end{split}$ | (9) |
| $\begin{split} Sc\left(\text{CH}_4\right)=1897.8-114.28t+3.2902t^2-0.03906t^3 \end{split}$ | (10) |
U10为水面上方10 m处的风速(m/s).通常现场监测所得的水体上方风速U1可用下式进行换算[24]:
| $\begin{split} U_{10}=1.22U_1 \end{split}$ | (11) |
监测得到的温室气体在水中的分压乘以亨利系数,便可以得到温室气体在水中的饱和浓度Cwater.计算公式为[24-25]:
| $\begin{split} C_{\text{water}}=K_0·p(\text{Gas}) \end{split}$ | (12) |
式中,K0为亨利系数,即气体溶解度(mol/(L·atm));p(Gas)为当前水温下的气体分压(μatm).
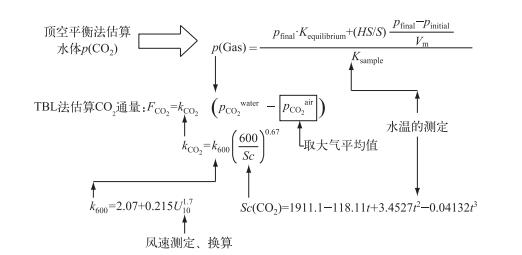
1.5 采样与分析方法水样用水质取样器采集,每个点位只取0.5 m处的表层水,顶空瓶置于采水器中,以淹没状态进行密封,采集的水样与顶空瓶均低温保存;pH、电导率、盐度采用YSI野外多参仪现场测定;气温、大气压来自手持式数字大气压计现场测定;碱度(TA)采用HACH公司的微量滴定器及标准硫酸溶液现场滴定(精度1.25 μl);光合作用有效强度采用LI-COR19OSA光量子仪现场测定;太阳辐射强度来自照度计;水温及溶解氧(DO)浓度采用YSIProODO溶解氧仪测定(精度分别为0.1℃、0.01 mg/L)现场测定;叶绿素a(Chl.a)浓度采用丙酮萃取分光光度法;溶解性总氮(DTN)及溶解性无机碳(DIC)浓度:水样过450℃烘干4 h的Whatman GF/F玻璃纤维滤纸,用岛津TOC-V总碳分析仪分析过滤液测定[26];溶解性总磷(DTP)浓度采用过硫酸钾氧化-分光光度计法测定;水体中p(CO2)与p(CH4)根据亨利系数、水温、大气压、顶空瓶气液体积比5/7,通过安捷伦7820A气相色谱仪,利用顶空平衡法计算得出;对于kx的确定,根据小型气象站测定的水面上方瞬时风速(U1)(精确度0.1 m/s),并根据式(11)换算成水面上方10 m处的风速(U10,m/s)、水温计算出的Schmidt常数;对于大气中的Cair,金沙江下游受农田、湿地、人为等因素影响很小,参考桂祖胜[27]、张龙军等[28]对黄河以及长江干流的研究,本研究取大气CO2平均浓度390.5 mg/L、CH4平均浓度1.803 mg/L(数据来自IPCC第五次评估报告).野外测量仪器在采样工作前都已经过标准校正程序,具体的模型实施技术路线见图 3.
|
图 3 模型估算法(顶空平衡)计算示意 Fig.3 The process of model calculated method (the headspace equilibrium) |
本研究的实验分析及计算所得数据全部录入SPSS©或Origin©进行统计分析,采用Spearman相关性分析对p(CO2)、p(CH4)、CO2通量、CH4通量及各理化指标(pH、TA、DO、水温、Chl.a、DIC等)进行回归分析,说明数据间变化的线性相关性.
2 结果与分析 2.1 环境因子的变化 2.1.1 水温与pH2015年8月,金沙江下游的水温沿程波动不大,最低温出现在龙街渡样点, 为21.7℃,最高温出现在皎平渡样点, 23.6℃.金沙江下游表层水体pH的沿程分布特征大致与水温一致,龙街渡样点为8.08,格勒渡样点为8.34 mg/L(图 4a).

|
图 4 金沙江下游水体环境因子沿程分布特征 Fig.4 Variation of streamwise of environment factors in the water of the downstream of Jinsha River |
2015年8月,金沙江下游表层水体的Chl.a浓度在邵女坪样点和燕子岩样点相对较高,分别为4.56和4.12 mg/L,分析邵女坪与燕子岩分别在向家坝水电站与溪洛渡水电站的坝前附近的库区范围,其水体的浮游植物相对较多,其中两大坝之间位于库区的林家坝样点也Chl.a浓度较高,达到2.2 mg/L,而其他点位的Chl.a浓度较低,这可能是因为金沙江水流湍急,含沙量大,不利于浮游植物的生长.而TA无明显变化规律,沿程分布大致相当(图 4b).
2.1.3 DTN与DTP浓度2015年8月,金沙江下游表层水体DTP浓度整体较低,其中燕子岩、林家坝、邵女坪样点位于库区,浮游植物生长旺盛(见Chl.a),对磷的吸收充分,因此DTP浓度相对其他点位较低. DTN浓度则无明显变化规律,沿程大致相当(图 4c).
2.1.4 DO与DIC浓度2015年8月,金沙江下游表层水体DO浓度沿程分布大致相当,无明显变化规律,DIC浓度在格里坪相对最高,达到54.43 mg/L,其余各点位大致相当,无明显变化规律(图 4d).
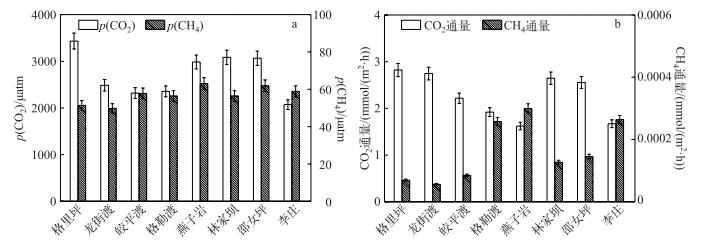
2.2 表层p(CO2)与p(CH4)和水-气界面通量2015年8月,金沙江下游表层水体p(CH4)沿程大致相当,无明显变化趋势,且整体分压不高,最高值出现在燕子岩样点(63.07 μatm),最低值出现在龙街渡样点(49.80 μatm),平均值为59.96±6.74 μatm.而p(CO2)无明显变化规律,在格里坪与燕子岩、林家坝、邵女坪样点相对较高,最高出现在格里坪样点(3433.10 μatm),最低出现在李庄样点(2070.91 μatm),平均值为2724.84±477.18 μatm(图 5a).水-气界面CH4通量全为正值,表现为“源”的特征,平均值为0.000163±0.00009 mmol/(m2·h),变化趋势与p(CH4)一致.由于TBL模型法估算CH4通量只考虑水体的气体分压,并未考虑气泡扩散这一CH4主要的扩散方式,可能造成所得结果偏小.水-气界面CO2通量全为正值,表现为“源”的特征,平均值为2.24±0.50 mmol/(m2·h),变化趋势基本与p(CO2)一致(图 5b).
|
图 5 金沙江下游表层水体p(CO2)和p(CH4)(a)以及水-气界面CO2与CH4通量(b)沿程分布特征 Fig.5 Variation of streamwise of p(CO2) and p(CH4)(a), exchange flux of CO2 and CH4 between water and air(b) in the surface water of the downstream of Jinsha River |
采用Spearman相关性分析对金沙江下游表层水体p(CO2)、p(CH4)、CO2通量、CH4通量与各环境影响因子进行回归分析,结果表明,表层水体p(CO2)与DIC浓度、碱度均呈显著正相关,水体中DIC浓度越高,p(CO2)就越大,另外,金沙江下游水体浮游植物光合作用在吸收水中溶解性C、N、P等营养物质的同时,会降低表层水体碱度[29],由于金沙江下游浮游植物光合作用效果不明显,因此碱度越高,p(CO2)也越大.而p(CH4)与水温、Chl.a均呈显著正相关,水温越高,深水部CH4在水中的溶解度减小,CH4扩散至表层水体,p(CH4)增大,而Chl.a是浮游植物生物量的直接表征,水温与大量的浮游植物为产CH4菌的代谢提供了良好的生长环境,有利于CH4的产生. CH4通量与p(CH4)和风速均呈正相关,p(CH4)越大,CH4通量越高,同时风速可能造成表层水体的扰动,使CH4的扩散通量增大. CO2扩散通量与p(CO2)、DIC、碱度和风速均呈显著正相关,可见,CO2扩散通量与p(CO2)仍然受DIC、碱度影响,DIC、碱度越高,p(CO2)越大,同时CO2扩散通量也越大(表 2).
| 表 2 CO2、CH4分压、通量与各环境因子的相关性分析 Tab.2 Correlations between p(CO2), p(CH4), CO2 flux, CH4 flux and environment factors |
一般河流中的CH4主要源于现场产生、沉积物的释放、周围富CH4水的输入,考虑长江水体中颗粒有机碳在总悬浮颗粒物中含量较低,现场产生对水体CH4的贡献可能较低,研究表明[30],金沙江下游表层水体CH4浓度较低,除了CH4的现场产生很低外,金沙江两岸人类活动较少,且输入金沙江的支流中所含CH4浓度也较低,表层水体CH4平均浓度为86.37±8.76 nmol/L,满足秋季长江上游表层水体CH4平均浓度90.3±53.6 nmol/L范围[31],在世界河流中处于较低水平.而CH4扩散通量平均值为3.912±2.16 μmol/(m2·d),水-气界面交换通量较小,这可能与测量方法和所选用公式有关,需要进一步充实数据和完善方法.
| 表 3 世界部分河流表层水体CH4浓度和CH4通量以及体p(CO2)及CO2通量 Tab.3 The c(CH4) and CH4 flux, p(CO2) and CO2 flux in the surface water of the world rivers |
世界绝大多数河流中的CO2都呈过饱和状态,p(CO2)基本在2000~8000 μatm之间,一些地区支流水体p(CO2)甚至高达10000 μatm以上[35-36].近年来,国内也有一些关于水体p(CO2)的报道,祖桂胜[27]、张龙军等[28]对黄河、长江主干流的研究表明, 秋季黄河干流水体p(CO2)为790~1600 μatm,而长江干流水体全年p(CO2)为860~1600 μatm.本研究金沙江下游表层水体p(CO2)平均值为2724.84±477.18 μatm,而与世界其他河流相比,如Amazonian河[32]、Hudson河[31],金沙江下游p(CO2)在世界主要河流中属中等水平.而金沙江下游水-气界面CO2扩散通量平均值为2.24±0.50 μmol/(m2·h),与其他河流相比,如Amazonian河[32]、Hudson河[31]、黄河,属于中等水平,因此作为大型河流的金沙江,对其CO2通量的研究意义重大.
金沙江下游建成、在建四座水电站,向家坝、溪洛渡水电站已于2014年正式投产,白鹤滩水电站将于2020年投产,而乌东德水电站将于2021年投产.水电站的建成投产、水库的蓄水,可能会影响到金沙江流域的碳循环,故对金沙江下游展开温室气体的监测研究,初步了解该流域水电站建成后温室气体的排放情况,对进一步揭示该流域的碳循环变化具有重要意义.研究发现,位于溪洛渡水电站坝前的燕子岩、向家坝库区的林家坝以及向家坝水电站坝前的邵女坪点位p(CO2)与p(CH4)相对较高,表明向家坝与溪洛渡水电站建成后,库区水体中的CO2与CH4较高,但CO2与CH4的通量相对其他点位并没有明显的增大,根据现有条件推测,水电站建成后造成的温室效应作用并不明显.
3 结论1)夏季金沙江下游汛期表层水体p(CO2)平均值为724.84±477.18 μatm,在世界主要河流中属中等水平,p(CO2)值在已建成的向家坝与溪洛渡水电站坝前以及库区部位相对较高;表层水体p(CH4)平均值为59.96±6.74 μatm,且空间分布较为均匀,在世界河流中处于较低水平.
2)夏季金沙江下游水-气界面CH4通量为正值,表现为“源”的特征,平均值为0.000163±0.00009 mmol/(m2·h),水-气界面CO2通量全为正值,表现为“源”的特征,平均值为2.24±0.50 mmol/(m2·h),在世界河流中处于中等水平.通量的的变化趋势基本与p(CO2)、p(CH4)保持一致.
3)2015年8月,金沙江下游水-气界面CH4通量与p(CH4)、风速均呈正相关,而CO2通量与p(CO2)、DIC、碱度、风速均呈正相关,其他环境因素的影响不明显,有待进一步研究.
| [1] |
Ludwig W, Probst JL, Kempe S. Predicting the oceanic input of organic carbon by continental erosion. Global Biogeochemistry Cycle, 1996, 10(1): 23-41. DOI:10.1029/95GB02925 |
| [2] |
Guo Jinsong, Jiang Tao, Li Zhe et al. Analysis on partial pressure of CO2 and influencing factors during spring phytoplankton bloom in the backwater area of Xiaojiang River in Three Gorges Reservoir. Advances in Water Science, 2011, 22(6): 829-838. [郭劲松, 蒋滔, 李哲等. 三峡水库澎溪河春季水华期p(CO2)及影响因素分析. 水科学进展, 2011, 22(6): 829-838.] |
| [3] |
Zhang Chao, Gao Quanzhou, Tao Zhen et al. Chemical weathering and CO2 consumption in the Wuhua River basin, eastern Guangdong Province. J Lake Sci, 2013, 25(2): 250-258. [张超, 高全洲, 陶贞等. 粤东五华河流域的化学风化与CO2吸收. 湖泊科学, 2013, 25(2): 250-258. DOI:10.18307/2013.0211] |
| [4] |
Cole JJ, Prairie YT, Caraco NF et al. Plumbing the global carbon cycle: Integrating inland waters into the terrestrial carbon budget. Ecosystems, 2007, 10(1): 172-185. DOI:10.1007/s10021-006-9013-8 |
| [5] |
Li Zhe, Bai Lei, Guo Jinsong et al. Comparative study on water-air CO2, CH4 flux in two tributaries in the Three Gorges Reservoir, China. Environmental Sciences, 2013, 34(3): 1008-1016. [李哲, 白镭, 郭劲松等. 三峡水库两条支流水-气界面CO2、CH4通量比较初探. 环境科学, 2013, 34(3): 1008-1016.] |
| [6] |
Degens ET, Kempe S, Richey JE eds. Biogeochemistry of major world rivers. New York: John Wiley and Sons, 1991, 42. |
| [7] |
Zhao Yan, Zeng Yuan, Wu Bingfang et al. Review of methods from easering greenhouse gas flux from the air-water interface of reservoirs. Advances in Water Science, 2011, 22(1): 135-146. [赵炎, 曾源, 吴炳方等. 水库水-气界面温室气体通量监测方法综述. 水科学进展, 2011, 22(1): 135-146.] |
| [8] |
Urabe J, Iwata T, Yagami Y et al. Within-lake and watershed determinants of carbon dioxide in surfacewater: A comparative analysis of a variety of lakes in the Japanese Islands. Limnology and Oceanography, 2011, 56(1): 49-60. DOI:10.4319/lo.2011.56.1.0049 |
| [9] |
Jonsson A, Aberg J, Jonsson M. Variations in p(CO2) during summer in the surface water of an unproductive lake in northern Sweden. Tellus B, 2007, 59: 797-803. DOI:10.1111/j.1600-0889.2007.00307.x |
| [10] |
Huotari J, Ojala A, Peltomaa E et al. Temporal variations in surface water CO2 concentration in a boreal humic lake based on high-frequency measurements. Borael Environment Research, 2009, 14: 48-60. |
| [11] |
Pumpanen J, Kolari P, Minkkinen K et al. Comparison of different chamber techniques for measuring soil CO2ef-flux. Agricultural and Forest Meteorology, 2004, 123: 159-176. DOI:10.1016/j.agrformet.2003.12.001 |
| [12] |
Tremblay A, Varfalvy L, Roehm C et al. Greenhouse gas emissions: Fluxes and processes, hydroelectric reservoirs and natural environments. New York: Springer, 2005, 725-732. |
| [13] |
Kolb B, Ettre LS eds. Static headspace-gas chromatography, theory and practice(Second Edition). New York: John Wiley and Sons, 2006, 349. |
| [14] |
Goldenfum J ed. GHG measurement guidelines for freshwater reservoirs. The UK: The International Hydropower Association, 2010, 76. |
| [15] |
Weiss RF. Carbon dioxide in water and seawater: The solubility of a non-ideal gas. Marine Chemistry, 1974, 2: 203-215. DOI:10.1016/0304-4203(74)90015-2 |
| [16] |
Waest RC, Astle MJ eds. CRC Handbook of Chemistry and physics. New York: CRC, 2007, 88. |
| [17] |
Kampbell DH, Vandegrift SA. Analysis of dissolved methane, ethane, and ethylene in ground water by a standard gas chromatographic technique. Journal of Chromatographic Science, 1998, 36: 253-256. DOI:10.1093/chromsci/36.5.253 |
| [18] |
Billen T, Libner P, Fischer R et al. Investigating the transfer processes across the free aqueous viscous boundary layer by the controlled flux method. Tellus Series B-Chemical and Physical Meteorology, 1989, 41: 177-195. DOI:10.3402/tellusb.v41i2.15068 |
| [19] |
Cole JJ, Caraco NF. Atmospheric exchange of carbon dioxide in a low-wind oligotrophic lake measured by addition of SF6. Limnology and Oceanography, 1998, 43: 647-656. DOI:10.4319/lo.1998.43.4.0647 |
| [20] |
Macintyre S, Wanninkhof R, Chanton JP. Trace gas exchange across the air-water interface in freshwater and coastal marine environments. New York: P. A. Matson and Harriss Blackwell Science, 2006, 52-97. |
| [21] |
Roehm CL, Prairie YT, Giorgio PA. The p(CO2) dynamics in lakes in the boreal region of northern Québec, Canada. Global Biogeochemical Cycles, 2009, 23: 3013. |
| [22] |
Wanninkhof BR. Relationship between gas exchange and wind speed over the ocean. Journal of Geophysical Research, 1992, 97(5): 7373-7381. |
| [23] |
Crusius J, Wanninkhof R. Gastransfer velocities measured at low wind speed over a lake. Limnology and Oceanography, 2003, 48(3): 1010-1017. DOI:10.4319/lo.2003.48.3.1010 |
| [24] |
Morel F ed. Principles of aquatic chemistry. New York: John Wliely and Sons, 1982, 446. |
| [25] |
Anderson CB. Understanding carbonate equilibria by measuring alkalinity in experimental and natural systems. Journal of Geoscience Education, 2002, 50(4): 389-403. DOI:10.5408/1089-9995-50.4.389 |
| [26] |
Bates NR, Mathis JT, Jeffries MA et al. Air-sea CO2 fluxes on the Bering Sea shelf. Biogeosciences Discussions, 2011, 8(5): 1237-1253. DOI:10.5194/bg-8-1237-2011 |
| [27] |
Gui Zusheng. Study on the distribution and influence mechanism of pCO2 in the Yangtze River mainstream and estuary[Dissertation]. Qingdao: Ocean University of China, 2007. [桂祖胜. 长江干流及其河口水体pCO2的分布与影响因素的初步研究[学位论文]. 青岛: 中国海洋大学, 2007. ]
|
| [28] |
Zhang Longjun, Xu Xuemei, Wen Zhichao. Control factors of pCO2 and CO2 degassing fluxes from the Yellow River in autumn. Advances in Water Science, 2009, 20: 227-235. [张龙军, 徐雪梅, 温志超. 秋季黄河pCO2控制因素及水-气界面通量. 水科学进展, 2009, 20: 227-235. DOI:10.3321/j.issn:1001-6791.2009.02.012] |
| [29] |
Davies JM, Hesslein RH, Kelly CA et al. pCO2 method for measuring photosynthesis and respiration in freshwater lakes. Journal of Plankton Research, 2003, 25(4): 385-395. DOI:10.1093/plankt/25.4.385 |
| [30] |
Zhang G, Zhang J, Liu S et al. Methane in the Changjiang(Yangtze River)Estuary and its adjacent marine area: Riverine input, sediment release and atmospheric fluxes. Biogeochemistry, 2008, 91(1): 71-84. DOI:10.1007/s10533-008-9259-7 |
| [31] |
Zhao Yuchuan. Distributions and fluxes of methane and nitrous oxide in the Changjiang(Yangtze River) and its estuary abstract[Dissertation]. Qingdao: Ocean University of China, 2011. [赵玉川. 长江流域及长江口溶解性甲烷和氧化亚氮的分布与释放通量[学位论文]. 青岛: 中国海洋大学, 2011. ]
|
| [32] |
Grunwald M, Dellwing O, Beck M et al. Methane in the southern North Sea: Sources, spatial distribution and budgets. Estuarine, Coastal and Shelf Science, 2009, 81(4): 445-456. DOI:10.1016/j.ecss.2008.11.021 |
| [33] |
De Angelis MA, Lilley MD. Methane in surface waters of Oregon estuaries and rivers. Limnology and Oceanography, 1987, 32(3): 716-722. DOI:10.4319/lo.1987.32.3.0716 |
| [34] |
Zhao Jing, Zhang Guiling, Wu Ying et al. Distribution and emission of methane from the Changjiang. Environmental Science, 2011, 32(1): 18-25. [赵静, 张桂玲, 吴莹等. 长江中溶存甲烷的分布与释放. 环境科学, 2011, 32(1): 18-25.] |
| [35] |
Cole JJ, Caraco NF. Carbon in catchments: Connecting terrestrial carbon losses with aquatic metabolism. Marine Freshwater Research, 2001, 52: 101-110. DOI:10.1071/MF00084 |
| [36] |
Richey JE, Melack JM, Aufdenkampe AK et al. Outgassing from Amazonian rivers and wetlands as a large tropical source of atmospheric CO2. Nature, 2002, 416: 617-620. DOI:10.1038/416617a |
 2017, Vol. 29
2017, Vol. 29 

