(2: 无锡市太湖湖泊治理有限责任公司, 无锡 214023)
(2: The Limited Liability Company of Wu Xi-Taihu Lake Controlling, Wuxi 214023, P. R. China)
溶解性有机质(DOM)是一种结构和组成较为复杂的有机混合物[1],主要源于沉积物与水体中动物与植物及微生物的降解,是湖泊生态系统的重要组成部分之一[2]. DOM可以通过各种物理化学过程,与水体中的颗粒物以及污染物如矿物颗粒、金属离子、有机污染物等相互作用,进而影响湖泊中水体与沉积物中污染物的来源、分布、生物毒性等[3-5],在湖泊各种物理、化学和生物反应中,特别是蓝藻水华暴发过程中扮演了非常重要的角色,因此受到越来越多研究者的关注.
有色溶解性有机质(chromophoric dissolved organic matter,CDOM)是水体及沉积物DOM储库中的主要组成部分,同时也是DOM中活性较高的成分之一[6].三维荧光光谱是种简便灵敏的光谱指纹技术,可以快捷揭示CDOM中所含荧光团的组成信息[7],有助于从定性和定量的角度揭示悬浮物中CDOM的性质、浓度变化特征及其控制因素和机制,作为新兴的研究方法被应用于湖泊水环境中.自从Coble等[8]利用三维荧光光谱技术将CDOM荧光峰分为3类(类腐殖酸峰、类富里酸峰和类蛋白质峰)、4个区域以后,三维荧光技术结合各种荧光指数、平行因子分析方法被广泛应用于海洋[9-11]、湖泊[12-13]、河流[14-15]等水体CDOM的组成结构及污染物迁移转化规律研究等方面.
由浮游动植物、微生物和有机碎屑等组成的有机物和由无机碎屑、黏土等组成的无机物共同构成了水体中的悬浮物.悬浮物浓度的增加是引起湖水透明度降低和光学衰减系数增大的主要原因,而湖底底泥受风生流扰动引起再悬浮会强烈影响营养盐在沉积物水界面间的再分配[16].目前对于DOM荧光光谱的研究多集中在水体方面[17-18],而悬浮物中水溶性有机质(WSOM)的荧光光谱鲜有研究.五里湖作为太湖北部的城市景观湖泊,在外源基本得到控制的情况下,内源污染依然严重,而降低悬浮物浓度、提高透明度是进一步解决五里湖水环境问题的关键之一[19].近年来,五里湖经过底泥疏浚、生态重建、环湖截污等治理工程,水质已经处于地表水质标准Ⅳ类水平,部分区域已经满足Ⅲ类水质要求,但悬浮物浓度没有显著降低[20].本研究采用EEMs-PARAFAC方法对五里湖水体悬浮物中WSOM的组成类型、分布特征、来源以及其生物有效性进行分析,为揭示悬浮物中WSOM的环境行为特征以及在水体、沉积物之间的迁移转化提供数据支撑,并为五里湖水生态环境保护提供理论基础和科学依据,对进一步提高五里湖水体水质有重要意义.
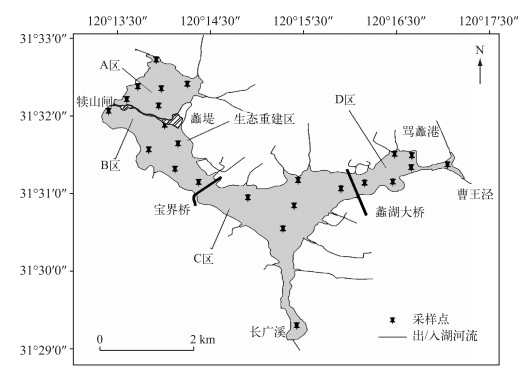
1 采样与数据处理 1.1 研究区概况五里湖(31.48°~31.55°N,120.22°~120.29°E)又称蠡湖,是太湖北部的一个湖湾,东西长约6 km,南北宽0.3~1.8 km,面积约8.6 km2,是一个既相对独立又与太湖相通的水体[21].为方便讨论,以蠡堤、宝界桥和五里湖大桥为边界,将五里湖划分为4个区域(图 1),其中五里湖A区进行过湖体清淤、水生植被重建工程;B区曾经展开过底泥环保疏浚治理工程和水生植被整治工程;C区沿岸实施了整治工程,例如长广溪湿地的建设;D区周围居民楼比较集中,富营养化问题严重[22].
|
图 1 五里湖采样点分布 Fig.1 Distribution of sampling sites in Lake Wuli |
于2014年10月1日在无锡市五里湖4个湖区及出入河口采集了24个悬浮物样品,每个湖区采集6个样品,采样布点见图 1.每个采样点采用5 L有机玻璃采水器,采集距水面0.5 m的水样40 L于干净塑料桶内,立即运回野外实验站,用Whatman GF/F玻璃纤维膜(0.45 μm, 450℃, 3 h)过滤获得悬浮物样品,而后在-50℃真空(1~10 kPa)条件下冷冻干燥,研磨过100目筛,保存备用.
每个点位分别称取(2±0.0005 g)干燥悬浮物样品于100 ml离心管中,加入50 ml超纯水,振荡2 h(220转/min,25℃)后离心(5000转/min, 15 min),取上清液,过滤膜(Whatman GF/F,450℃,5 h)后,扫描三维荧光光谱并测定水提取态总氮(WTN)、水提取态有机氮(WSON)等指标,其中水提取态无机氮(WSIN)为水提取态铵态氮与水提取态硝态氮之和,WSON为WTN与WSIN之差.具体分析测试方法见《沉积物质量调查评估手册》[23].
1.3 悬浮物水溶解性有机碳(WSOC)的测定采用TOC-VCPH型总有机碳分析仪(厂家)分析测定悬浮物提取液中WSOC含量.每个样品均重复测定3次,保证其测定结果变异系数 < 2 %.
1.4 紫外-可见吸收光谱扫描和处理紫外-可见吸收光谱由紫外-可见分光光度计(D5000,哈希)测定,扫描波长范围为200~700 nm,步长为1 nm,以超纯水为参比,中速扫描254 nm处吸光系数(a254)按照公式(1)进行计算,为了消除滤液中可能残留细小颗粒而引起的光散射,通过公式(2)校正其散射效应[24].为了尽量降低硝态氮和亚硝态氮在200~250 nm处吸收光子而引发干扰,对扫描的样品进行稀释,直至其在波长254 nm处的吸光度小于0.1.
| $ {a_{254}}\prime = 2.303{\rm{ }}{A_{254}}/L $ | (1) |
| $ {a_{254}} = {a_{254}}\prime-254{\rm{ }}{a_{700}}\prime /700 $ | (2) |
式中,a254为经过校正的波长254处的吸收系数(m-1);A254为波长254 nm处的吸光度;L为光程路径(m);a254′为未经过校正的波长λ处的吸收系数(m-1);a700′为波长700 nm处的吸收系数(m-1).
1.5 荧光光谱扫描和处理采用(Hitachi F-7000)进行WSOM荧光光谱测定,扫描速度为2400 nm/min,激发光源为150 W氛弧灯,PMT电压为400 V,信噪比>110,响应时间为自动,扫描光谱波长范围为Ex:200~450 nm,Em:250~600 nm,狭缝跨度均为10 nm;以Milli-Q超纯水作为空白样,所有样品三维荧光光谱扣除空白样品的光谱信号,然后在Matlab12.0软件中进行平行因子模型分析,并通过裂半分析对分离出的组分进行验证,最后确定最优的WSOM组分数目[25].
1.6 荧光光谱校正为保证荧光光谱特性的可比性,所得到的光谱均为经过扣除空白后的矫正结果,以减少仪器条件和拉曼散射对荧光光谱的影响.每隔5个样品测定超纯水在350 nm激发波长处拉曼峰(380~420 nm)的面积,用于检测仪器的稳定性,得到相对标准偏差为0.53 %.同时将荧光光谱单位转换为拉曼单位(R.U.)[26].通过扣除λEm < λEx +20 nm的区域消除一级瑞利散射对EEMs的影响,通过扣除λEm >2λEx-20 nm的区域扣除二级瑞利散射对EEMs的影响,扣除部分用零替换,其中λEm为发射波长,λEx为激发波长.
为了校正由于内过滤效应或自吸收引起的荧光淬灭, 需要利用公式(3)对扣除空白荧光之后的荧光光谱进行校正[27].
| $ {F_{{\rm{corr}}}} = {F_{{\rm{obs}}}} \times {10^{[({\rm{O}}{{\rm{D}}_{{\rm{Ex}}}}{\rm{ + O}}{{\rm{D}}_{{\rm{Em}}}})/2]}} $ | (3) |
式中,Fcorr和Fobs分别是校正后和实测的荧光光谱(已经扣除空白荧光);ODEx和ODEm分别为激发和发射波长下的吸光度.
1.7 数据处理主要通过SPSS 19.0、ArcMap 10.2、Matlab 12.0、OriginPro 9.0、Surfer 10.0、Excel 2010等软件进行绘图及数据分析.采样点布点图利用ArcMap 10.2绘制;三维荧光光谱和平行因子模型模拟均在Matlab 12.0中进行分析处理.
2 结果与分析 2.1 悬浮物WSOC和a254的空间分布特征悬浮物溶解性有机碳(WSOC)可以反映WSOM的总体分布水平.湖区各采样点WSOC含量的变化范围为288.0~1371.4 mg/kg,平均值为714.87±69.24 mg/kg.不同采样点WSOC含量差异明显,各湖区WSOC含量平均值的高低顺序为A区 < B区 < C区 < D区,其中D区悬浮物WSOC含量较高,尤其是五里湖大桥东侧和金城湾附近WSOC平均值为1329.00 mg/kg,是湖区均值的1.86倍(图 2a).可能与作为溶解性有机质重要来源的藻源性有机悬浮物在开展了底泥疏浚、水生植物重建等生态修复工程的A区和B区含量较低有关[20].

|
图 2 悬浮物中WSOC含量(a)和a254(b)的空间变化 Fig.2 Spatial variation of WSOC content (a) and a254 (b) in suspended solids |
悬浮物水提取液中a254是反映悬浮物中WSOM的又一关键指标[28].湖区各悬浮物采样点a254变化范围在22.73~107.71 m-1之间,均值为52.11 m-1,其均值空间变化趋势与WSOC相似(图 2b),两者呈极显著正相关(R2=0.72,n=24,P < 0.01).
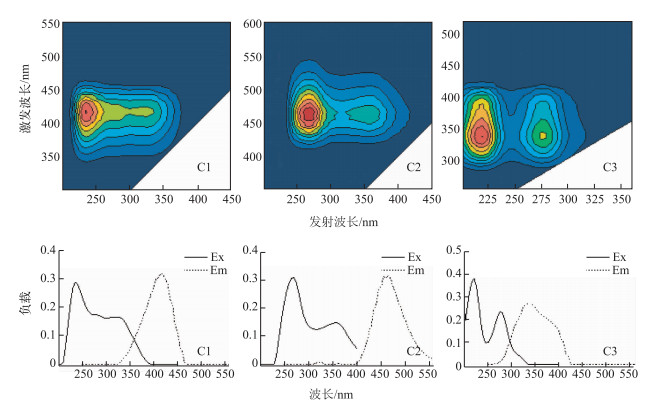
2.2 悬浮物WSOM荧光组分鉴别利用PARAFAC模型对五里湖悬浮物中WSOM的三维荧光光谱矩阵数据进行分析,悬浮物WSOM主要解析出3个荧光组分.通过裂半分析,残差分析检验,结果证明该PARAFAC模型有效,悬浮物中WSOM各荧光组分的荧光光谱及组分最大激发、发射波长分布如图 3.
|
图 3 悬浮物中WSOM的荧光组分(C1、C2和C3) Fig.3 Fluorescence component(C1, C2 and C3)of WSOM in suspended solids |
悬浮物WSOM共解析出2个类腐殖质组分和1个类蛋白组分.组分1(C1)在240和320 nm处存在2个明显激发波长,最大发射波长在420 nm处,反映的是自生源腐殖质物质,与富里酸物质波峰相近,可能主要来源于藻类微生物的降解[29-30];组分2(C2)在260和360 nm处存在2个明显的激发波长,最大发射波长在460 nm处,反映的是陆源腐殖质物质,与腐殖质中胡敏酸物质波峰相近,主要来源于高等植物腐解[31];组分3(C3)在225和275 nm处存在明显的激发波长,最大发生波长在335 nm,反映的是类蛋白物质的类色氨酸荧光峰,通常来源于水中微生物和浮游植物等残体分解[32].
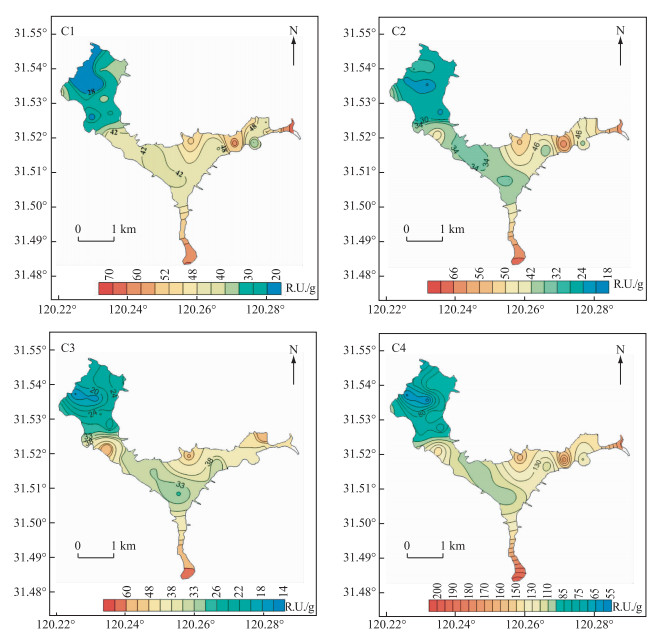
2.3 悬浮物WSOM荧光组分的空间分布特征五里湖各采样点悬浮物中表示自生源腐殖质的C1荧光强度在20.33~70.41 R.U./g之间,平均值为41.04 R.U./g;表示陆源腐殖质的C2荧光强度在19.28~68.79 R.U./g之间,平均值为39.30 R.U./g;表示类色氨酸的C3荧光强度在15.70~64.61 R.U./g之间,平均值为35.09 R.U./g.总荧光强度(Ct)在57.56~200.01 R.U./g之间,平均为115.42 R.U./g(图 4).
|
图 4 悬浮物WSOM中各组分荧光强度的空间分布特征 Fig.4 Spatial distribution characteristics of fluorescence intensity for WSOM components in the suspended solids |
总体上看,C1、C2和C3组分的荧光强度均由西向东逐渐增强,呈现东五里湖高于西五里湖,沿岸区高于湖心区的趋势.同时,C1、C2、C3组分的空间分布趋势基本一致,说明三者的来源可能相同.从荧光强度值来看,低值主要分布于A区,可能是由于沉水植物的大量恢复对水体起着抑制底泥上浮、净化水质的作用,再加之环保疏浚工程实施后,清除了表层淤泥;高值均集中在C区长广溪以及D区金城湾附近,其中D区周围居民楼密集,内源中WSOM含量较高.从各荧光组分占总组分的相对比例来看,C1、C2和C3组分的相对比例分别为35.55 %、34.05 %和30.40 %.其中,A区C1、C2和C3组分的相对比例分别为35.86 %、36.28 %和27.85 %,D区中C1、C2和C3组分的相对比例分别为35.83 %、32.87 %和31.30 %.可以看出,水质较好的A区高等植物腐解的C2组分所占比例较大,与A区不同的是,D区则是浮游植物、藻类微生物降解的C1组分所占比例大.说明多来源于自生源.
3 讨论 3.1 悬浮物WSOM的荧光强度与WSOC的关系CDOM组成对其在环境中的作用具有十分重要的影响,在研究CDOM循环过程中需要选择合适的参数和手段进行观察,以便有效反映CDOM浓度、来源、光吸收性质和生物可利用性等方面的信息. CDOM中具有光学效应的组分作为标志物用以研究DOM的迁移转化过程[33].荧光光谱和紫外可见吸收光谱的出现为传统鉴定方法提供了新的思路,为水体生态系统CDOM的鉴别提供了新的方法.本次研究利用三维荧光光谱-平行因子分析法对悬浮物中WSOM组分进行了解析,分别得到3个荧光组分的荧光强度,将其分别与WSOC和a254浓度进行相关分析(图 5).

|
图 5 悬浮物中WSOC、a254与总荧光强度的相关性分析 Fig.5 Correlation analysis between WSOC, a254 and the total fluorescence intensity in suspended solids |
WSOM总荧光强度同WSOC含量和a254都存在明显的线性正相关(图 5),与文献关于水体中DOC的浓度与荧光强度显著相关相似[23],说明紫外可见吸收光谱和荧光光谱均可以用来反映悬浮物中有机物含量,进一步表明五里湖悬浮物中可以利用CDOM的荧光强度来定量表征WSOM的含量.但也有相关研究表明,由于CDOM中存在一定量不吸收光的天然有机物,进而导致荧光强度和DOC之间并不总是相关[34-36].
3.2 悬浮物中WSOM的来源辨识CDOM的来源可以按陆源和生物来源进行区分,也可以按外源和内源进行区分.陆源由细菌和真菌降解流域土壤中高等动植物残体形成,多表现为类腐殖质峰占绝对优势[37];生物来源是由水体中浮游生物、水生细菌、藻类等生物活动产生,多表现为类蛋白峰占绝对优势[38].五里湖是太湖伸入陆地而形成的城市湖泊,是一个典型的小型浅水湖泊,先前的研究表明[39],五里湖与周边河流基本上以闸控的方式隔绝,外源河流输入的颗粒物可以忽略不计,因此水体中悬浮物以风浪扰动引起的沉积物再悬浮物、浮游生物、水生植物腐烂后的残体为主.
荧光光谱特性是理想的表征天然水体中CDOM以及评估其来源的重要参数.荧光指数(FI)是在370 nm激发波长处,450与500 nm发射波长下的荧光强度比值[40],可用来表征溶解有机质中腐殖质的来源,大于1.9说明主要来源于微生物代谢等过程,小于1.4说明陆源占主要贡献.本次研究中,采用I(370:450)/I(370:500)作为荧光指数,悬浮物中FI范围为1.48~2.34,平均值为1.83,说明各采样点生物来源的贡献大于陆源.
生物源指数(BIX)是310 nm激发波长下380 nm发射波长处荧光强度与420~435 nm区间最大荧光强度的比值[41],反映了新产生的WSOM在整体WSOM中所占的比例,生物源指数越高,说明新近自生源组分的比例越高. Huguet等[42]指出,BIX在0.6~0.7之间时,具有较少的自生成分;BIX在0.7~0.8时具有中度新近自生源特征;在0.8~1.0之间时, 具有较强自生源特征;大于1.0时为细菌活动产生.本次研究中,悬浮物WSOM的BIX指数在0.65~0.87之间,平均值为0.76,说明各采样点整体具有较强的中度新近自生源特征.
综上所述,悬浮物中WSOM的FI和BIX来源在表征上都具有良好的指示性,都显现出五里湖悬浮物中WSOM主要来源于自生微生物、藻类的自生源,与五里湖与周边河流基本上以闸控的方式隔绝相呼应.但同时也可以看出,五里湖悬浮物中CDOM的BIX指数均值为0.76,而五里湖水体的BIX为0.96[24],反映了五里湖悬浮物可能经过长时间的微生物或者光漂白作用的降解.
3.3 悬浮物中WSOM荧光组分与氮形态的相关性分析WSOM与N、P元素的迁移转化密切相关,可通过微生物降解和光降解过程释放出氮、磷等浮游植物和细菌可直接吸收利用的营养元素.五里湖悬浮物中水提取态总氮(WTN)在64.48~309.83 mg/kg之间,均值为168.69 mg/kg,其中以WSON占优势,占WTN的62.34 %. WSIN为水提取态铵态氮与水提取态硝态氮之和,占WTN的比例较小,其中水提取态铵态氮含量在10.86~101.43 mg/kg之间,均值为45.82 mg/kg,占WTN含量的27.16 %,水提取态硝态氮含量在6.61~35.93 mg/kg之间,均值为17.71 mg/kg,占WTN含量的比重较小,为10.50 %.通过悬浮物WSOM荧光组分与生物可利用性较强的水提取态氮形态做回归分析发现,悬浮物WSOM的3个荧光组分的荧光强度与WSIN和WSON都呈正相关(图 6),说明五里湖悬浮物WSOM与氮元素的迁移转化密切相关.悬浮物中的WTN以WSON为主,与C1、C2和C3都呈极显著正相关,且与C2的相关系数比C1和C3大,说明悬浮物中WSON受WSOM各组分的共同影响,尤其受到类腐殖质组分的影响较大.同时可以看出,悬浮物中WSOM各组分荧光强度与SON的相关性系数都大于WSIN,说明悬浮物中WSOM被微生物矿化分解或者光降解后产生的无机铵态氮可能释放到了水体中.

|
图 6 悬浮物WSOM荧光组分(C1、C2和C3)与WSIN和WSON的相关性 Fig.6 Correlation between WSIN, WSON and WSOM fluorescent components (C1, C2 and C3) in suspended solids |
1) 五里湖悬浮物中WSOM主要由3个荧光组分组成,分别为类腐殖质荧光组分C1、陆源腐殖质荧光组分C2和类色氨酸荧光组分C3,荧光强度均值分别为41.04、39.30和35.09 R.U./g.
2) 悬浮物中WSOM的FI和BIX分别在1.48~2.34和0.65~0.87之间,平均值分别为1.83和0.76.表明五里湖悬浮物中WSOM主要来源于自生微生物、藻类的自生源,并且以新近自生源为主.
3) 悬浮物中WSOM的荧光组分与WSIN和WSON都呈正相关,相关系数分别为0.88和0.57,且有机氮与WSOM荧光组分的线性回归更显著于无机氮,说明悬浮物有机氮可能来源于WSOM的降解.
| [1] |
Kalbitz K, Solinger S, Park JH et al. Controls on the dynamics of dissolved organic matter in soils:A review. Soil Science, 2000, 165(4): 277-304. DOI:10.1097/00010694-200004000-00001 |
| [2] |
Gao J, Jiang T, Liu LL et al. Ultraviolet-visible (UV-Vis) and fluorescence spectral characteristics of dissolved organic matter(DOM) in soils of water-level fluctuation zones of the three gorges reservoir region. Environmental Science, 2015, 36(1): 151-162. [高洁, 江韬, 李璐璐等. 三峡库区消落带土壤中溶解性有机质(DOM)吸收及荧光光谱特征. 环境科学, 2015, 36(1): 151-162. DOI:10.13227/2015.01020] |
| [3] |
Wu FC, Xing BS eds. Natural organic matter and its significance in the environment. Beijing: Geological Publishing House, 2010, 61-68. [吴丰昌, 邢宝山. 天然有机质及其在环境中的作用机理. 北京: 地质出版社, 2010, 61-68.]
|
| [4] |
Zhou YQ, Zhang YL, Shi K et al. Lake Taihu, a large, shallow and eutrophic aquatic ecosystem in China serves as a sink for chromophoric dissolved organic matter. Journal of Great Lakes Research, 2015, 41(2): 597-606. DOI:10.1016/j.jglr.2015.03.027 |
| [5] |
Wei QS, Luo ZX, Chen Q et al. Florescence responses of dissolved organic matter (DOM) fractions to typical urban source pollution in Natural water. Research of Environmental Science, 2010, 23(10): 1229-1235. [魏群山, 罗专溪, 陈强等. 天然水体溶解性有机物(DOM)分级组分对典型城市源污染的荧光响应. 环境科学研究, 2010, 23(10): 1229-1235.] |
| [6] |
Yao X, Zhang YL, Zhu GW et al. Resolving the variability of CDOM fluorescence to differentiate the sources and fate of DOM in Lake Taihu and its tributaries. Chemosphere, 2011, 82(2): 145-155. DOI:10.1016/j.chemosphere.2010.10.049 |
| [7] |
Henderson RK, Baker A, Murphy K et al. Fluorescence as a potential monitoring tool for recycled water systems:A review. Water Research, 2009, 43(4): 863-881. DOI:10.1016/j.watres.2008.11.027 |
| [8] |
Coble PG, Schultz CA, Mopper K. Fluorescence contouring analysis of DOC intercalibration experiment samples:A comparison of techniques. Marine Chemistry, 1993, 41(1/2/3): 173-178. |
| [9] |
Stedmon CA, Markage S, Tranvik L et al. Photoehemical produetion of ammonium and transformation of dissolved organic matter in the Baltie Sea. Mar Chem, 2007, 104(3): 227-240. |
| [10] |
Du CF, Shang SL, Dong Q et al. Characteristics of chromophoric dissolved organic matter in the nearshore waters of the western Taiwan Strait. Estuarine, Coastal and Shelf Science, 2010, 88(3): 350-356. DOI:10.1016/j.ecss.2010.04.014 |
| [11] |
Hancke K, Hovand EK, Volent Z et al. Optical properties of CDOM across the Polar Front in the Barents Sea Origin, distribution and significance. Journal of Marine Systems, 2014, 130(6): 219-227. |
| [12] |
Xu HC, Jiang HL. UV-induced photochemical heterogeneity of dissolved and attached organic matter associated with cyanobacteria blooms in a eutrophic freshwater lake. Water Research, 2013, 47(17): 6506-6515. DOI:10.1016/j.watres.2013.08.021 |
| [13] |
Wang Y, Zhang D, Shen Z et al. Characterization and spacial distribution variability of chromophoric dissolved organic matter (CDOM) in the Yangtze Estuary. Chemosphere, 2014, 95: 353-362. DOI:10.1016/j.chemosphere.2013.09.044 |
| [14] |
Han YC, Guo WD. Factors influencing analysis of chromophoric dissolved organic matter in estuarine waters by excitation emission matrix spectroscopy (EEMS). Acta Scieniae Circumstantiae, 2008, 28(8): 1646-1653. [韩宇超, 郭卫东. 河口区有色溶解有机物(CDOM)三维荧光光谱的影响因素. 环境科学学报, 2008, 28(8): 1646-1653.] |
| [15] |
Liu ML, Zhang YL, Qin BQ. Characterization of absorption and three-dimensional excitation-emission matrix spectra of chromophoric dissolved organic matter at the river inflow and the open area in Lake Taihu. J Lake Sci, 2009, 21(2): 234-241. [刘明亮, 张运林, 秦伯强. 太湖入湖河口和开敞区CDOM吸收和三维荧光特征. 湖泊科学, 2009, 21(2): 234-241. DOI:10.18307/2009.0212] |
| [16] |
Almroth RE, Eilola K, Hordoir R. Transport of fresh and resuspended particulate organic material in the Baltic Sea-A model study. Journal of Marine Systems, 2011, 87(1): 1-12. DOI:10.1016/j.jmarsys.2011.02.005 |
| [17] |
Wang ZG, Liu WQ, Li HB et al. Analysis of CDOM spatial distributions variations in Chaohu Lake and its sources by three dimensional fluorescence excitation-emission matrix. Acta Scieniae Circumstantiae, 2006, 26(2): 275-279. [王志刚, 刘文清, 李宏斌. 三维荧光光谱法分析巢湖CDOM的空间分布及其来源. 环境科学学报, 2006, 26(2): 275-279.] |
| [18] |
Zhang YL, Yin Y, Feng LQ et al. Characterizing chromophoric dissolved organic matter in Lake Tianmuhu and its catchment basin using excitation-emission matrix fluorescence and parallel factor analysis. Water Research, 2011, 45(16): 5110-5122. DOI:10.1016/j.watres.2011.07.014 |
| [19] |
Wang SH, Jiang X, Wang WW et al. Dynamic spatial and temporal changes in water transparency and their influencing factors in Lihu Lake. Research of Environmental Science, 2014, 27(7): 688-695. [王书航, 姜霞, 王雯雯等. 蠡湖水体透明度的时空变化及其影响因素. 环境科学研究, 2014, 27(7): 688-695.] |
| [20] |
Wang SH, Jiang X, Wang WW et al. Spatial-temporal dynamic changes of the water suspended matter and its influencing factors in Lihu Lake. China Environmental Science, 2014, 34(6): 1548-1555. [王书航, 姜霞, 王雯雯等. 五里湖水体悬浮物的时空变化及其影响因素. 中国环境科学, 2014, 34(6): 1548-1555.] |
| [21] |
Chen KN, Bao XM, Shi LX et al. Ecological restoration engineering in Lake Wuli, Lake Taihu:a large enclosure experiment. Journal of Lake Sciences, 2016, 18(2): 139-149. [陈开宁, 包先明, 石龙新等. 太湖五里湖生态重建示范工程——大型围隔试验. 湖泊科学, 2016, 18(2): 139-149.] |
| [22] |
Jiang X, Wang SH, Yang XF et al. Change in water quality and ecosystem of Lihu Lake before and after comprehensive water environmental improvement measures. Research of Environmental Science, 2014, 27(6): 595-601. [姜霞, 王书航, 杨小飞等. 五里湖水环境综合整治工程实施前后水质及水生态差异. 环境科学研究, 2014, 27(6): 595-601.] |
| [23] |
Jiang X, Wang SH. The handbook of sediment quality assessment. Beijing: Science Press, 2012, 30-37. [姜霞, 王书航. 沉积物质量调查评估手册. 北京: 科学出版社, 2012, 30-37.]
|
| [24] |
Wang SH, Wang WW, Jiang X et al. Distribution of chromophoric dissolved organic matter in Lihu Lake using excitation-emission matrix fluorescence and parallel factor analysis. China Environmental Science, 2016, 36(2): 517-524. [王书航, 王雯雯, 姜霞等. 基于三维荧光光谱-平行因子分析技术的五里湖CDOM分布特征. 中国环境科学, 2016, 36(2): 517-524.] |
| [25] |
Stedmon CA, Bro R. Characterizing dissolved organic matter fluorescence with parallel factor analysis:A tutorial. Limnology and Oceanography:Methods, 2008, 6(11): 572-579. DOI:10.4319/lom.2008.6.572 |
| [26] |
Lawaetz AJ, Stedmon CA. Fluorescence intensity calibration using the Raman scatter peak of water. Applied Spectroscopy, 2009, 63(8): 936-940. DOI:10.1366/000370209788964548 |
| [27] |
Yan LH, Chen XJ, Su RG et al. Resolving characteristic of CDOM by excitation-emission matrix spectroscopy combined with parallel factor analysis in the seawater of outer Yangtze estuary in autumn in 2010. Environmental Science, 2013, 34(1): 51-60. [闫丽红, 陈学君, 苏荣国等. 2010年秋季长江口外海域CDOM的三维荧光光谱-平行因子分析. 环境科学, 2013, 34(1): 51-60.] |
| [28] |
Albrecht R, Le PJ, Terrom G et al. Comparison between UV spectroscopy and nirs to assess humification process during sewage sludge and green wastes co-composting. Bioresource Technology, 2011, 102(6): 4495-4500. DOI:10.1016/j.biortech.2010.12.053 |
| [29] |
Mesfioui R, Abdulla HA, Hatcher PG. Photochemical alterations of natural and anthropogenic dissolved organic nitrogen in the York River. Environmental Science and Technology, 2015, 49(1): 159-167. DOI:10.1021/es504095c |
| [30] |
Zhang YL, Zhang EL, Yin Y et al. Characteristic and sources of chromophoric dissolved organic matter in lakes of the Yungui Plateau, China, differencing in trophic state and altitude. Limnology and Oceanography, 2011, 55(6): 2645-2659. |
| [31] |
Zsolnay A, Baigar E, Jimenez M et al. Differentiating with fluorescence spectroscopy the sources of dissolved organic matter in soils subjected to drying. Chemosphere, 1999, 38(1): 45-50. DOI:10.1016/S0045-6535(98)00166-0 |
| [32] |
Zhang YL, Mark AV, Liu ML et al. The contribution of phytoplankton degradation to chromophoric dissolved organic matter(CDOM) in eutrophic shallow lakes:Field and experimental evidence. Water Research, 2009, 43(18): 4685-4697. DOI:10.1016/j.watres.2009.07.024 |
| [33] |
Zeri C, Besikepe S, Giannakouroua et al. Chemical properties and fluorescence of DOM in relation to biodegradation in the interconnected Marmara-North Aegean Seas during August 2008. Journal of Marine Systems, 2014, 135: 124-136. DOI:10.1016/j.jmarsys.2013.11.019 |
| [34] |
Zhang YL, Gao G, Shi K et al. Absorption and fluorescence characteristics of rainwater CDOM and contribution to Lake Taihu, China. Atmospheric Environment, 2014, 98: 483-491. DOI:10.1016/j.atmosenv.2014.09.038 |
| [35] |
Stutter MI, Richards S, Dawson JC. Biodegradability of natural dissolved organic matter collected from a UK moorland stream. Water Research, 2013, 47(3): 1169-1180. DOI:10.1016/j.watres.2012.11.035 |
| [36] |
Chen ZQ, Li Y, Pan JM. Distributions of colored dissolved organic matter and dissolved organic carbon in the Pearl River Estuary, China. Continental Shelf Research, 2004, 24: 1845-1856. DOI:10.1016/j.csr.2004.06.011 |
| [37] |
Zhang YL, Liu XH, Wang MZ et al. Compositional differences of chromophoric dissolved organic matter derived from phytoplankton and macrophytes. Organic Geochemistry, 2013, 55: 26-37. DOI:10.1016/j.orggeochem.2012.11.007 |
| [38] |
Zhao J, Cao WX, Wang GF et al. The variations in optical properties of CDOM throughout an algal bloom event. Estuarine, Coastal and Shelf Science, 2009, 82: 225-232. DOI:10.1016/j.ecss.2009.01.007 |
| [39] |
Hu JC, Jiang X, Li YF et al. Influences of environmental governance project on spatial distribution of nitrogen in Lihu Lake. Research of Environmental Science, 2013, 26(4): 380-388. [胡佳晨, 姜霞, 李永峰等. 环境治理工程对五里湖水体中氮空间分布的影响. 环境科学研究, 2013, 26(4): 380-388.] |
| [40] |
Song XN, Yu T, Zhang Y et al. Distribution characterization and source analysis of dissolved organic matters in Taihu Lake using three dimensional fluorescence excitation-emission matrix. Acta Scieniae Circumstantiae, 2010, 30(11): 2321-2331. [宋晓娜, 于涛, 张远等. 利用三维荧光技术分析太湖水体溶解性有机质的分布特征及来源. 环境科学学报, 2010, 30(11): 2321-2331.] |
| [41] |
Copy RM, Mcknight DM. Fluorescence spectroscopy reveals ubiquitous presence of oxidized and reduced quinones in DOM. Environmental Science Technology, 2005, 39: 8142-8149. DOI:10.1021/es0506962 |
| [42] |
Huguet A, Vacher L, Relexans S et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary. Organic Geochemistry, 2009, 40(6): 706-719. DOI:10.1016/j.orggeochem.2009.03.002 |
 2018, Vol. 30
2018, Vol. 30 

