(2: 广东省地质过程与矿产资源探查重点实验室, 广州 510275)
(2: Guangdong Key Laboratory of Geological Processes and Mineral Resource Exploration, Guangzhou 510275, P. R. China)
近年来,温室气体引起的全球变暖问题日益受到关注.尽管二氧化碳(CO2)是大气中的微量气体,但却是引起全球升温的最重要温室气体[1]. IPCC第五次报告指出,自工业革命以来CO2浓度已增加40 % [2],大气中CO2浓度急剧上升主要是由化石燃料的燃烧和水泥生产所导致的[3].修建开发可再生能源的基础设施为减少大气中CO2浓度进而缓解温室效应提供了可能,其中水库因具有灌溉、发电、防洪和养鱼等多种经济效益而被广泛重视.我国是世界上建立水库数量最多的国家,截止到2011年底,我国共有98002座水库,总库容约为9.323×1011 m3[4].
水库修建给当地带来巨大经济和社会效益的同时,也附带产生一系列生态环境问题.人工水库的建立可能会增加温室气体排放、影响库区周围的碳循环机制以及流域内生态系统的平衡.近来的一些研究表明人工水库可能是大气CO2的源[5-8].水库向大气排放温室气体的过程较为复杂,受流域地表理化和生物学性质、人类活动以及水体碳酸盐体系等因素的影响,水库温室气体的源/汇变化表现出一定的地域差异性.已有研究发现,热带和寒温带的水库向大气中排放大量CO2[6, 9-11],其中热带水力发电站向大气排放量更大,如巴西Curuá-Una水库温室气体排放量比利用石油发电所释放出的温室气体还要多3.6倍[11].地处寒温带的加拿大境内水库的温室气体通量要低得多[10, 12],但瑞士温带水库Wohlen湖的CH4排放通量却高于热带水库[13],这说明水库温室气体的排放具有地域性和类型差别性.我国水库数量众多、分布较广且呈逐年增多的趋势.已有研究表明它们多为大气CO2的源,但存在明显的通量差别[14-16].因此,正确衡量我国各类具有代表性的水库水-气界面CO2交换通量对于系统地了解水库在全球或区域碳循环中的角色具有重要意义.
新丰江水库又名万绿湖,是具有发电、防洪、灌溉和航运等综合效益的大型水利工程.该水库位于南亚热带,水温较高,水力滞留时间长;水库流域的降水丰富,年际和年内的降水不均匀[17],其水文及气候条件都对水库的碳源/汇估算有一定影响.基于此本文对新丰江水库丰水期和枯水期的表层水体进行定点采样,分析p(CO2)的时空变化及其影响因素,并计算CO2的扩散通量,探讨南亚热带大型深水贫营养水库——新丰江水库CO2的源/汇问题.
1 数据与方法 1.1 研究区概况新丰江水库(23°43′~24°10′N,114°15′~114°45′E)位于南亚热带季风区的新丰江下游,由距广东省河源市区6 km的亚婆山峡谷修筑拦河大坝蓄水形成,多年平均水深为28.7 m,最大水深为93 m,水库水质为地表水Ⅰ类标准[18-19].水库正常蓄水位水域面积为364 km2,年平均气温为20.8℃,年均降水量为1974.7 m (最大为2857.5 mm,最小为1261.2 mm)[17].库区周围为低山丘陵,土壤为赤红壤,地带性植被为亚热带常绿阔叶林.
1.2 样品采集与分析2012年7月23-24日(丰水期)和2013年1月5-6日(枯水期)乘船以5 km/h的速度航行,每隔15 min用抽水泵(广州钜豪OHZ-128A)采集水库表层0.5 m深水样并用GPS记录采样点位置(图 1).

|
图 1 新丰江水库丰水期(a)和枯水期(b)采样点分布 Fig.1 Distribution of sampling sites in wet (a) and dry (b) seasons in the Xinfengjiang Reservoir |
水温(T)、pH值、叶绿素a(Chl.a)浓度和溶解氧(DO)浓度使用UltrameterTM Model 6P型便携式电导率仪(美国Myron L公司)和Hydrolab DS5(美国Hach公司)现场测量,测试精度分别为±0.1℃、±0.01、±0.01 μg/L和±0.01 mg/L.阴离子(Cl-、SO42-和NO3-)、阳离子(K+、Ca2+、Na+和Mg2+)、溶解硅(DSi)、溶解无机碳(DIC)、溶解有机碳(DOC)以及碱度(Alkalinity,Alk)等指标需将水样装入聚乙烯瓶中带回实验室测定,其中阴离子采用ICS-900型离子色谱仪(美国戴安)测定,阳离子和DSi浓度采用IRIS(HR)型全谱直读等离子体原子发射光谱仪(ICP-AES,美国TJA)测定,DIC和DOC浓度采用TOC-V型总有机碳分析仪(日本岛津)测定,Alk采用TIM856型自动滴定仪(Radiometer)测定.在盛装水样前抽取现场水体清洗采样瓶3次以上,盛装过程中尽量避免出现空隙,将水样密封后装入黑色塑料袋中储存在阴暗处,为避免微生物活动影响,在测DOC的滤液中加入一滴过饱和HgCl2溶液.将采集的样品带回实验室后4℃左右冷藏并在一周内完成测定.采集的样品用孔径为0.7 μm的滤膜(Whatman GF/F)过滤,滤膜使用前用锡纸包装放入马弗炉(上海康路5-12型号)在450℃温度下灼烧24 h.样品过滤后将滤液装入用去离子水充分清洗的聚乙烯瓶.
1.3 基于水化学平衡的p(CO2)计算理论上,水体中溶解无机碳(DIC)由重碳酸盐(HCO3-)、碳酸根离子(CO32-)、碳酸(H2CO3)和溶解态CO2(aq)组成,水溶液平衡时各个组分的浓度与pH值、温度和离子强度有关[20].根据pH、HCO3-、亨利常数(Kh)以及水中主要离子含量可计算碳酸盐体系中的p(CO2),其反应可用下列各式表达[21]:
| $ {\rm{C}}{{\rm{O}}_2} + {{\rm{H}}_2}{\rm{O}} \rightleftharpoons {{\rm{H}}_2}{\rm{CO}}_3^ * \rightleftharpoons {{\rm{H}}^ + } + {\rm{HCO}}_3^ - \rightleftharpoons 2{{\rm{H}}^ + } + {\rm{CO}}_3^{2 - } $ | (1) |
| $ {K_{{\rm{C}}{{\rm{O}}_2}}} = \left[ {{{\rm{H}}_2}{\rm{CO}}_3^ * } \right]\left[ {p\left( {{\rm{C}}{{\rm{O}}_2}} \right)} \right] $ | (2) |
| $ {K_1} = \left[ {{{\rm{H}}^ + }} \right]\left[ {{\rm{HCO}}_3^ - } \right]/\left[ {{{\rm{H}}_2}{\rm{CO}}_3^ * } \right] $ | (3) |
| $ {K_2} = \left[ {{{\rm{H}}^ + }} \right]\left[ {{\rm{CO}}_3^{2 - }} \right]/\left[ {{\rm{HCO}}_3^ - } \right] $ | (4) |
| $ p{K_{{\rm{C}}{{\rm{O}}_2}}} = - 7 \times {10^{ - 5}}{T^2} + 0.016T + 1.11 $ | (5) |
| $ p{K_1} = 1.1 \times {10^{ - 4}}{T^2} - 0.012T + 6.58 $ | (6) |
| $ p{K_2} = 9 \times {10^{ - 5}}{T^2} - 0.0137T + 10.62 $ | (7) |
式中,pKCO2、pK1和pK2分别表示KCO2、K1和K2的负对数,其中T表示水温(℃).
根据亨利定律,p(CO2)可由下式计算:
| $ p\left( {{\rm{C}}{{\rm{O}}_2}} \right) = \left[ {{{\rm{H}}_2}{\rm{CO}}_3^ * } \right]/{K_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}} = \alpha \left( {{{\rm{H}}^ + }} \right) \cdot \alpha \left( {{\rm{HCO}}_3^ - } \right)/\left( {{K_{{\rm{C}}{{\rm{O}}_2}}} \cdot {K_1}} \right) $ | (8) |
式中,α(H+)和α(HCO3-)分别表示H+和HCO3-的离子活度,可由下式计算:
| $ \alpha \left( {{{\rm{H}}^ + }} \right) = {10^{ - \left[ {{\rm{pH}}} \right]}} $ | (9) |
| $ \alpha \left( {{\rm{HCO}}_3^ - } \right) = \left[ {{\rm{HCO}}_3^ - } \right] \times {10^{ - 0.5\sqrt I }} $ | (10) |
| $ I = 0.5\left( {\left[ {{{\rm{K}}^ + }} \right] + 4\left[ {{\rm{C}}{{\rm{a}}^{2 + }}} \right] + \left[ {{\rm{N}}{{\rm{a}}^{2 + }}} \right] + 4\left[ {{\rm{M}}{{\rm{g}}^{2 + }}} \right] \\+ \left[ {{\rm{C}}{{\rm{l}}^ - }} \right] + 4\left[ {{\rm{SO}}_4^{2 - }} \right] + \left[ {{\rm{NO}}_3^ - } \right] + \left[ {{\rm{HCO}}_3^ - } \right]} \right)/1000000 $ | (11) |
式中,I表示离子强度.
1.4 水-气界面CO2扩散通量的计算水-气界面CO2扩散受到大气和水体中p(CO2)之差、温度、盐度、风速等因素影响.水-气二氧化碳扩散通量计算公式为:
| $ {F_{{\rm{C}}{{\rm{O}}_2}}} = {k_0} \cdot {k_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}} \cdot \Delta p\left( {{\rm{C}}{{\rm{O}}_2}} \right) $ | (12) |
式中,FCO2为水-气CO2扩散通量(mmol/(m2 ·d)),k0为某气温条件下CO2溶解度(mol/L ·atm),kCO2为CO2交换系数(cm/h),Δp(CO2)=p(CO2)(water)-p(CO2)(air),表示水体p(CO2)与大气p(CO2)的差值,p(CO2)(air)由Vaisala CARBOCAP手持式二氧化碳测量仪GM70(Vaisala公司生产)测定.若水体p(CO2)高于大气p(CO2),FCO2为正,表示水体是大气的源,向大气释放CO2;若水体p(CO2)低于大气p(CO2),FCO2为负,表示水体是大气的汇,从大气吸收CO2.
k0大小受到水体中温度、盐度、压强等因素的影响,其计算公式为[23]:
| $ \ln {k_0} = {{\rm{A}}_1} + {{\rm{A}}_2}\left( {100/T} \right) + {{\rm{A}}_3}\ln \left( {T/100} \right) + S\left[ {{{\rm{B}}_1} + {{\rm{B}}_2}\left( {T/100} \right) + {{\rm{B}}_3}{{\left( {T/100} \right)}^2}} \right] $ | (13) |
式中,常数A1、A2、A3、B1、B2和B3分别为-58.0931、90.5069、22.2940、0.027766、-0.025888和0.0050578. S为盐度(‰),T为开尔文温度(K).
kCO2是水-气CO2扩散通量计算的关键,但由于kCO2的计算方式较多,其选取与估算仍存在很大争议,其中比较常用的有以下3种计算模式.
在海洋研究中应用较为广泛的为Wanninkhof[24]模式:
| $ {k_{{\rm{C}}{{\rm{O}}_{2{\rm{wan}}}}}} = 0.39{U^2}{\left( {Sc/600} \right)^{ - 0.5}} $ | (14) |
在湖泊、水库研究中应用较多的是Cole[20]和Upstill[25]模式:
| $ {k_{{\rm{C}}{{\rm{O}}_{2{\rm{cole}}}}}} = {k_{600}}\left( {{{600}^{0.67}}} \right)/S{c^{0.67}} $ | (15) |
| $ {k_{600}} = 2.07 + 0.215{U^{1.7}} $ | (16) |
| $ {k_{{\rm{C}}{{\rm{O}}_{2{\rm{up}}}}}} = 1.11U + 0.35 $ | (17) |
式中,U为采样时间点的平均风速(m/s),数据来自气象数据共享网站(http://data.cma.cn/)中国地面国际交换站日值数据集河源站点. Sc是在t℃下CO2的Schmidt常数,其计算公式为:Sc=1911.1-118.11t+3.4527t2-0.04132t3.
1.5 数据处理运用Excel 2013软件对数据进行统计计算,运用ArcGIS 10.0和Origin 9.0软件制作图表,运用SPSS 19.0软件对数据进行相关性分析.
2 结果 2.1 新丰江水库水质参数变化水质参数反映水体的理化及生物学性质.温度主要影响水体的物理性质,表层水温高低间接反映了太阳辐射的强弱,是水体对外界气候变化的综合性响应.水库水温季节性变化较为明显,丰水期的水温高出枯水期近15℃(表 1),这会导致丰水期水体出现温度分层现象[14],进而阻碍表层水体与下层水体之间物质、能量交换,影响CO2扩散通量的大小和方向. pH值受到水生生物光合作用和呼吸作用以及水中碳酸盐平衡体系的共同影响,在一定程度上影响着物质的转化和迁移.新丰江水库水体的pH值季节差别不大,均为弱碱性,这是因为浮游植物光合作用吸收大量CO2,释放大量O2,使pH升高,此外水中还含有大量K+、Ca2+、Na+、Mg2+等离子,因此水库水体pH值整体呈现弱碱性.丰水期和枯水期Chl.a浓度的变异系数分别为56.74 %和45.86 %,说明水体Chl.a的稳定性较弱,并且丰水期水体Chl.a与枯水期相比较不稳定,同时说明水库中Chl.a分布极不均衡.丰水期的DO浓度较枯水期低,因为丰水期水温较高,微生物代谢耗氧量大[26].丰水期DOC浓度大于枯水期,说明随着降雨的增加,水库输入了一定量的陆源DOC.此外,丰水期水体中的Chl.a、DSi、NO3-、Alk和DIC浓度也均小于枯水期,反映出丰水期水体对稀释效应的响应[27].
| 表 1 新丰江水库表层水体水质参数 Tab.1 Quality parameters of surface water in the Xinfengjiang Reservoir |
新丰江水库p(CO2)的分布存在较大的季节性差异.丰水期p(CO2)从水库上游到坝前逐渐升高(图 2a),在坝前狭窄的水道前以及水库西南侧达到最高,为3545 μatm;在丰水期14#采样点,p(CO2)达到最小值,为16 μatm.枯水期p(CO2)值从水库上游到坝前呈下降趋势(图 2b),其变化趋势与丰水期相反.在水库上段的枯水期21#采样点,p(CO2)达到最大值,为1355 μatm;在水库下段的枯水期1#采样点,p(CO2)达到最小值(399 μatm). p(CO2)均值在丰水期(999 μatm)大于枯水期(756 μatm),这是因为丰水期水库上游带来大量有机物,为生物呼吸作用和分解作用提供营养物质,产生大量CO2.新丰江水库表层水体丰水期和枯水期p(CO2)均值为877 μatm,略小于全球湖泊平均值1000 μatm[28],但远大于现今全球大气CO2平均浓度(409 μatm)[29].

|
图 2 新丰江水库丰水期(a)和枯水期(b) p(CO2)的时空变化 Fig.2 Temporal and spatial variation of p(CO2) in wet (a) and dry (b) seasons in the Xinfengjiang Reservoir |
温度会影响碳酸盐的热力学平衡,一般情况下,p(CO2)随着温度的升高而增大[30].新丰江水库丰水期和枯水期表层水温分别为28~30.9℃和16.13~17.13℃,其变化范围均小于2℃,对水库p(CO2)影响较小.本文利用Zhai等[31]的温度校正的经验公式将丰水期和枯水期p(CO2)矫正到丰水期和枯水期的平均温度,具体计算公式为:
| $ {\rm{N}}p\left( {{\rm{C}}{{\rm{O}}_2}} \right) = p\left( {{\rm{C}}{{\rm{O}}_2}} \right) \cdot \exp \left[ {\left( {0.215S + 1.875} \right)\left( {{T_{{\rm{mean}}}} - {T_{{\rm{obs}}}}} \right)/100} \right] $ | (18) |
式中,Tobs和Tmean分别为原位实测水温和采样期间平均水温(℃),S为盐度(‰),p(CO2)为实测p(CO2).校正之后的p(CO2) (Np(CO2))分布趋势与校正前一致.丰水期p(CO2)校正后为16.51~3626.41 μatm,平均值增加了20.12 μatm;枯水期p(CO2)校正后为397.68~362.95 μatm,平均值增加了0.57 μatm.温度的校正并没有显著改变新丰江水库p(CO2)的源/汇角色,说明温度对采样时水库丰水期和枯水期p(CO2)分布的影响较小.
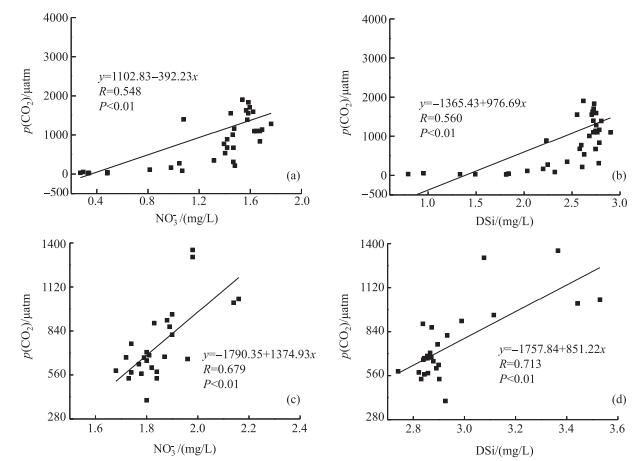
3.1.2 p(CO2)与营养盐DSi、NO3-浓度的关系营养盐是浮游植物的生长的限制性因素[32],其浓度高低在一定程度上影响有机物的生产速率.丰水期与枯水期p(CO2)与NO3-、DSi浓度均呈显著正相关(图 3).但丰水期和枯水期影响p(CO2)与NO3-、DSi浓度相互关系的因素却不尽相同.丰水期NO3-、DSi浓度与p(CO2)从水库上游到坝前逐渐升高,而枯水期NO3-、DSi浓度与p(CO2)则呈下降趋势.丰水期在8#~11#采样点(水库上游)Chl.a浓度均较高(均在3 μg/L以上,在10#采样点达到7.75 μg/L),NO3-和DSi浓度在此处达到最小(NO3-浓度低于0.5 mg/L,DSi浓度低于1.5 mg/L),这间接表明浮游植物由于吸收了大量NO3-、DSi进行光合作用,其生长较为茂盛,进而影响p(CO2)的大小.而枯水期在25#、26#采样点处(丰水期8#~11#采样点附近)NO3-、DSi浓度却达到最高,这与枯水期水库中的微生物对有机质的降解有关[33],当枯水期DO浓度取最小值7.37 mg/L时,DSi和NO3-浓度较大,分别为3.08和1.98 mg/L,此时的p(CO2)与枯水期p(CO2)最大值相近,高达1310.16 μatm.这意味随着微生物分解作用增强,DO浓度随之减少,产生大量生营养盐以及CO2,使p(CO2)升高.
|
图 3 新丰江水库丰水期(a、b)和枯水期(c、d) p(CO2)与NO3-和DSi浓度的相互关系 Fig.3 Relationship among p(CO2), NO3- and DSi concentrations in wet(a, b) and dry(c, d) seasons in the Xinfengjiang Reservoir |
水中Chl.a浓度可以定量表征浮游植物的量[34],浮游植物则通过光合作用吸收水体中的CO2,使水中的p(CO2)降低,浮游植物的光合作用表达式为:
| $ 136{\rm{C}}{{\rm{O}}_2} + 16{\rm{NO}}_3^ - + {\rm{HPO}}_4^{2 - } + 0.5{\rm{SO}}_4^{2 - } + 85{{\rm{H}}_2}{\rm{O + 19}}{{\rm{H}}^ + } \\= {{\rm{C}}_{136}}{{\rm{H}}_{190}}{{\rm{O}}_{37}}{{\rm{N}}_{16}}{{\rm{P}}_1}{{\rm{S}}_{0.5}} + 188{{\rm{O}}_2} $ | (19) |
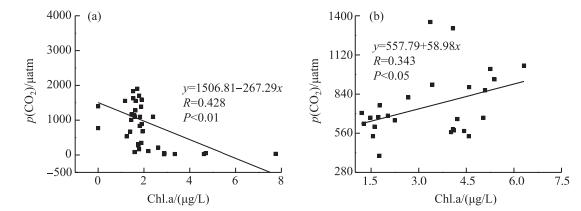
新丰江水库中的浮游植物种类繁多,丰水期以蓝、绿藻为主,枯水期以硅藻为优势种群[17, 19].水库位于华南地区,丰水期降雨充沛,水体中携带大量上游冲刷下来的陆源性营养物[35].水中浮游植物吸收水体中的NO3-、DSi以及CO2进行光合作用,使水中pH升高,从而使p(CO2)降低,因此丰水期Chl.a浓度与p(CO2)呈负相关(图 4a)[36].此外丰沛的降雨还带来了上游水体中的泥沙和悬浮物,水库的透光度降低,这影响了浮游植物的光合作用强度,因此水体Chl.a浓度达到最大值7.75 μg/L时,水体中的p(CO2)(30.77 μatm)仍然大于丰水期p(CO2)的最小值.这说明丰水期浮游植物的光合作用是受到限制的,光合作用并不是影响水中p(CO2)大小的唯一因素.此外,悬浮物能在一定程度上影响浮游动物对浮游植物的捕食[37],降低Chl.a浓度进而影响水中p(CO2)大小.枯水期p(CO2)与Chl.a浓度呈正相关(图 4b),Zhang等[38]发现由于浮游动物的摄食作用南黄海春末p(CO2)与Chl.a呈正相关关系.新丰江水库的浮游动物有22种,丰水期以轮虫为主,枯水期以挠足类浮游动物为主,枯水期生物量大于丰水期[18, 39].因此枯水期p(CO2)与Chl.a浓度呈正相关,这可能与浮游动物的摄食有关.
|
图 4 新丰江水库丰水期(a)和枯水期(b)p(CO2)与Chl.a浓度的相互关系 Fig.4 Relationship between p(CO2) and Chl.a concentration in wet(a) and dry(b) seasons in the Xinfengjiang Reservoir |
枯水期DIC浓度大于丰水期,这是因为丰水期径流量较大,水体发生稀释效应[27].在枯水期23#采样点,DIC浓度出现最大值(7.44 mg/L),同时NO3-、ALK、Chl.a和DSi浓度均达到最大,p(CO2)高达1043.04 μatm.新丰江水库的DIC浓度与亚马逊河的DIC浓度[40]相近,但远远低于黄河河流水体[41]和密西西北河[42]水体的DIC浓度.珠江口水体p(CO2)主要受到呼吸作用的影响,其p(CO2)与DIC浓度呈负相关[31].而黄河的水体p(CO2)主要受到碳酸盐平衡体系控制,p(CO2)与DIC浓度呈正相关[41].泰晤士河的p(CO2)由于受到光合作用和呼吸作用双重影响,与DIC浓度无明显相关性[43],新丰江水库研究结果与之一致(图 5a),说明新丰江水库丰水期的p(CO2)受到浮游植物的光合作用和微生物、藻类的呼吸作用影响.枯水期p(CO2)与DIC浓度呈正相关(图 5b),表明枯水期水库中水体通过碳酸盐系统水化学平衡原理[41],调整HCO3-、CO32-、CO2和H2CO3等DIC浓度的各分量,而在一定程度上控制水中的p(CO2)大小.

|
图 5 新丰江水库丰水期(a)和枯水期(b)p(CO2)与DIC浓度的相互关系 Fig.5 Relationship between p(CO2) and DIC concentration in wet (a) and dry (b) seasons in the Xinfengjiang Reservoir |
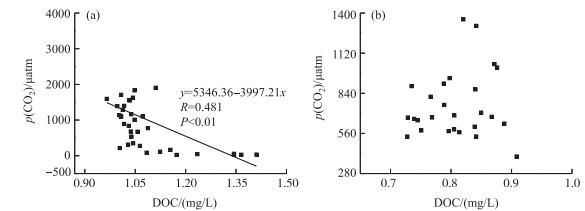
水库中的DOC来源分为内源DOC和外源DOC.内源DOC指的是水库浮游植物光合作用、细菌分解作用等产生的有机物;外源DOC指来自土壤有机物降解和人类生产、生活的排废物[21, 26-27].在富含有机碳的湖泊或者水库中,微生物对外源DOC进行降解,p(CO2)与DOC浓度呈现良好的正相关性;而土壤层薄弱,外源DOC输入较低的水库或湖泊,p(CO2)与DOC浓度呈负相关;水库中浮游植物吸收CO2进行光合作用产生有机物,p(CO2)与DOC浓度也呈负相关[44].新丰江水库丰水期p(CO2)与DOC浓度呈负相关(图 6a),这是因为新丰江水库水力滞留时间长达2 a[18],其DOC可能以内源DOC为主.枯水期p(CO2)与DOC浓度没有明显相关性(图 6b),是因为枯水期浮游植物光进行合作用产生CO2但是其作用弱于丰水期,同时细菌利用内源DOC进行呼吸作用释放CO2,枯水期水库CO2吸收与释放受到两个相反过程的限制.
|
图 6 新丰江水库丰水期(a)和枯水期(b)p(CO2)与DOC浓度的相互关系 Fig.6 Relationship between p(CO2) and DOC concentration in wet (a) and dry (b) seasons in the Xinfengjiang Reservoir |
气体交换系数kCO2的选取对水-气界面的CO2交换通量(FCO2)的计算至关重要,其大小受到水电导率、流速、风速等众多因素的影响[45].水库与海洋在水流模式及底部地貌形态方面相差甚远[46-47].水库水域面积远小于海洋且地处内陆,与陆地生态系统的物质、能量、信息交换强烈,因此Wanninkhof模式计算出来的kCO2与基于水库、湖泊计算出来的kCO2略有不同(表 2),故不选取Wanninkhof模式计算新丰江水库FCO2,而选取基于水库、湖泊的kCO2计算模式计算新丰江水库FCO2.
| 表 2 不同模式计算的FCO2 Tab.2 Values of FCO2 calculated by different patterns |
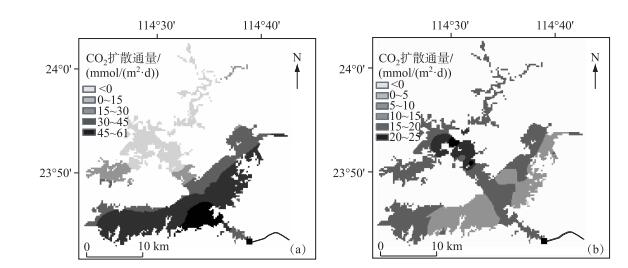
将基于Cole和Upstill模式计算的FCO2求平均值后,在ArcGIS中运用Kriging插值方法得出新丰江水库丰水期和枯水期的FCO2(图 7).丰水期FCO2从水库上游到坝前逐渐增大,在水库上段FCO2为负值,是大气CO2的汇,在水库下段FCO2均为正值,是大气CO2的源;枯水期FCO2从水库上游到坝前逐渐减小,总的来说是大气CO2的源,只有在1#采样点FCO2为负值,其余均为正值.总而言之,枯水期和丰水期FCO2均值为正值且丰水期FCO2较枯水期大,因此新丰江水库是一个大气CO2源.在ArcGIS中运用区域统计分析求得新丰江水库丰水期和枯水期FCO2的均值分别为20.78和8.09 mmol/(m2 ·d).
|
图 7 新丰江水库枯水期(a)和丰水期(b)表层CO2扩散通量 Fig.7 Surface degassing flux of CO2 in wet (a) and dry (b) seasons in the Xinfengjiang Reservoir |
由表 3可知亚热带水库FCO2值略大于部分温带水库,但远远小于热带水库.新丰江水库FCO2不仅小于世界上水力发电的水库,而且与中国其他水库相比也较小.这是因为新丰江水库属于贫营养水库,水库中CO2的释放与水库沉积物中有机物的种类和数量等有关[33].新丰江水库地处亚热带季风区,温度相对于巴西等热带地区较低,有机碳的降解率较低,其次新丰江水库为山谷型水库,水库淹没面积较小,并且库区内生态环境较好,有机质含量相对较小,因此生物代谢产生的CO2较少,FCO2值也较低.此外,从建库至2013年新丰江水库已有55 a历史,随着蓄水年限的延长,水库淹没区域的有机质降解强度逐渐下降,温室气体释放通量逐渐降低,这与Louis等[6]在美国Wisconsin州内对不同库龄水库的温室气体排放研究结果相似.
| 表 3 世界主要水库的FCO2比较 Tab.3 Values of FCO2 of main reservoirs in the world |
运用2012年7月和2013年1月新丰江水库的水质参数,计算新丰江水库p(CO2)并讨论其时空分布与影响因素,最后计算新丰江水库的CO2扩散通量,可得到以下结论:
1) 新丰江水库p(CO2)变化有明显季节性.丰水期p(CO2)从水库上游到坝前逐渐升高,枯水期p(CO2)从水库上游到坝前呈下降趋势.
2) 新丰江水库丰水期和枯水期p(CO2)受温度影响均较小,丰水期p(CO2)与NO3-和DSi浓度呈正相关,与Chl.a和DOC浓度呈显著负相关,与DIC浓度没有明显相关性;枯水期p(CO2)与NO3-、DSi、Chl.a和DIC浓度均呈显著正相关,与DOC浓度没有明显相关性.
3) 运用Wanninkhof、Cole、Upstill模式计算出来的新丰江水库全年CO2扩散通量均值均为正值,且丰水期CO2扩散通量较枯水期大.水库CO2扩散通量略大于部分温带地区,但远远小于热带地区.总的来说新丰江水库是一个通量值偏低的大气CO2源.
| [1] |
Gao QZ, Shen CD. Riverine carbon flux and continental erosion. Advance in Earth Sciences, 1998, 13(4): 369-375. [高全洲, 沈承德. 河流碳通量与陆地侵蚀研究. 地球科学进展, 1998, 13(4): 369-375.] |
| [2] |
IP CC. Working group Ⅰ contribution to the IPCC Fifth Assessment Report-climate change 2013:the physical science basis. Cambridge: Cambridge University Press, 2013.
|
| [3] |
Sabine CL, Feely RA, Gruber N et al. The oceanic sink for anthropogenic CO2. Science, 2004, 305(5682): 367-371. DOI:10.1126/science.1097403 |
| [4] |
Sun ZG, Zhang L, Duan ZD. The quantity and distribution of reservoir engineering in China. China Water Resources, 2013, 48(7): 10-11. [孙振刚, 张岚, 段中德. 我国水库工程数量及分布. 中国水利, 2013, 48(7): 10-11.] |
| [5] |
Duchemin E, Lucotte M, Canuel R et al. Production of the greenhouse gases CH4 and CO2 by hydroelectric reservoirs of the boreal region. Global Biogeochemical Cycles, 1995, 9(4): 737-757. DOI:10.1029/95GB02202 |
| [6] |
Louis VLS, Kelly CA, Duchemin E et al. Reservoir surfaces as sources of greenhouse gases to the atmosphere:a global estimate. Bioscience, 2000, 50(9): 766-775. DOI:10.1641/0006-3568(2000)050[0766:RSASOG]2.0.CO;2 |
| [7] |
Santos MAD, Rosa LP, Sikar B et al. Gross greenhouse gas fluxes from hydro-power reservoir compared to thermo-power plants. Energy Policy, 2006, 34(4): 481-488. DOI:10.1016/j.enpol.2004.06.015 |
| [8] |
Raymond PA, Hartmann J, Lauerwald R et al. Global carbon dioxide emissions from inland waters. Nature, 2013, 503(7476): 355-359. DOI:10.1038/nature12760 |
| [9] |
Tremblay A, Lambert M, Gagnon L. Do hydroelectric reservoirs emit greenhouse gases?. Environmental Management, 2004, 33(1): S509-S517. DOI:10.1007/s00267-003-9158-6 |
| [10] |
Yang L, L uF, Zhou X et al. Progress in the studies on the greenhouse gas emissions from reservoirs. Acta Ecologica Sinica, 2014, 34(4): 204-212. DOI:10.1016/j.chnaes.2013.05.011 |
| [11] |
Fearnside PM. Do hydroelectric dams mitigate global warming? The case of Brazil's CuruÁ-una Dam. Mitigation & Adaptation Strategies for Global Change, 2005, 10(4): 675-691. DOI:10.1007/s11027-005-7303-7 |
| [12] |
Demarty M, Bastien J, Tremblay A et al. Greenhouse gas emissions from boreal reservoirs in Manitoba and Quebec, Canada, measured with automated systems. Environmental Science & Technology, 2009, 43(23): 8908-8915. DOI:10.1021/es8035658 |
| [13] |
Delsontro T, Mcginnis DF, Sobek S et al. Extreme methane emissions from a Swiss hydropower reservoir:contribution from bubbling sediments. Environmental Science & Technology, 2010, 44(7): 2419-2425. DOI:10.1021/es9031369 |
| [14] |
Li S, Wang YC, Cao M et al. Partial pressure and diffusion flux of mainstream and tributary of the central dissolved carbon dioxide in the Three Gorges Reservoir in summer. Environmental Science, 2014, 35(3): 885-891. [李双, 王雨春, 操满等. 三峡库区库中干流及支流水体夏季二氧化碳分压及扩散通量. 环境科学, 2014, 35(3): 885-891.] |
| [15] |
Mei HY, Wang FS, Yao CC et al. Diffusion flux of partial pressure of dissolved carbon dioxide in Wan'an Reservoir in spring. Environmental Science, 2011, 32(1): 58-63. [梅航远, 汪福顺, 姚臣谌等. 万安水库春季二氧化碳分压的分布规律研究. 环境科学, 2011, 32(1): 58-63.] |
| [16] |
Yang L, Lu F, Wang X et al. Spatial and seasonal variability of CO2 flux at the air-water interface of the Three Gorges Reservoir. Journal of Environmental Sciences, 2013, 25(11): 2229-2238. DOI:10.1016/S1001-0742(12)60291-5 |
| [17] |
Hu R, Lei LM, Han BP. Phytoplankton assemblage and seasonal dynamics in the large oligotrophy in Xinfengjiang reservoir in southern China. Acta Ecologica Sinica, 2008, 28(10): 4652-4664. [胡韧, 雷腊梅, 韩博平. 南亚热带大型贫营养水库浮游植物群落结构与季节变化——以新丰江水库为例. 生态学报, 2008, 28(10): 4652-4664. DOI:10.3321/j.issn:1000-0933.2008.10.005] |
| [18] |
Zhao SY, Han BP. Structural analysis of zooplankton community in a large deep oligotrophic reservoir-Xinfengjiang Reservoir, South China. J Lake Sci, 2007, 19(3): 305-314. [赵帅营, 韩博平. 大型深水贫营养水库——新丰江水库浮游动物群落分析. 湖泊科学, 2007, 19(3): 305-314. DOI:10.18307/2007.0312] |
| [19] |
Chen LF, Lin QJ, Hu R et al. Plankton community in a subtropical large reservoir (Xinfengjiang reservoir). Ecologic Science, 2002, 21(2): 104-107. [陈丽芬, 林举贤, 胡韧等. 亚热带大型水库——新丰江水库的浮游生物群落特征. 生态科学, 2002, 21(2): 104-107.] |
| [20] |
Cole JJ, Caraco NF. Atmospheric exchange of carbon dioxide in a low-wind oligotrophic lake measured by the addition of SF6. Limnology & Oceanography, 1998, 43(4): 647-656. DOI:10.4319/lo.1998.43.4.0647 |
| [21] |
Yao G, Gao Q, Wang Z et al. Dynamics of CO2 partial pressure and CO2 outgassing in the lower reaches of the Xijiang River, a subtropical monsoon river in China. Science of the Total Environment, 2007, 376(1/2/3): 255-266. DOI:10.1016/j.scitotenv.2007.01.080 |
| [22] |
Telmer K, Veizer J. Carbon fluxes, pCO2, and substrate weathering in a large northern river basin, Canada:carbon isotope perspectives. Chemical Geology, 1999, 159(1/2/3/4): 61-86. DOI:10.1016/S0009-2541(99)00034-0 |
| [23] |
Weiss RF. The solubility of nitrogen, oxygen and argon in water and seawater. Deep Sea Research and Oceanographic Abstracts, 1970, 17(4): 721-735. DOI:10.1016/0011-7471(70)90037-9 |
| [24] |
Wanninkhof R. Relationship between wind speed and gas exchange over the ocean. Journal of Geophysical Research Atmospheres, 1992, 12(6): 351-362. DOI:10.1029/92JC00188 |
| [25] |
Upstill-Goddard RC, Watson AJ, Liss PS et al. Gas transfer velocities in lakes measured with SF 6. Tellus Series B-chemical & Physical Meteorology, 1990, 42(4): 364-377. DOI:10.3402/tellusb.v42i4.15230 |
| [26] |
Varola M, Siyue L. Biotic and abiotic controls on CO2 partial pressure and CO2 emission in the Tigris River, Turkey. Chemical Geology, 2017, 449(1): 182-193. DOI:10.1016/j.chemgeo.2016.12.003 |
| [27] |
Li S, Lu XX, He M et al. Daily CO2 partial pressure and CO2 outgassing in the upper Yangtze River basin:A case study of the Longchuan River, China. Journal of Hydrology, 2012, 466/467(5): 141-150. DOI:10.1016/j.jhydrol.2012.08.011 |
| [28] |
Cole JJ, Caraco NF, Kling GW et al. Carbon dioxide supersaturation in the surface waters of lakes. Science, 1994, 265(5178): 1568-1570. DOI:10.1126/science.265.5178.1568 |
| [29] |
https: //www. co2. earth/2017. 8. 9.
|
| [30] |
Takahashi T, Olafsson J, Goddard JG et al. Seasonal variation of CO2 and nutrients in the high-latitude surface oceans:A comparative study. Global Biogeochemical Cycles, 1993, 7(4): 843-878. DOI:10.1029/93GB02263 |
| [31] |
Zhai WD, Dai MH, Cai WJ et al. High partial pressure of CO2 and its maintaining mechanism in a subtropical estuary:The Pearl River estuary, China. Marine Chemistry, 2005, 93(1): 21-32. DOI:10.1016/j.marchem.2004.07.003 |
| [32] |
Zhang W, Sun J, Nie HT et al. Seasonal and spatial variations of nutrient and the response of phytoplankton in PRE and Adjacent Sea Areas. Acta Ecologica Sinica, 2015, 35(12): 4034-4044. [张伟, 孙健, 聂红涛等. 珠江口及毗邻海域营养盐对浮游植物生长的影响. 生态学报, 2015, 35(12): 4034-4044.] |
| [33] |
Lv YC, Liu CQ, Wang SL et al. Distribution of p(CO2) in Hongfeng lake in summer stratification. Advances in Water Science, 2008, 19(1): 106-110. [吕迎春, 刘丛强, 王仕禄等. 红枫湖夏季分层期间p(CO2)分布规律的研究. 水科学进展, 2008, 19(1): 106-110.] |
| [34] |
Krasakopoulou E, Rapsomanikis S, Papadopoulos A et al. Partial pressure and air-sea CO2 flux in the Aegean Sea during February 2006. Continental Shelf Research, 2009, 29(11/12): 1477-1488. DOI:10.1016/j.csr.2009.03.015 |
| [35] |
Yin K. Monsoonal influence on seasonal variations in nutrients and phytoplankton biomass in coastal waters of Hong Kong in the vicinity of the Pearl River estuary. Marine Ecology, 2002, 245(4): 111-122. DOI:10.3354/meps245111 |
| [36] |
Tan Y, Zhang LJ, Wang F et al. Summer surface water pCO2 and CO2 flux at air-sea interface western part of the East China Sea. Oceanologia Et Limnologia Sinica, 2004, 35(3): 239-245. [谭燕, 张龙军, 王凡等. 夏季东海西部表层海水中的pCO2及海-气界面通量. 海洋与湖沼, 2004, 35(3): 239-245.] |
| [37] |
Zhou LB, Chen FZ. Effect of sediment resuspension on predation of planktivorous fish on zooplankton. J Lake Sci, 2015, 27(5): 911-916. [周礼斌, 陈非洲. 沉积物再悬浮对食浮游动物鱼类捕食浮游动物的影响. 湖泊科学, 2015, 27(5): 911-916. DOI:10.18307/2015.0518] |
| [38] |
Zhang L, Xue L, Song M et al. Distribution of the surface partial pressure of CO2 in the southern Yellow Sea and its controls. Continental Shelf Research, 2010, 30(3/4): 293-304. DOI:10.1016/j.csr.2009.11.009 |
| [39] |
Li Y, Lin QQ, Han BP. Comparative analysis of community structures of planktonic copepods in three large reservoirs, south China. Ecologic Science, 2010, 29(1): 22-29. [李莹, 林秋奇, 韩博平. 三座南亚热带大型水库敞水区桡足类群落结构比较. 生态科学, 2010, 29(1): 22-29.] |
| [40] |
Ternon JF, Oudot C, Dessier A et al. A seasonal tropical sink for atmospheric CO2 in the Atlantic Ocean:the role of the Amazon River discharge. Marine Chemistry, 2000, 68(3): 183-201. DOI:10.1016/S0304-4203(99)00077-8 |
| [41] |
Su Z, Zhang LJ, Wang XL. Influencing factors of partial pressure of CO2 in Huanghe (Yellow) River. Marine Sciences, 2005, 29(4): 41-44. [苏征, 张龙军, 王晓亮. 黄河河流水体二氧化碳分压及其影响因素分析. 海洋科学, 2005, 29(4): 41-44.] |
| [42] |
Cai WJ. Riverine inorganic carbon flux and rate of biological uptake in the Mississippi River plume. Geophysical Research Letters, 2003, 30(2): 61-79. DOI:10.1029/2002GL016312 |
| [43] |
Neal C, Harrow M, Williams RJ. Dissolved carbon dioxide and oxygen in the River Thames:Spring-summer 1997. Science of the Total Environment, 1998, 210/211(6): 205-217. DOI:10.1016/S0048-9697(98)00013-8 |
| [44] |
Lv YC, Liu CQ, Wang SL et al. Seasonal variability of p(CO2) in the two Karst reservoirs, Hongfeng and Baihua Lakes in Guizhou Province, China. Environmental Science, 2007, 28(12): 2674-2681. [吕迎春, 刘丛强, 王仕禄等. 贵州喀斯特水库红枫湖、百花湖p(CO2)季节变化研究. 环境科学, 2007, 28(12): 2674-2681. DOI:10.3321/j.issn:0250-3301.2007.12.002] |
| [45] |
Abril G, Etcheber H, Borges AV et al. Excess atmospheric carbon dioxide transported by rivers into the Scheldt estuary. Comptes Rendus de l'Academie des Sciences Series ⅡA Earth and Planetary Science, 2000, 330(11): 761-768. DOI:10.1016/S1251-8050(00)00231-7 |
| [46] |
Broecker WS, Peng TH. Gas exchange rates between air and sea. Tellus, 1974, 26(1/2): 21-35. DOI:10.1111/j.2153-3490.1974.tb01640.x |
| [47] |
Crusius J, Wanninkhof R. Gas transfer velocities measured at low wind speed over a lake. Limnology & Oceanography, 2003, 48(3): 1010-1017. DOI:10.4319/lo.2003.48.3.1010 |
| [48] |
Kemenes A, Forsberg BR, Melack JM. CO2 emissions from a tropical hydroelectric reservoir (Balbina, Brazil). Journal of Geophysical Research Biogeosciences, 2011, 116(G3): 1-11. DOI:10.1029/2010JG001465 |
| [49] |
Soumis N, Duchemin É, Canuel RE et al. Greenhouse gas emissions from reservoirs of the western United States. Global Biogeochemical Cycles, 2004, 18(3): 1-11. DOI:10.1029/2003GB002197 |
| [50] |
Wang F, Wang B, Liu CQ et al. Carbon dioxide emission from surface water in cascade reservoirs-river system on the Maotiao River, southwest of China. Atmospheric Environment, 2011, 45(45): 3827-3834. DOI:10.1016/j.atmosenv.2011.04.014 |
| [51] |
Yu YX, Liu CQ, Wang FS et al. Spatiotemporal characteristics and diffusion flux of partial pressure of dissolved carbon dioxide (pCO2) in Hongjiadu Reservoir. Chinese Journal of Ecology, 2008, 27(7): 1193-1199. [喻元秀, 刘丛强, 汪福顺等. 洪家渡水库溶解二氧化碳分压的时空分布特征及其扩散通量. 生态学杂志, 2008, 27(7): 1193-1199.] |
| [52] |
Barros N, Cole JJ, Tranvik LJ et al. Carbon emission from hydroelectric reservoirs linked to reservoir age and latitude. Nature Geoscience, 2011, 4(9): 593-596. DOI:10.1038/ngeo1211 |
 2018, Vol. 30
2018, Vol. 30 

