(2: 南昌大学资源环境与化工学院, 鄱阳湖环境与资源利用教育部重点实验室, 南昌 330047)
(2: Key Laboratory of Poyang Lake Environment and Resource Utilization, Ministry of Education, School of Resources Environmental & Chemical Engineering, Nanchang University, Nanchang 330047, P. R. China)
氮污染一直是水环境问题研究的热点,过量的氮输入引起湖泊富营养化、水生生物死亡和湖水不能利用等一系列水环境问题[1-2].湖泊氮的来源具有多样性,分为内源和外源,内源通常是湖泊内部水生生物碎屑和沉积物孔隙水释放等;外源则十分广泛,有大气干湿沉降、河流径流带来的土壤有机质、陆地植物碎屑、农业粪肥、生活污物和工业排污等[3].湖泊氮的循环转化过程也较复杂,主要为有机质矿化分解、无机氮的硝化与反硝化作用等生物地球化学过程.
碳氮稳定同位素技术可以较好地示踪湖泊氮的来源,并可大致作为判别氮的贡献和转化过程的理论依据[4-6].因为不同形态和来源的碳或氮具有相异的同位素值,并且在转化过程中具有同位素分馏效应.比如农业输入河流硝态氮同位素组成(-4 ‰ ~4 ‰)低于城市、工业污染河流硝态氮同位素值(10 ‰ ~25 ‰)[7].研究表明人为氮源的过量输入改变了水环境的性质,研究氮同位素组成(δ15N)的变化可以有效地示踪受人类活动及污水影响的水环境的过程和变化[5, 8-9].颗粒有机质氮的来源通常是利用碳氮稳定同位素结合碳氮比(δ13C、δ15N和C/N比)来判别[10],C/N比也作为有机质分解程度的指示剂,一般随分解程度的增加而减小[11],水体中无机氮的来源及转化可以利用铵态氮同位素(δ15NH4+)和硝态氮同位素(δ15NO3-)来示踪[12-13].
不同地域、时空变化和不同类型的水域应用同位素的方法研究氮来源的结果差异较大,具有重要的研究意义.例如,太湖东部氮污染的主要氮源为土壤有机氮、大气沉降及围网养殖[14];太湖北部氮污染的主要氮源为生活污水与粪便[15];太湖西部氮污染在枯水期的主要氮源为农业化肥,在丰水期主要为生活污水[16].鄱阳湖是长江中下游的重要湖泊之一,近些年来王毛兰等[17-19]应用同位素方法对鄱阳湖主干和入湖口河道的颗粒有机质进行了研究,表明不同湖水段,有机质氮含量和氮同位素组成有较大的时空差异,是受当地土地利用类型和污染类型不同所致,是氮污染物不同来源的有效指示.鄱阳湖也是一个过水性洪泛湖泊,在年内水位差异很大(8~12 m),丰水期的水面积往往是枯水期的十几倍以上(江西省水文局星子站水位),鄱阳湖的边缘湖区即是水位上涨扩散而成的水域(一般在5-9月),对于这种边缘类型湖泊氮的来源和转化过程研究较少.蚌湖即为鄱阳湖典型的边缘深水区,位于鄱阳湖两大支流(赣江北支和修河)入湖口附近,枯水期秋、冬季节是一个湿地,除了少量降雨外,几乎没有外来水源;丰水期夏季便是周边水域扩散而成且水面积大了几十倍的湖泊,水流相对缓慢,污染物来源广泛而复杂,相对较弱的水交换能力有利于营养元素和污染物的蓄积,易产生富营养化现象[20-21].本研究将利用稳定同位素示踪蚌湖在丰水期多种形式氮污染的来源,包括δ13C、δ15N结合C/N比示踪表层沉积物、水生植物和悬浮颗粒有机氮的来源;δ15NH4+和δ15NO3-示踪铵态氮和硝态氮的来源及可能发生的转化过程,为这种洪泛类型湖泊的氮污染治理提供科学依据.
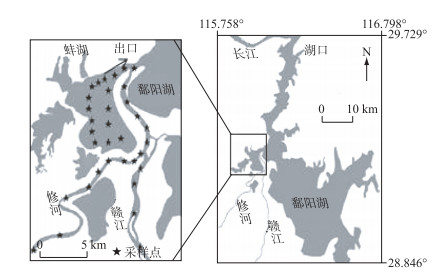
1 材料与方法 1.1 研究区域与样品采集蚌湖(29.268°~29.271°N, 115.934°~115.979°E)位于江西省星子县南部和吴城镇北面之间,起始于赣江北支与修河入鄱阳湖口附近,是鄱阳湖边缘的一个天然湖泊,面积约80 km2.蚌湖和其周边水域(赣江、修河入湖口以及鄱阳湖主体)之间存在一天然堤坝(图 1).丰水期周边水域越过堤坝进入蚌湖,实际上它们已成为一整体水域,呈现高水位一致性.
|
图 1 蚌湖及其周边水域采样点 Fig.1 Sampling sites in Lake Bang and the surrounding waters |
样品采集:2012年6月于水深5 m左右和7月于水深6 m左右的丰水期在蚌湖采集水样、表层沉积物和水生植物(浮叶植物:荇菜),同时采集周边河流—赣江和修河的入湖口处的水样,各样品的采集数量为10~20个,其中湖泊中乘船在同地点采集水样、表层沉积物和水生植物,采样量各20个左右;周边河流乘船采集水样量各10个.沿河还进行了岸边土壤、陆地植物、农业废水、养殖废水、雨水和城市污水等的采集,采样量2~5个,其中湿地采样是在枯水期4月进行. GPS定位,水样用5 L有机玻璃采水器采集表层0.5 m处的湖水,密封保存于干净聚乙烯瓶中,其中500 ml水样现场加入浓H2SO4使pH<2,供实验室分析总氮(TN)、总磷(TP)、铵态氮(NH4+-N)、硝态氮(NO3--N)和化学需氧量(CODCr). HCO3-现场滴定. 1.5 L水样用0.7 μm Waterman玻璃纤维滤膜(预先灼烧,去除氮)过滤,留在滤膜上的悬浮物(浓度用重量法)用于C、N含量、C/N比和同位素分析,水样用于无机氮同位素分析.表层沉积物和土壤样品利用自制采样器采集0~5 cm的样品,周边3次采样合并为1个样品,存放于聚乙烯自封袋中,于实验室冷冻干燥并磨碎过100目筛,供C、N含量、C/N比和同位素分析.陆地植物和水生植物样品经数次纯水洗涤去除泥沙和藻类,冷冻干燥并磨碎过100目筛,供C、N含量、C/N比和同位素分析.
1.2 样品分析水体理化分析:水温、pH、DO、Eh和叶绿素a(Chl.a)等由HACH水质参数分析仪和叶绿素仪现场测定. TN、TP、NH4+-N、NO3--N、HCO3-和CODCr浓度,分别采用过硫酸钾氧化紫外分光光度法、过硫酸钾氧化钼锑抗分光光度法、纳氏试剂分光光度法、酚二磺酸分光光度法、酸碱指示剂滴定法和重铬酸钾氧化滴定法进行测定[22].
同位素分析:水样无机氮同位素δ15NH4+、δ15NO3-分析之前进行预处理,取过滤好的1.5 L水样通过阴阳离子交换树脂Dowex1-x8、Dowex50w-x8分别富集NO3-、NH4+,之后用2 mol/L KCl洗脱再扩散,NO3-的洗脱液中加入定氮合金[23],最后干燥成粉末供连续流同位素质谱仪分析(CF-IRMS,Euro3000, Isoprine),以标定硫酸铵和IAEA硫酸铵分别为工作标准和国际标准,分析误差为±0.3 ‰.固体样品有机碳处理:加入0.5 mol/L的HCl酸化以去除无机碳,淋洗至中性,冷冻干燥.有机C、N含量和C/N比分析使用元素分析仪(VarioMacro,German).有机C、N同位素分析采用石英管灼烧法,加入CuO丝,N分析还需加入线状精Cu丝,在真空系统中抽真空后焊封,于马弗炉850℃灼烧5 h,然后纯化CO2或N2. N同位素以IAEA硝酸钾为国际标准,分析误差为±0.2 ‰;C同位素以美国南卡罗莱纳州白垩系Pee Dee组拟箭石化石(简称PDB)作为标准品,分析误差为±0.2 ‰.
| $ {{\rm{ \mathit{ δ} }}^{{\rm{15}}}}{\rm{N(或}}{{\rm{ \mathit{ δ} }}^{{\rm{13}}}}{\rm{C) = 1000 ‰ }}({R_{样品}}/{R_{标准}}-1) $ | (1) |
式中,R为15N/14N(或13C/12C)自然丰度比.
运用SPSS 19.0和Sigmaplot 12.0软件进行数据统计分析和作图.
2 结果与讨论 2.1 蚌湖及相邻水域水质特征鄱阳湖流域汛期是5-8月,蚌湖在6月和7月水深分别为5±0.3和6±0.3 m,是丰水期,水位的差异主要是因为7月比6月更多的大到暴雨以及7月长江汛期对鄱阳湖水位的顶托作用.湖水溶解氧浓度、弱碱性. 7月与6月相比,样品的化学参数有较大增加,NH4+-N浓度增加了0.3倍,TN、HCO3-和CODCr浓度均增加了1倍(表 1),NO3--N浓度几乎增加了2倍,反映了湖水有机质和无机氮的输入增加.蚌湖Chl.a浓度不高,说明藻类含量不高. TP浓度变化范围为0.04~0.12 mg/L.以CODCr、TN、TP和NH4+-N作为评价因子,按照模糊综合评价法的计算过程[24],蚌湖丰水期为Ⅳ类水质,处于中度富营养状态.蚌湖水质差的决定因素是TN浓度.评价因子对蚌湖水质影响的程度依次为TN>TP>NH4+-N>CODCr[20].蚌湖在丰水期悬浮颗粒物含量高,6月和7月均值分别为65.6和78.3 mg/L,从湖水外观也可以看出水体较为混浊.
| 表 1 蚌湖水体理化参数 Tab.1 The physical and chemical parameters of water in Lake Bang |
在水环境中,有机δ13C、δ15N结合C/N比可以有效地示踪有机质的来源,不同来源的碳氮同位素有各自的相对范围[25-26]. C3植物的有机δ13C为-32 ‰ ~-24 ‰,δ15N值为3 ‰ ~7 ‰;土壤有机质δ13C为-25 ‰ ~-22 ‰,δ15N值为0~5 ‰;C4植物δ13C为-17 ‰ ~-9 ‰;水体中水生植物δ13C为-31 ‰ ~-26 ‰,δ15N值为6 ‰ ~11 ‰;藻类的δ13C偏负,为-42 ‰ ~-24 ‰,均值为-30 ‰.陆源植物C/N比通常为15~30,藻类的降解产物含有较多的蛋白质,其C/N比一般小于7,水生植物C/N比介于陆源植物与藻类之间,为10~20,土壤有机质C/N比为8~15,同时有机质的降解也将改变C/N比[6, 27].
蚌湖周边陆地C3植物的δ13C较负,均值小于-27.9 ‰,δ15N均值大于7 ‰ [28],C4植物的δ13C均值为-17.4 ‰ ±1.0 ‰;土壤有机质δ13C比C3植物偏正,均值大于-25.2 ‰,δ15N最低,均值范围为3.2 ‰ ~3.7 ‰;沉积物的δ13C值介于C3植物和土壤有机质之间,δ15N范围为5 ‰ ~7 ‰.陆地植物的C/N比最大,大于17,土壤有机质的C/N比均值大于12(蚌湖堤坝土壤C/N比小于10,实际上在丰水期被水淹),沉积物的C/N比均值在10左右(表 2).这些不同来源的δ13C、δ15N及C/N比差异较大,较好区分.
| 表 2 蚌湖和周边河流有机质碳、氮稳定同位素特征值 Tab.2 Carbon and nitrogen stable isotopes of organic matter in Lake Bang and the surrounding rivers |
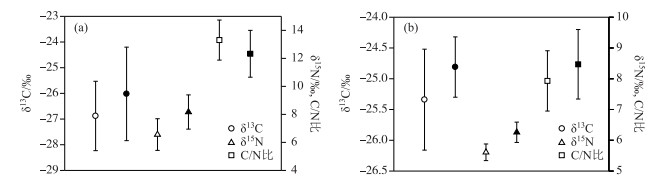
水生植物δ13C在6月范围为-28.8 ‰ ~-24.9 ‰,均值为-26.8 ‰ ±1.3 ‰,7月范围为-29.3 ‰ ~-23.2 ‰,均值为-26.0 ‰ ±1.8 ‰ (图 2a).采集的水生植物是浮叶植物,6月和7月是夏季,有较高的温度和强烈的光照,δ13C主要影响因素是光合作用和呼吸作用,与水体的无机碳含量关系不大,故δ13C差别较小. δ15N在6月范围为5.3 ‰ ~8.2 ‰,均值为6.6 ‰ ±1.1 ‰,7月范围为7.4 ‰ ~11.0 ‰,均值为8.8 ‰ ±1.1 ‰,比6月偏正2.2 ‰.水生植物氮的主要来源是叶片和根系从水体和底泥中吸收无机氮,无机氮δ15N的变化会使有机质的δ15N值存在明显差异,水生植物的δ15N可以作为人为氮输入影响的指标[29]. 7月水生植物δ15N的明显升高说明吸收了δ15N值更高的无机氮,比如废水无机氮. C/N比在6月为9.9~16.7,均值为13.5±1.3;7月为8.8~14.9,均值为12.6±1.5,比6月略有降低.
|
图 2 水生植物(a)和表层沉积物(b)的δ13C、δ15N和C/N比分布(白色和黑色图例分别表示6月和7月样品) Fig.2 Distributions of δ13C, δ15N and C/N of aquatic plant (a) and surface sediment (b) |
蚌湖表层沉积物δ13C在6月范围为-26.5 ‰ ~-24.4 ‰,均值为-25.3 ‰ ±0.8 ‰;7月范围为-25.7 ‰ ~-24.3 ‰,均值为-24.8 ‰ ±0.5 ‰,比6月略偏正(图 2b). δ15N在6月范围为5.2 ‰ ~6.2 ‰,均值为5.6 ‰ ±0.3 ‰;7月范围为5.7 ‰ ~6.8 ‰,均值为6.3 ‰ ±0.3 ‰,比6月偏正0.7 ‰. C/N比在6月为6.2~9.1,均值为7.9±1.0;7月为7.3~10.3,均值为8.4±1.1,比6月略偏高,整体来说沉积物的δ13C、δ15N和C/N比在7月比6月略偏高.沉积物的δ13C落在水生植物和土壤有机质的δ13C之间(表 2,图 2a),与藻类的δ13C(-30 ‰)相差较大;沉积物的δ15N比土壤有机质的偏高2.5 ‰ ~3.2 ‰,而比水生植物的偏低1 ‰ ~2.5 ‰;沉积物的C/N比水生植物和土壤有机质的都低于4以上,但是沉积物的C/N比都大于7(一般藻类小于7).沉积物在成岩过程中伴随着矿化降解,矿化作用的同位素分馏较小[30],但矿化降解降低了C/N比值[11].藻类对表层沉积物的贡献较弱.
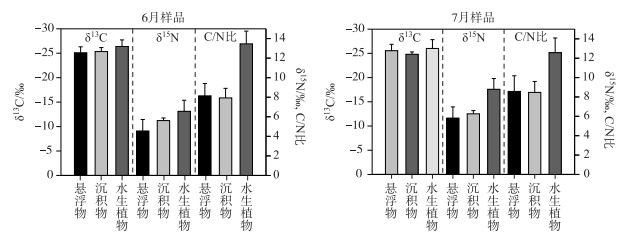
2.2.3 蚌湖悬浮颗粒物、表层沉积物和水生植物的关系蚌湖的悬浮颗粒物、表层沉积物和水生植物的δ13C差别不大(图 3),悬浮颗粒物的δ15N(4 ‰ ~6 ‰)比表层沉积物和水生植物的δ15N都低,归因于土壤有机质参与其组成(表 2),悬浮颗粒物比沉积物的C/N比稍高,但比水生植物低较多,可能是因为悬浮颗粒物往往是由降解的碎屑组成.
|
图 3 悬浮物与表层沉积物、水生植物的碳氮同位素关系 Fig.3 The relations of suspend particle matter and the carbon and nitrogen stable isotopes of surface sediment and aquatic plant |
蚌湖丰水期水深有4.8~6.5 m,风浪的作用使表层沉积物悬浮作用不大,所以悬浮物的组成中沉积物的悬浮较小,沉积物的组成则是悬浮颗粒物携带的土壤有机质和水生植物经过矿化改造的混合沉降.
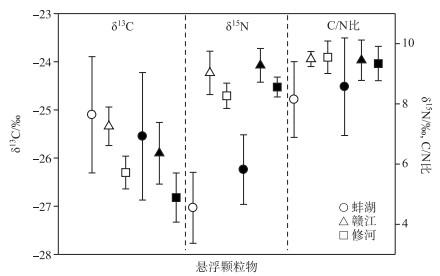
2.2.4 蚌湖及周边河流中悬浮颗粒物的同位素特征及其来源悬浮颗粒物在蚌湖6月的δ13C范围为-26.7 ‰ ~-23.7 ‰,平均值为-25.1 ‰ ±1.2 ‰ (图 4),7月δ13C范围为-27.6 ‰ ~-23.2 ‰,均值为-25.5 ‰ ±1.3 ‰,比6月略偏负;赣江6月的δ13C范围为-26.3 ‰ ~-24.3 ‰,均值为-25.3 ‰ ±0.4 ‰,7月范围为-26.8 ‰ ~ -24.8 ‰,均值为-25.9 ‰ ±0.7 ‰,比6月略偏负,赣江与蚌湖的δ13C差别不大;修河6月的δ13C范围为-27.23 ‰ ~-25.72 ‰,均值为-26.32 ‰ ±0.35 ‰,7月范围为-27.47 ‰ ~-26.31 ‰,均值为-26.82 ‰ ±0.51 ‰,比6月略偏负,修河比赣江和蚌湖的δ13C均偏负0.8 ‰ ~1.7 ‰,可能有更多的陆地植物碎屑进入修河.蚌湖悬浮颗粒物δ13C值均介于土壤有机质和水生植物碎屑之间,比陆地植物偏正(大约3 ‰),表明其来源主要是土壤有机质和水生植物的混合(表 2).赣江和修河的悬浮颗粒物δ13C介于土壤有机质和陆地植物的δ13C之间. δ13C在7月比6月偏负,表明7月有更多的陆源物质输入.
|
图 4 蚌湖及周边河流悬浮颗粒物的δ13C、δ15N和C/N比分布(白色和黑色图例分别表示6月和7月样品) Fig.4 Distributions of δ13C, δ15N and C/N of suspend particle matter in Lake Bang and the surrounding rivers |
悬浮颗粒物在蚌湖6月δ15N的范围为2.6 ‰ ~6.2 ‰,均值为4.1 ‰ ±1.2 ‰,7月的范围为4.3 ‰ ~7.7 ‰, 均值为5.8 ‰ ±1.2 ‰,7月比6月偏正1.7 ‰,但均值都小于7 ‰,大于3.5 ‰,表现为土壤有机质和水生植物的混合特征(表 2, 图 2a);赣江6月的范围为5.34 ‰ ~10.32 ‰,均值为9.03 ‰ ±0.72 ‰,7月为9.3 ‰ ±0.6 ‰,比6月略偏正,赣江悬浮颗粒物的δ15N比土壤有机质的高5 ‰以上,也比陆地植物的δ15N高(7.43 ‰ ±3.01 ‰,表 2),结合δ13C,表明赣江有更高δ15N的废水有机质(7 ‰ ~25 ‰)输入;修河6月为8.3 ‰ ±0.4 ‰,7月为8.5 ‰ ±0.3 ‰,比6月略偏正,修河的δ15N比土壤有机质(3.79 ‰ ±0.37 ‰)高较多,比陆地植物(9.39 ‰ ±0.95 ‰)略低(表 2),表明修河的悬浮颗粒有机质中陆地植物碎屑的贡献较大,不能排除废水有机质输入的可能.赣江和修河的δ15N比蚌湖高4 ‰ ~5 ‰,表明蚌湖的悬浮颗粒有机质的来源不仅有河流的运输,更多地来自于土壤有机质和水生植物的混合,因为丰水期大到暴雨冲刷陆地带来周边更多的土壤有机质输入蚌湖.蚌湖与河流的悬浮颗粒有机质δ15N的较大差别,从另一方面反映蚌湖与河流的水交换在丰水期不彻底,蚌湖水源主要是滞留的河水与湖面降雨的混合,后面无机氮的来源也将说明这一点.
蚌湖悬浮颗粒物C/N比在6月范围为6.2~9.2(均值为8.2±1.3),7月范围为5.7~11.9(均值为8.6±1.6);赣江的悬浮颗粒物C/N比在6月为9.5±0.3,7月为9.5±0.7;修河的悬浮颗粒物C/N比在6月为9.5±0.5,7月为9.3±0.6.湖泊和河流的悬浮颗粒物的C/N比低于水生植物和土壤有机质的C/N比(均值>12)(图 1, 图 3, 表 2),一方面是由于悬浮颗粒物组成往往是衰败的植物碎屑,在夏季水环境中较强的矿化、生物降解作用降低了C/N比.另一方面不能排除大雨冲刷陆地带来的低C/N比的废水有机质输入的可能(如城镇污物、动物粪肥的C/N比范围6~13[3]).
悬浮颗粒物的δ13C、δ15N结合C/N比示踪湖泊和河流的有机质的来源,表明蚌湖的悬浮颗粒物主要来源于土壤有机质和水生植物的混合.赣江和修河的悬浮颗粒物主要来源于土壤有机质和陆地植物碎屑,并且废水有机质有一定贡献.藻类对湖泊和河流悬浮颗粒有机质的贡献较小.
2.3 无机氮同位素特征及转化过程不同来源的无机氮组成有不同的δ15N特征值,合成化肥大约为0±2 ‰ [31], 其中NO3-肥的δ15N值一般在-2.5 ‰ ~2.0 ‰之间,NH4+肥的δ15N值一般在-4 ‰ ~2 ‰之间;动物废水δ15N范围为8 ‰ ~20 ‰ [32],雨水中NH4+的δ15N范围为-30 ‰ ~0,NO3-的δ15N范围为-10 ‰ ~2 ‰ [33].无机氮同位素被广泛应用于水环境中氮的来源与转化研究[34-37].我国不同地区地表水、地下水和雨水的无机氮δ15N现有数据不同,对于研究区域水体中氮的来源和氮循环转化具有重要的意义[8, 38-39].
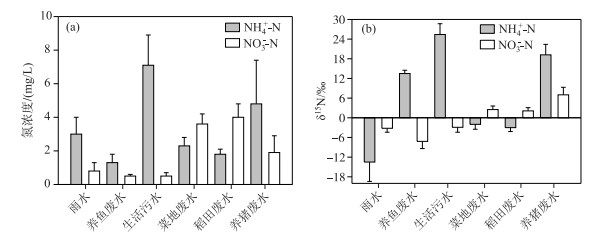
本研究中雨水、养鱼废水、养猪废水和城镇生活废水中无机氮都是以铵态氮为主,只有农田、蔬菜地以硝态氮为主(图 5a).雨水中的铵态氮同位素值最负(-13.5 ‰ ±5.9 ‰)(图 5b),养鱼和养猪废水和城镇废水的铵态氮同位素值较正(大于12 ‰),而硝态氮同位素以养鱼废水为最负(-7.2 ‰ ±2.2 ‰),养猪废水为最正(7.0 ‰ ±2.3 ‰),这些氮同位素值差异较大,容易区分.雨水、城镇废水、农业蔬菜地和化肥的硝态氮同位素值差别不大.农业蔬菜地和稻田废水的铵态氮同位素值也表现为化肥的氮同位素值,表明农业种植地的氮来源以化肥为主.
|
图 5 沿河流域废水中铵态氮和硝态氮浓度(a)以及同位素特征值(b) Fig.5 Concentrations (a) and isotopes(b) of ammonia-N and nitrate-N of waste water along rivers |
蚌湖从6-7月无机氮主要形式从铵态氮转变为硝酸盐氮,表明暴雨的冲涮带来了更多面源污染的农业化肥输入,实际上此时也是农田第二季水稻种植的时期.
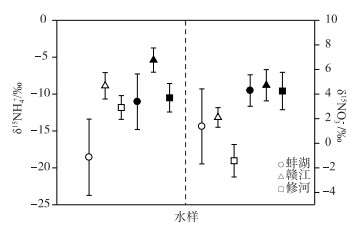
蚌湖的δ15NH4+在6月最负(-18.6 ‰ ±5.2 ‰),表现为雨水铵态氮同位素特征,以雨水输入为主,在7月则显著升高(-12.2 ‰ ±3.2 ‰),增加了6 ‰ (图 6).蚌湖的相邻水域赣江和修河在6月的δ15NH4+也为负值(分别为-8.9 ‰ ±1.8 ‰和-11.8 ‰ ±1.6 ‰),表现为以雨水输入为主,在7月也升高了2.6 ‰和1.3 ‰ (分别为-5.4 ‰ ±1.64 ‰和-10.5 ‰ ±1.4 ‰).蚌湖的δ15NH4+比赣江和修河的均值偏负7 ‰ ~10 ‰,蚌湖的湖面降雨量更明显,也表明蚌湖与河流的水量交换不彻底,蚌湖水源可能主要为滞留的河水和湖面降雨.
|
图 6 蚌湖及周边河流δ15NH4+和δ15NO3-分布特征(白色和黑色图例分别表示6月和7月水样) Fig.6 Distribution of δ15NH4+ and δ15NO3- in Lake Bang and the surrounding rivers |
蚌湖的δ15NO3-在6月变化范围较宽,为-5.5 ‰ ~5.8 ‰,均值1.4 ‰ ±3.0 ‰,表现为雨水和农业化肥混合输入特征;7月范围为-1.7 ‰ ~5.9 ‰,均值升高到4.3 ‰ ±1.3 ‰,表现为农业化肥输入为主,可能还有高同位素值的废水输入.赣江和修河的δ15NO3-在6月分别为2.2 ‰ ±0.8 ‰和-1.4 ‰ ±1.3 ‰,表现为农业化肥和雨水输入特征,7月有明显的升高, 分别为4.7 ‰ ±1.3 ‰和4.2 ‰ ±1.6 ‰,表现为农业化肥输入为主,可能还有高同位素值的废水输入.
无机氮在水体迁移转化过程中发生的硝化作用、反硝化作用和同化作用等过程会引起氮同位素分馏[13, 40].硝化作用使剩余的δ15NH4+升高,NH4+-N浓度降低,且δ15NO3-降低(轻同位素首先参与转化);反硝化作用使δ15NO3-升高,而NO3--N浓度降低,这些浓度与同位素的关系常用来示踪水体氮的转化过程[41],或判别来自动物粪便或污水的氮污染[42],比如Mariotti等[43]示踪地下水氮的稀释作用在δ15NO3-与1/NO3-关系图上为一直线,而反硝化作用在δ15NO3-与ln[NO3-]关系图上为一直线.吴庆乐等[16]在太湖西部湖区分析氮污染转化过程中发现,无机氮浓度与同位素值存在相反关系,认为发生了较为显著的硝化作用.蚌湖从6月到7月δ15NH4+大幅增加了6 ‰,δ15NO3-均值也增加3 ‰,NH4+-N和NO3--N浓度也分别增加了0.3和2倍,统计结果表明蚌湖的δ15NH4+与δ15NO3-不存在相反关系,浓度与同位素值直线关系也弱(R2=0.1124或0.1949).蚌湖是浅水湖泊,夏季温度高,溶解氧丰富,水体容易发生矿化作用和硝化作用,不容易发生反硝化作用.大幅增加的无机氮同位素值和浓度表明蚌湖存在较高δ15N的外源废水氮输入(图 5a,b).在赣江近蚌湖100 km处有南昌市大城市存在,修河近蚌湖10 km处有永修县县城分布,而且鄱阳湖流域是农业河流,前些年沿河和蚌湖沿岸有不少分散的养猪养牛场分布.丰水期经常性的暴雨冲刷陆地容易将畜禽粪肥输入水域,严重增加了水体的氮污染. 7月采样的时间即是在暴雨过后的第3天.丰水期蚌湖与鄱阳湖水位保持一致,同时长江在7月也是汛期,鄱阳湖水受长江来水的顶托作用不能下泄,故蚌湖水流缓慢,污染物容易蓄积在湖内.
从以上分析无机氮同位素值和浓度的变化可知,丰水期蚌湖的无机氮主要来自于雨水和农业化肥,暴雨的冲涮会带来城镇生活废水和畜禽养殖废水的威胁.
3 结论利用碳氮同位素结合碳氮比示踪丰水期蚌湖有机质氮和无机氮的来源,蚌湖悬浮颗粒有机质以土壤有机质和水生植物碎屑的混合为主.水生植物是蚌湖重要的内源氮来源,其δ15N值主要受到无机氮δ15N的影响,暴雨冲涮带来的高δ15N废水明显提高了水生植物的δ15N值.藻类对有机质的贡献较弱.蚌湖的无机氮主要来源于雨水和农业化肥,暴雨的冲涮作用也带来了城镇生活废水和畜禽养殖废水的威胁.蚌湖和鄱阳湖一样是洪泛湖泊,本研究有利于对这种类型湖泊的营养输入和控制污染的管理提供科学依据,更期望于加强长江中下游洪泛类型湖泊的氮循环和迁移转化研究.
| [1] |
Camargo JA, Alonso A. Ecological and toxicological effects of inorganic nitrogen pollution in aquatic ecosystems:A global assessmen. Environment International, 2006, 32(6): 831-849. DOI:10.1016/j.envint.2006.05.002 |
| [2] |
Shan BQ, Jian YX, Tang WZ et al. Temporal and spatial variation of nitrogen and phosphorus and eutrophication assessment in downstream river network areas of North Canal River Watershed. Environmental Science, 2012, 33(2): 352-358. [单保庆, 菅宇翔, 唐文忠等. 北运河下游典型河网区水体中氮磷分布与富营养化评价. 环境科学, 2012, 33(2): 352-358.] |
| [3] |
Guo QJ, Wang CY, Zhu GX et al. Research on the source and migration process of organic matter of lake sediments using nitrogen isotope-A case study in Beijing. Bulletin of Mineralogy, Petrology and Geochemistry, 2015, 34(3): 532-538. [郭庆军, 王春雨, 朱光旭. 氮同位素研究城市湖泊沉积物有机质来源和迁移过程——以北京为例. 矿物岩石地球化学通报, 2015, 34(3): 532-538.] |
| [4] |
Kelley CJ, Keller CK, Evans RD et al. Nitrate-nitrogen and oxygen isotope ratios for identification of nitrate sources and dominant nitrogen cycle processes in a tile-drained dryland agricultural field. Soil Biology and Biochemistry, 2013, 57: 731-738. DOI:10.1016/j.soilbio.2012.10.017 |
| [5] |
Hadas O, Altabet MA, Agnihotri R. Seasonally varying nitrogen isotope biogeochemistry of particulate organic matter in Lake Kinneret, Israel. Limnology and Oceanography, 2009, 54: 75-85. DOI:10.4319/lo.2009.54.1.0075 |
| [6] |
Kendall C, Silva SR, Kelly VJ. Carbon and nitrogen isotopic compositions of Particulate organic matter in four large river systems across the United States. Hydrology Process, 2001, 15: 1301-1346. DOI:10.1002/(ISSN)1099-1085 |
| [7] |
Xiao HY, Liu CQ. Nitrogen isotope studies on seasonal nitrogen pollution of inflowing rivers of Hongfeng Lake, Guizhou Province. Earth and Environment, 2004, 32(1): 71-75. [肖化云, 刘丛强. 氮同位素示踪贵州红枫湖河流季节性氮污染. 地球与环境, 2004, 32(1): 71-75.] |
| [8] |
Lin L, Wu JL, Zeng HA et al. Stable nitrogen isotope tracing anthropogenic influence on Lake Taihu. J Lake Sci, 2012, 24(4): 546-552. [林琳, 吴敬禄, 曾海鳌等. 人类活动对太湖水环境影响的氮同位素示踪. 湖泊科学, 2012, 24(4): 546-552. DOI:10.18307/2012.0407] |
| [9] |
Xiao HY, Liu CQ. Composition of nitrogen isotope in recent sediment of Hongfeng Lake indicating waste water condition, Guizhou. Chinese Science Bulletin, 2006, 51(9): 1091-1096. [肖化云, 刘丛强. 贵州红枫湖现代沉积物氮同位素组成反映的废水输入状况. 科学通报, 2006, 51(9): 1091-1096.] |
| [10] |
Besemer K, Luef B, Preiner S et al. Sources and composition of organic matter for bacterial growth in a large European river ffloodplain system (Danube, Austria). Org Geochem, 2009, 40: 321-331. DOI:10.1016/j.orggeochem.2008.12.005 |
| [11] |
Liu CQ, Lang YC, Li SL et al. Researches on biogeochemical processes and nutrient cycling in karstic ecological systems, southwest China:A review. Earth Science Frontiers, 2009, 16(6): 1-12. [刘丛强, 郎赟超, 李思亮等. 喀斯特生态系统生物地球化学过程与物质循环研究:重要性、现状与趋势. 地学前缘, 2009, 16(6): 1-12.] |
| [12] |
Xing M, Liu WG, Hu J. Using nitrate isotope to trace the nitrogen pollution in Chanhe and Laohe River. Environmental Science, 2010, 10(10): 2305-2310. [邢萌, 刘卫国, 胡婧. 浐河、涝河河水硝酸盐氮污染来源的氮同位素示踪. 环境科学, 2010, 10(10): 2305-2310.] |
| [13] |
Xue D, Botte J, Baets BD et al. Present limitations and future prospects of stable isotope methods for nitrate source identification in surface and groundwater. Water Research, 2009, 43: 1159-1170. DOI:10.1016/j.watres.2008.12.048 |
| [14] |
Xing GX, Cao YC, Shi SL et al. N pollution sources and denitrification in waterbodies in Taihu Lake region. Science in China Series B:Chemistry, 2001, 44(3): 304-314. DOI:10.1007/BF02879621 |
| [15] |
Chen ZX, Yu L, Liu WG et al. Nitrogen and oxygen isotopic compositions of water-soluble nitrate in Taihu Lake water system, China:implication for nitrate sources and biogeochemical process. Environmental Earth Sciences, 2013, 71(1): 217-223. |
| [16] |
Wu QL, Ruan XH, Wu CM et al. Analyses of sources and transformation of nitrogen as a contaminant in the river and lake water in the western region of the Taihu Lake basin. Acta Scientiae Circumstantiae, 2015, 35(12): 3883-3889. [吴庆乐, 阮晓红, 吴朝明等. 太湖西部河湖氮污染物来源及转化途径分析. 环境科学学报, 2015, 35(12): 3883-3889.] |
| [17] |
Wang ML, Lai JP, Hu KT et al. Compositions and sources of stable organic carbon and nitrogen isotopes in surface sediments of Poyang Lake. China Environmental Science, 2014, 34(4): 1019-1025. [王毛兰, 赖建平, 胡珂图等. 鄱阳湖表层沉积物有机碳、氮同位素特征及其来源分析. 中国环境科学, 2014, 34(4): 1019-1025.] |
| [18] |
Wang ML, Lai JP, Hu KT et al. Compositions of stable organic carbon and nitrogen isotopes in wetland soil of Poyang Lake and its environmental implications. China Environmental Science, 2016, 36(2): 500-505. [王毛兰, 赖建平, 胡珂图等. 鄱阳湖湿地土壤有机碳氮同位素特征及其环境意义. 中国环境科学, 2016, 36(2): 500-505.] |
| [19] |
Wang ML, Zhang DL, Lai JP et al. Distribution and sources of stable organic carbon and nitrogen isotopes in suspended particulate organic matter of Poyang Lake. China Environmental Science, 2014, 34(9): 2342-2350. [王毛兰, 张丁苓, 赖建平等. 鄱阳湖水体悬浮有机质碳氮同位素分布特征及来源探讨. 中国环境科学, 2014, 34(9): 2342-2350.] |
| [20] |
Liang Y, Xiao H, Liu X et al. Spatial and temporal water quality characteristics of Poyang Lake Migratory Bird Sanctuary in China. Chinese of Journal Geochemistry, 2015, 34(1): 34-48. |
| [21] |
Hu CH, Huang D, Zhou WB et al. Study on Trophic status and influencing factors of typical lake fringe area in wet seasonA case study of Banghu Lake. Journal of Hydroecology, 2013, 34(3): 32-38. [胡春华, 黄丹, 周文斌等. 典型湖泊边缘区丰水期营养状态及其影响因子研究——以蚌湖为例. 水生态学杂志, 2013, 34(3): 32-38.] |
| [22] |
Ministry of Environmental Protection of the People's Republic of China, Editorial Board of Water and Wastewater Monitoring and Analysis Methods ed. Water and wastewater monitoring and analysis methods: 4th edition. Beijing: China Environmental Science Press, 2002. [国家环境保护总局《水和废水监测分析方法》编委会. 水和废水监测分析方法: 第4版. 北京: 中国环境科学出版社, 2002. ]
|
| [23] |
Xiao HY, Liu CQ. Sources of nitrogen and sulfur in wet deposition at Guiyang, southwest China. Atmospheris Environment, 2002, 36: 5121-5130. DOI:10.1016/S1352-2310(02)00649-0 |
| [24] |
Wu HY, Chen KL, Chen ZH et al. Evaluation for the ecological quality status of coastal waters in East China Sea using fuzzy integrated assessment method. Mar Pollut Bull, 2012, 64: 546-555. DOI:10.1016/j.marpolbul.2011.12.022 |
| [25] |
Xiao HY, Liu CQ. Identifying organic matter provenance in sediments using isotopic ratios in an urban river. Geochemical Journal, 2010, 44: 181-187. DOI:10.2343/geochemj.1.0059 |
| [26] |
Sigleo AC, Macko SA. Carbon and nitrogen isotopes in suspended particles and colloids, Chesapeake and San Francisco estuaries, USA. Estuarine. Coastal and Shelf Science, 2002, 54: 701-711. DOI:10.1006/ecss.2001.0853 |
| [27] |
Goni MA, Teixeira MJ, Perkey DW. Sources and distribution of organic matter in a river dominated estuary (Winyah Bay, SC, USA). Estuarine, Coastal and Shelf Science, 2003, 57: 1023-1048. DOI:10.1016/S0272-7714(03)00008-8 |
| [28] |
Liang Y, Liu XZ, Xiao HY et al. Impact of high water level fluctuations on stable isotopic signature of POM and source identification in a floodplain lake-Bang Lake (Poyang Lake). Environmental Earth Sciences, 2016, 75(3): 1-12. |
| [29] |
Liu YL, Yu H, Xu J et al. Stable nitrogen isotope in aquatic macrophytes as an indicator of anthropogenic nitrogen inputs to Lake Taihu. J Lake Sci, 2015, 27(2): 243-249. [刘勇丽, 余辉, 徐军等. 利用水生植物氮同位素作为人为氮输入太湖的生物指标. 湖泊科学, 2015, 27(2): 243-249. DOI:10.18307/2015.0207] |
| [30] |
Kendall C, Silva SR, Kelly VJ. Carbon and nitrogen isotopic compositions of particulate organic matter in four large river systems across the United States. Hydrological Processes, 2001, 15: 1301-1346. DOI:10.1002/(ISSN)1099-1085 |
| [31] |
Marion GS, Dunbar RB, Mucciarone DA et al. Coral skeletal δ15N reveals isotopic traces of an agricultural revolution. Marine Pollution Bulletin, 2005, 50: 931-944. DOI:10.1016/j.marpolbul.2005.04.001 |
| [32] |
Xie YX, Xiong ZQ, Xing GX et al. Assessment of nitrogen pollutant sources in surface waters of Taihu Lake region. Pedosphere, 2007, 17: 200-208. DOI:10.1016/S1002-0160(07)60026-5 |
| [33] |
Zhao LJ, Yin L, Xiao HL et al. Isotopic evidence for the moisture origin and composition of surface runoff in the headwaters of the Heihe River basin. Chinese Science Bulletin, 2011, 56(4/5): 406-415. |
| [34] |
Yoshikawa C, Abe H, Aita MN et al. Insight into nitrous oxide production processes in the western North Pacific based on a marine ecosystem isotopomer model. Journal of Oceanography, 2016, 72(3): 491-508. DOI:10.1007/s10872-015-0308-2 |
| [35] |
Chang CCY, McCormick PV, Newman S et al. Isotopic indicators of environmental change in a subtropical wetland. Ecological Indicators, 2009, 5: 825-836. |
| [36] |
Li S, Liu C, Li J et al. Assessment of the sources of nitrate in the Changjiang River, China using a nitrogen and oxygen isotopic approach. Environmental Science and Technology, 2010, 44: 1573-1578. DOI:10.1021/es902670n |
| [37] |
Kendall C. Tracing sources and cycling of nitrate in catchments. In: Kendall C, Mcdonnell J eds. Isotope tracers in catchment hydrology. Amsterdam: Elsevier, 1998: 519-576.
|
| [38] |
Fan LJ, Zhao FH, Cheng C. Research advances in stable nitrogen isotope in water bodies. Chinese Journal of Applied Ecology, 2016, 27(8): 2699-2707. [范丽俊, 赵峰华, 程晨. 水体中氮稳定同位素的研究进展. 应用生态学报, 2016, 27(8): 2699-2707.] |
| [39] |
Li SL, Liu CQ, Xiao HY et al. Using δ15N to assess groundwater nitrogen pollution in Guiyang. Geochimica, 2005, 34(3): 257-262. [李思亮, 刘丛强, 肖化云等. δ15N在贵阳地下水氮污染来源和转化过程中的辨识应用. 地球化学, 2005, 34(3): 257-262.] |
| [40] |
Heaton T. Isotopic studies of nitrogen pollution in the hydrosphere and atmosphere:A review. Chemical Geology:Isotope Geoscience Section, 1986, 59: 87-102. DOI:10.1016/0168-9622(86)90059-X |
| [41] |
Deutsch B, Voss M, Fischer H. Nitrogen transformation processes in the Elbe River:Distinguishing between assimilation and denitrification by means of stable isotope ratios in nitrate. Aquat Sci, 2009, 71(2): 228-237. DOI:10.1007/s00027-009-9147-9 |
| [42] |
Zhang CY, Zhang S, Li ZH et al. Nitrogen isotope discrimination the source of nitrate pollution of underground water in Shijiazhuang City. Advances in Earth Sciences, 2004, 19(2): 183-191. [张翠云, 张胜, 李政红等. 用氮同位素技术判别石家庄市地下水硝酸盐污染的来源. 地球科学进展, 2004, 19(2): 183-191.] |
| [43] |
Mariotti A, Landreau A, Simon B. 15N isotope biogeochemistry and natural denitrification process in groundwater:Application to the chalk aquifer of northern France. Geochimica et Cosmochimica Acta, 1988, 52: 1869-1878. DOI:10.1016/0016-7037(88)90010-5 |
 2018, Vol. 30
2018, Vol. 30 


