(2: 江西省环境保护科学研究院, 南昌 330039)
(3: 江西省环境保护工程技术研究中心, 南昌 330039)
(2: Jiangxi Academy of Environmental Sciences, Nanchang 330039, P. R. China)
(3: Environmental Pollution Engineering Center of Jiangxi, Nanchang 330039, P. R. China)
目前,浅水湖泊富营养化及其水华已成为突出的全球性生态学问题,在国内外有关富营养化水体中沉水植物衰退乃至消失的报道日趋普遍[1-8].由于我国湖泊富营养化进程的加快,沉水植物等水生植物栖息生境片断化加剧,其种群数量渐趋于临近值甚至接近零,原有广布种逐渐变为稀有种[6-12],湖泊也由早期以沉水植被占优势的草型—清水稳态向当前以小型化浮游植物占优势的藻型—浊水稳态逆行演替(如武汉东湖、太湖、滇池等湖泊)[6-7, 10, 13].大型沉水植物作为湖泊重要功能群,生态作用突出[1, 6-8, 10-14],其大面积退化则带来了一系列的次生环境问题,如水质急剧恶化、顽固性蓝藻水华暴发和水生生物食物网深度破裂,直接影响到湖泊生态服务功能乃至区域环境健康[1, 6-8, 10-14].为恢复我国湖泊生态系统的功能与健康,揭示湖泊沉水植物退化的深层驱动机制是摆在我国湖沼学者面前的重要科学问题.
富营养化湖泊中沉水植物类群“消失”之谜存在多种理论学说.理论一:高营养负荷所带来的水下低光被认为是富营养化湖泊中的基本特征,已有研究证实这些特征影响着沉水植物的生长与代谢、种群繁殖与结构分布.低光能减弱沉水植物的抗逆境与抗胁迫能力,并进一步导致水生生态系统尤其是沉水植物的衰退,主要表现为:植物生长速率降低、光合作用减弱、植物组织含氮量增加和碳源性次生产物产量下降[15-23].理论二:富营养化湖泊中高铵是导致沉水植物衰退的重要机制. Cao等[2, 13, 17-19, 21-38]也曾开展一系列的水生植物铵胁迫生理学的研究,发现高铵会强烈抑制植物的生长,对其抗氧化系统产生强烈的攻击并使得植物组织内抗氧化酶系统被激活、出现ROS(reactive oxygen species)氧化胁迫以及C-N代谢失衡紊乱.其他可能的机制,如低氧可对其他环境胁迫因子所造成的生理胁迫及毒害产生促进作用,从而对植物的生长、代谢与存活构成不利影响,相关研究有待深入[13, 23, 35, 37, 39]. Morris等[23]通过野外试验和温室室内模拟试验发现美洲苦草(Vallisneria americana)在城市湖泊中的大面积衰退主要归因于水体中低氧及水下低光的综合作用.以往研究注重高铵、低光与低氧等单因子或两因子胁迫作用,对于这3种主要胁迫因子的综合作用的模拟实验研究仍未见报道.在富营养化背景下,这些因子的协同作用对沉水植物生长与C-N代谢的致胁迫和植被的致退化机制值得深入研究.
本研究重点探索3种重要的环境胁迫因子低氧、高铵与低光对沉水植物世界广布种苦草(Vallisneria natans)生长与代谢的综合胁迫影响规律,探究影响苦草生长与代谢的主效因子及其胁迫影响特征,探讨苦草在综合胁迫下影响生长与代谢的敏感指标及其贡献程度,为富营养化湖泊沉水植被的恢复与重建提供理论依据.
1 材料与方法 1.1 实验材料苦草(V. natans)属于水鳖科苦草属,世界广布种,遍布于我国长江中下游淡水湖库,是长江中下游淡水水域优势水生植物之一,作为一种基生叶、莲座型沉水植物,其光需求量一般较低、繁殖速度较快、生态幅度较广、营养盐及重金属吸收能力较强、鱼类适口性较好和耐受水深较高(洱海发现水深10 m区域有分布)等特点,常被用于富营养化水体的生态修复[2, 20-23, 30-31, 33-34, 38-39].
本研究的苦草收集于鄱阳湖国家级自然保护区、抚河下游支流的滨河湿地和南昌玉带河上游,混合预培养于装有自来水(总氮(TN): 0.45 mg/L;铵态氮(NH4+-N):未检出;总磷(TP): 0.01 mg/L)和石英砂培养的塑料箱中,预培养12个月.挑选生长良好,长势一致的植株作为实验材料.
1.2 实验设计本实验选择在江西省环境保护科学研究院半室外试验区进行,设计系统如图 1所示,实验时间为7月中旬8月中旬,光为自然光.正交试验设计因试验次数少,适合多因子综合效应的分析研究,在化工、食品、医药和农林等领域应用广泛,本研究拟采用正交试验设计进行.根据已有的实验研究[22-23, 30, 33, 35]及野外监测数据对环境因子进行参数设置,采用L16(45)的正交试验设计,实验包括4个低光照强度(50 %、40 %、30 %和20 %自然光照分别用L1、L2、L3和L4表示)和4个铵态氮浓度水平(0.5、1、2和4 mg/L分别用N1、N2、N3和N4表示)以及4个低氧处理浓度(7.5、6.5、5.5和4 mg/L分别用O1、O2、O3和O4表示),共16个组合的无交互正交设计方案.正交实验表设计与方案分别见表 1和表 2.

|
图 1 复合因子胁迫处理系统概图 Fig.1 The overview of compound stresses treatment system |
| 表 1 正交实验因素水平 Tab.1 The levels of orthogonal experiment factors |
| 表 2 正交实验L16(45)设计 Tab.2 Orthogonal experiment design for L16(45) |
实验体系供试水体体积为55±0.72 L,每个钢化玻璃水族箱(30 cm×40 cm×60 cm)装有5 cm高的石英砂和45 cm高的水,石英砂(均长6.923 mm,宽5.653 mm,重0.226 g/粒)作为植物固定基质(培养前利用低浓度NaOH溶液浸泡杀藻处理24 h),选择初始长度为24.18±6.19 cm,株重为2.78±0.55 g规格的苦草,枝条均一,16个不同处理水族箱中均种植12株苦草,并设置2个重复.试验期间尽可能保证其采光和通风条件的一致性.实验共进行30 d,于第1天和第30天分别采集植株进行相应的理化实验分析.
实验体系用水采用简化的1/10倍Hongland溶液配置[40].配方如下:在1 L水中加入l ml 1 mol/L磷酸二氢钾溶液、5 ml 1 mol/L硝酸钾溶液、5 ml l mol/L硝酸钙溶液和2 ml l mol/L硫酸镁溶液,pH维持在6.8~7.2之间.
实验体系采用磷酸氢二铵溶液作为氮源,所配置的N1、N2、N3和N4的NH4+-N浓度分别在0.5~0.7、1.0~1.2、2.0~2.2和4.0~4.2 mg/L之间;低氧每天早(7:00)晚(19:00)利用高纯氮(99.99 %)通过自制的曝气装置进行均匀曝气,采用不同的曝气时间和曝气压力调节制得不同低氧梯度并测定,O1、O2、O3和O4的低氧浓度分别在7.5~7.8、6.5~6.8、5.5~5.8和4.0~4.5 mg/L之间.光照梯度采用增加或减少遮荫网层数获得.水族箱每隔3 d换一次体系用水,保持水深高度及浓度不变,实验期间,空气湿度60 % ~80 %,温度30±2℃.
1.3 分析方法水质指标测定:NH4+-N浓度采用纳氏试剂分光光度法进行测定,TN浓度采用过硫酸钾氧化-紫外分光光度法测定,TP浓度采用过硫酸钾消解-钼锑抗分光光度法测定[41].水体溶解氧浓度采用美国奥利龙(ORION)DO探头测定,温度、氧化还原电位和pH采用多参数水质分析仪测定,水下光照强度采用Li-1400于中午12:00在水下约30 cm处测定.
水生植物生长指标的测定:于第1天和第30天,随机收割每个水族箱中3株植物,采用蒸馏水洗净后用吸水纸将植物表面的水吸干净,随后称量植物鲜重(FW)等基本生长指标.再取部分叶片储存于-20℃环境中保存,可用于叶绿素浓度的分析.叶绿素浓度采用95 %乙醇提取48 h以上直至细粉完全变成白色并采用多波段分光光度法测定.以提取溶剂为空白,扫描测定提取液的吸收值A665、A649和A470,利用以下公式计算Chl.a、Chl.b、Chl.c.x和叶绿素总浓度(Tchl)(mg/L)[13, 42-44]:
| $ {\rm{Chl}}.{\rm{a = 13}}{\rm{.95}}{{\rm{A}}_{665}}-6.88{{\rm{A}}_{649}} $ | (1) |
| $ {\rm{Chl}}.b{\rm{ = 24}}{\rm{.96}}{{\rm{A}}_{649}}-7.32{{\rm{A}}_{665}} $ | (2) |
| $ {\rm{Chl}}{\rm{.c}}{\rm{.x = }}\left( {1000{{\rm{A}}_{470}}-2.05{\rm{Chl}}{\rm{.a-114}}{\rm{.8}}\;{\rm{Chl}}{\rm{.b}}} \right)/245 $ | (3) |
| $ {\rm{Tchl = Chl}}{\rm{.a + Chl}}{\rm{.b}} $ | (4) |
最后根据提取液中叶绿素浓度,换算为每克鲜叶中总叶绿素含量(mg/g(FW))[13, 42-44].
水生植物C-N代谢生理指标的测定:于第1天和第30天,随机收割每个水族箱中3株植物,采用蒸馏水洗净后用吸水纸将植物表面的水吸干净,于80℃烘干至恒重,研磨过200目筛后用于相应指标测定.植株粉末用80 %乙醇于80℃萃取20 min,离心后收集上清液,重复萃取2次并合并上清液.往上清液中加入10 mg的活性炭粉,并在60℃下水浴10 min使上清液褪色,经0.45 μm的滤膜过滤后,滤液用于测定游离氨基酸(FAA)和可溶性糖(SC)含量.残渣经30 %高氯酸萃取90 min后离心,上清液用于测定淀粉含量[45-47].
1.4 数据统计与处理采用DPS 9.50软件进行正交实验设计与统计分析.在正交实验方差分析之前所有数据都进行了正态性和齐性检验,显著性水平设置为0.05.对于非正态的数据需采取适当的方法(例如log10X,log10(1+X)或ln)进行转换后统计分析.图表采用MS Excel软件制作.
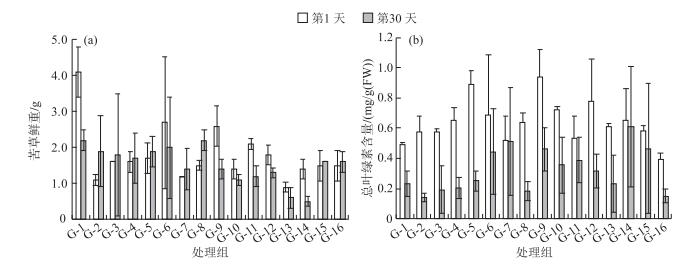
2 结果与分析 2.1 低氧、高铵和低光对苦草生长指标的影响30 d试验处理后,处理组G-13和G-14鲜重较低且与第1天相比分别下降27.8 %和33.3 %,即苦草在4 mg/L低氧、1 mg/L高铵及20 % ~30 %光照条件下不利于苦草植株的生长(图 2).在植株处理前期,低光照对其鲜重影响较大,经过30 d暴露处理后,低氧占主要胁迫地位,其次为低光和高铵,对鲜重减少的影响最为明显的组合为O4L4N2(即:O4=4 mg/L、L4=20 %、N2=1 mg/L,表 3).
|
图 2 低氧、高铵和低光对苦草鲜重(a)与总叶绿素含量(b)的影响 Fig.2 The effects of hypoxia, high ammonia and low light on fresh weights (a) and total chlorophyll contents (b) of V. natans |
| 表 3 苦草生长指标的极差与方差分析 Tab.3 ANOVA and orthogonal range analysis on growth indices of V. natans |
随着暴露时间的增加,各处理组苦草植株叶片受胁迫作用呈现不同程度的脱绿而变黄.处理组G-2叶绿素含量最低,仅为第1天含量的24.7 % (图 2).表明苦草在7.5 mg/L低氧、4 mg/L高铵和40 % ~50 %光强条件下,苦草光合色素的形成受阻,不利于苦草光合作用的进行.高铵对苦草植株光合作用的抑制作用相比低光和低氧影响更为突出,1 d处理后,胁迫叶绿素合成过程最为明显的试验组合为N3L1O1(即:N3=2 mg/L、L1=50 %、O1=7.5 mg/L),30 d处理后胁迫叶绿素合成过程最为明显的试验组合则为N4O1L2(即:N4=4 mg/L、O1=7.5 mg/L、L2=40 %,表 3).
极差与方差分析结果显示:苦草的鲜重在生长期不仅受低光和高营养盐浓度的影响,还受低氧较为显著的胁迫(P < 0.05).高铵、低氧和低光对苦草叶绿素含量影响不显著(表 3).
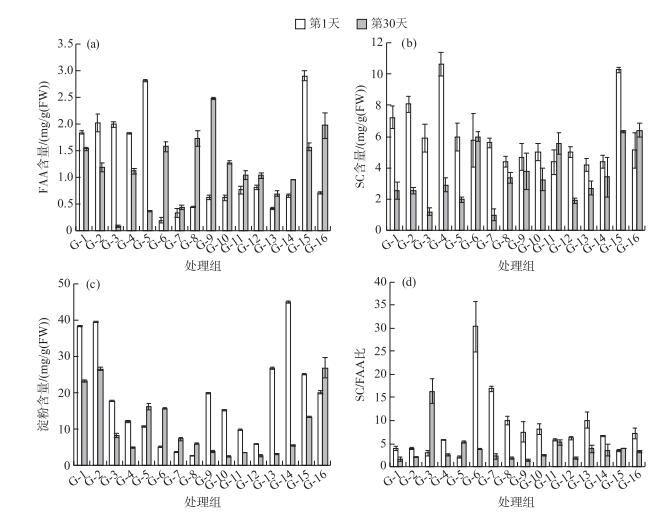
2.2 低氧、高铵和低光对苦草C-N代谢生理指标的影响30 d慢性处理后,处理组G-9的FAA含量最高而处理组G-3最低,即苦草在5.5 mg/L低氧、4 mg/L高铵及50 %光照组合条件下FAA含量最高,表明N-代谢活跃.处理组G-3和G-7的SC含量较低,数据表明随着光照强度的减弱,SC含量呈下降趋势,而在低氧水平上呈负相关关系.当铵浓度>1.0 mg/L时,SC含量波动范围小,但高于当铵浓度=0.5 mg/L时的值(图 3),淀粉含量呈降低趋势(正向影响最大的出现在N=1 mg/L,负向影响最大的出现在N=2 mg/L,表 4).而在1 d急性胁迫下,处理组G-7和G-8淀粉含量较低,表明苦草在6.5 mg/L低氧、2~4 mg/L高铵浓度、20 % ~30 %低光环境中受到明显抑制;第30天时,处理组G-5、G-6、G-7、G-8和G-16淀粉含量有所增加,而其余各组含量均呈现下降趋势.在20 %低光条件下淀粉含量下降较为明显(图 3). 30 d慢性处理后,苦草体内淀粉含量在20 %低光照条件、5.5 mg/L低氧及2 mg/L高铵(L4O3N3)下最低,低光影响最大;SC/FAA比在5.5 mg/L低氧、4 mg/L高铵及20 %低光照条件(N4L4O3)下最低,且高铵对其影响最大(图 3和表 4).
|
图 3 低氧、高铵和低光对苦草FAA(a)、SC(b)、淀粉含量(c)和SC/FAA比(d)的影响 Fig.3 The effects of hypoxia, high ammonia, low light on the contents of free amino acids (a), soluble carbohydrate (b), starch (c) and the ratio of SC/FAA (d) of V. natans |
| 表 4 苦草C-N代谢指标的极差与方差分析 Tab.4 ANOVA and orthogonal range analysis on C-N metabolism indices of V. natans |
极差与方差分析结果显示:沉水植物苦草的C-N代谢生理活动会因外界环境因素的影响而变化.高铵对FAA含量及SC/FAA比影响较大,但差异不显著(P>0.05),其次为低光与低氧;而低光照对SC含量变化影响大,其次为低氧与高铵;而淀粉含量在处理1 d时受低氧(P < 0.01)与高铵(P < 0.05)的显著影响而骤增,处理30 d后苦草受低光影响较高,但差异不显著(P>0.05),其次为低氧和高铵(表 4).
3 讨论 3.1 低氧、高铵和低光对苦草生长指标的影响植物鲜重可直观反映植株生长状况[15, 19, 25].本研究发现随着氧含量和光强的降低,苦草鲜重减少,即苦草生长受到抑制,其中低氧对苦草鲜重影响较大,差异显著(P < 0.05).李宽意等[38]发现低氧导致苦草的生物量降低但影响不显著,而对其块茎的形成显著不利,进而影响其生长与繁殖,这与本实验结果相似,但有所偏差,可能与本实验所设置的高营养盐水平及低光处理梯度差异有关,致使苦草对低氧胁迫表现出不同的响应.叶绿素含量是叶片衰老的重要标志之一,不仅表征植物生长状况,还与植物光合作用效率、营养状态等息息相关[19, 21-22, 42-44].本实验结果表明高铵对苦草叶绿素的形成影响较大,高于低氧与低光,且当铵态氮浓度高于1 mg/L时,叶绿素含量呈现下降趋势.在40 %光照强度、7.5 mg/L氧浓度和4 mg/L高铵浓度下,苦草叶绿素含量最低,表现出一定的抑制作用.尽管苦草可通过主动运输、氨基酸代谢等途径减轻高铵的胁迫与毒害[15, 17-21],但过量的铵会通过阻碍苦草对Mg2+的吸收和运输过程,进而影响植物光合作用以及光合色素的形成[25-32].
以往对长江中下游湖泊群的野外抽样调查研究发现,当铵态氮浓度>0.56 mg/L时,其对沉水植物苦草的生长会产生抑制作用,甚至全部消亡,当铵浓度较低时,可表现出一定的生长促进作用[30-31],与本实验结果一致.本研究中高铵对苦草影响不显著,可能与试验体系中铵态氮和硝态氮的比例有关.已有研究指出,苦草可在中营养湖泊中生存,即对水体营养盐有一定的耐受性,但营养盐的胁迫途径与阈值在很大程度上会因光照强度与水体氧含量的不同而发生改变[20-23, 29-31, 33, 39].黎慧娟等[22]研究也表明,其他生态因子对沉水植物的抑制作用仅在光照充足时发挥,而弱光照会降低高营养所产生的抑制作用[17-22],且高营养盐的抑制作用需要协同水体低氧实现[37, 39],这与本实验结果一致.从作为高浊度且富营养化水体的优势种及其低光合补偿点、饱和点等特性来看,莲座型的苦草较适宜生长在水体下层,即使在有限光强和氧含量条件下也能从周围环境中迅速摄取养分[16-17, 23, 39-40].在低光低氧环境下,苦草会增加体内叶绿素含量,以获得最大光合作用能力,从而应对逆境的胁迫压力[23, 39-40].
3.2 低氧、高铵和低光对苦草C-N代谢生理指标的影响植物体内FAA是合成蛋白质等含N化合物的原料,更是N-代谢过程重要中间产物,测定其在胁迫条件下的含量变化对研究植物在生长发育过程中的N-代谢具有重要意义[17, 19, 21, 27, 29, 32, 35-37].实验结果表明:当光照充足时,苦草植株内的FAA含量在低氧与高铵胁迫下呈上升趋势,这与Cao等[17, 19, 31-32]的研究结果相一致.高铵对植物体内FAA含量影响较大,归因于在高铵环境中植物体可通过消耗大量碳水化合物合成FAA,进而规避或缓解NH4+在体内过多累积而诱发的生理毒性[33, 37].
SC作为联接植物体内的光合作用、呼吸作用和碳水化合物储备的重要中间代谢产物与植物铵同化所需的重要底物,在植物C-N代谢中占有重要位置[17, 19, 21, 28, 32, 47].在本研究中,SC含量随光强减弱而降低,随氧含量降低而升高.当铵浓度高于0.5 mg/L时,SC含量变化不明显,表明高铵对SC含量影响较小.在20 %低光环境中,苦草生长代谢过程受到较高限制,能量短缺,SC消耗量增加,合成量减少.即使在氧含量充足且铵浓度不构成威胁时,SC也不足以缓解低光造成的胁迫压力.黎慧娟等[22]的研究发现,2.5 %低光处理较10 %光强下SC含量降低了82 % ~89 %.在本实验中,低光处理植株的FAA与SC含量均较低,发现SC消耗并非FAA合成的唯一途径,Cao等[17, 31]也曾表明此观点.而低氧处理的植株FAA与SC含量均相应升高,表明苦草即使在低氧环境下可通过储能物质如淀粉的分解产生大量的SC来同化氨氮合成FAA以抵抗逆境.本研究发现低氧、低光与高铵均会使得淀粉含量降低.在处理前期,苦草植株受低氧胁迫影响显著,其次是高铵与低光.实验30 d后,长期遮光与低氧处理,严重影响到植物的光合作用与呼吸作用,使得淀粉逐渐被消耗或合成储存量减少.淀粉作为植物重要碳水化合物储备物质,其含量高低能直接影响沉水植物的胁迫耐受能力,且与植物在不同营养水平、不同环境湖泊中的分布情况息息相关[17, 19, 21, 47].
Yu等[2, 17, 21, 36-37]发现SC/FAA比的变化能够反映胁迫环境对植物体内C-N代谢的影响,且可用来评估水生植物的生长和资源平衡[2, 17, 21, 36-37].在本实验中,SC/FAA比变化敏感,且在高铵胁迫时比值较小,这归因于高铵环境下植物体通过自身N代谢调节FAA的合成量抵抗外界高NH4+渗透或胁迫压力[17, 21-22, 25, 31-32],且在FAA的合成过程会消耗碳水化合物SC及其他物质.低光与低氧主要通过抑制植物光合作用和呼吸作用导致C-N代谢失衡,且在高铵条件下加重紊乱.
综上,苦草在低氧、高铵与低光环境中会受到三者的综合作用而致其生长受阻且C-N代谢失衡.我国富营养化湖泊中严重富营养化水域的底层溶解氧浓度甚至低至1 mg/L,水体氨氮浓度多在0.5~4 mg/L之间(苦草消失的富营养化湖泊水柱氨氮浓度>1 mg/L,而历史数据显示武汉南湖、龙阳湖和上海淀山湖氨氮浓度分别高达5.06、10.93和14.20 mg/L),消光系数2~5 m-1不等[8, 13, 31, 37].水生植物恢复一般受到低光的限制,对水下植物而言,在有毒物质(如氨氮)高浓度影响和低氧胁迫下植物恢复性生长更容易受到抑制.对于我国的富营养化浅水湖泊或深水湖泊而言,湖泊的水位、季节性波动、控制外源氮磷的大量输入、部分湖湾的跌水或适度曝气等措施进行人工调节可改善水生植物恢复的限制条件,可在一定程度地逐步推进富营养化湖泊系统向清水稳态转换.本研究是对三种关键胁迫因子耦合作用的阶段性成果,依然存在原位试验控制的诸多不确定难题,但客观反映了在自然光周期下多环境因子作用的复杂性和趋势,以及非线性光周期或比光量子强度对水下植物胁迫的影响机制更为复杂.本研究只是揭开富营养化湖泊沉水植物功能群遭受复合胁迫的冰山一角,对于推进深入认识其潜在胁迫机制具有价值,而深入研究和完善性试验依然有待继续.
4 结论本研究通过初步探索低氧、高铵与低光对沉水植物世界广布种苦草生长与C-N代谢的复合胁迫影响,主要得到以下结论:
1) 低光与低氧是通过抑制植物光合作用和呼吸作用而导致苦草生长受限、C-代谢失衡的主要因素.光照低于30 %,溶氧低于5.5 mg/L时,植株生长与C代谢受阻严重,碳水化合物储存量降低;高铵主要通过在植物体内大量累积而诱发毒性,消耗植物体内大量碳水化合物,从而抑制植物生长及代谢. NH4+-N>1.0 mg/L时,苦草N代谢活跃,FAA含量明显升高,SC/FAA比降低,淀粉含量呈降低趋势.
2) 富营养湖泊中苦草的衰退是多种因素综合作用的结果,本试验研究的低氧、高铵与低光3种环境因子均会对苦草的生长与C-N代谢产生不利影响.
3) 受损沉水植被在藻-草稳态转换的富营养化湖泊中应通过控制水体铵态氮浓度,严控低氧出现,及时提高水下照度或透明度(如控磷)来予以保护和科学管理;而在次生裸地且藻类占优势的富营养化水体中沉水植被的恢复与重建过程不仅要降低水体营养盐水平尤其是氨氮的水平,还应着重考虑如何有效提高水下光强与溶解氧浓度,并将如上环境因子控制在一定变幅范围内,且控制条件应原则上严于保护受损沉水植被所需的条件.
| [1] |
Phillips G, Willby N, Moss B. Submerged macrophyte decline in shallow lakes:what have we learnt in the last forty years?. Aquatic Botany, 2016, 135: 37-45. DOI:10.1016/j.aquabot.2016.04.004 |
| [2] |
Yu Q, Wang HJ, Wang HZ et al. Does the responses of Vallisneria natans (Lour.) Hara to high nitrogen loading differ between the summer high-growth season and the low-growth season?. Science of the Total Environment, 2017, 601/602: 1513-1521. DOI:10.1016/j.scitotenv.2017.05.268 |
| [3] |
Jupp BP, Spence DHN. Limitation on macrophytes in an eutrophic lake, Loch Leven:I. Effects of phytoplankton. Journal of Ecology, 1977, 65(1): 175-186. DOI:10.2307/2259493 |
| [4] |
Kemp WM, Twilley RR, Stevenson JC et al. The decline of submerged vascular plants in upper Chesapeake Bay:Summary of results concerning possible causes. Mar Tech Soc, 1983, 17: 78-89. |
| [5] |
Phillips GL, Eminson D, Moss B. A mechanism to account for macrophyte decline in progressively eutrophicated freshwaters. Aquatic Botany, 1978, 4: 103-126. DOI:10.1016/0304-3770(78)90012-8 |
| [6] |
Xu QJ, Jin XC, Yan CZ. Macrophyte degradation status and countermeasures in China. Ecology and Environmental Sciences, 2006, 15(5): 1126-1130. [许秋瑾, 金相灿, 颜昌宙. 中国湖泊水生植被退化现状与对策. 生态环境, 2006, 15(5): 1126-1130.] |
| [7] |
Qiu DR, Wu ZB. On the decline and restoration of submerged vegetation eutrophic shallow lakes. J Lake Sci, 1997, 9(1): 82-88. [邱东茹, 吴振斌. 富营养化浅水湖泊沉水水生植被的衰退与恢复. 湖泊科学, 1997, 9(1): 82-88. DOI:10.18307/1997.0113] |
| [8] |
Jin XC. Analysis of eutrophication state and trend for lakes in China. J Limnol, 2003, 62: 60-66. DOI:10.4081/jlimnol.2003.s1.60 |
| [9] |
Yu D, Chong YX, Tu MH et al. Study on the threatened aquatic higher plant species of China. Biodiversity Science, 1998, 6(1): 13-21. [于丹, 种云霄, 涂芒辉等. 中国水生高等植物受危种的研究. 生物多样性, 1998, 6(1): 13-21.] |
| [10] |
Li WC. Multiplicity of Stable States in Shallow Lakes and its Application. J Lake Sci, 1997, 9(2): 97-104. [李文朝. 浅水湖泊生态系统的多稳态理论及其应用. 湖泊科学, 1997, 9(2): 97-104. DOI:10.18307/1997.0201] |
| [11] |
Nian YG, Song YW, Li YJ et al. Regime shift theory and ecological restoration discussion in eutrophic shallow lakes. Research of Environmental Sciences, 2006, 19(1): 67-70. [年跃刚, 宋英伟, 李英杰等. 富营养化浅水湖泊稳态转换理论与生态恢复探讨. 环境科学研究, 2006, 19(1): 67-70. DOI:10.13198/j.res.2006.01.69.nianyg.017] |
| [12] |
Kong XH, Xiao LL, Su HJ et al. Status of aquatic plants and its relationship with water environment factors in the lakes along the lower reaches of the Yangtze River. J Lake Sci, 2015, 27(3): 385-391. [孔祥虹, 肖兰兰, 苏豪杰等. 长江下游湖泊水生植物现状及与水环境因子的关系. 湖泊科学, 2015, 27(3): 385-391. DOI:10.18307/2015.0303] |
| [13] |
Zhang M. Physio-ecological responses of aquatic macrophytes to the stresses of lake eutrophication[Dissertation]. Wuhan: Institute of Hydrobiology, Chinese Academy of Sciences, 2010. [张萌. 水生植物对湖泊富营养化胁迫的生理生态学响应[学位论文]. 武汉: 中国科学院水生生物研究所, 2010. ]
|
| [14] |
Scheffer M, Jeppesen E. Alternative stable states:The structuring role of submerged macrophytes in lakes. Ecological Studies, 1998, 131: 397-406. DOI:10.1007/978-1-4612-0695-8_31 |
| [15] |
Ni LY. Growth of Potamageton maackianus under low-light stress in eutrophic water. Journal of Freshwater Ecology, 2001, 16: 249-256. DOI:10.1080/02705060.2001.9663809 |
| [16] |
Zou LS, Nie ZY, Yao XY et al. Effects of light on submerged macrophytes in eutrophic water:Research progress. Chinese Journal of Applied Ecology, 2013, 24(7): 2073-2080. [邹丽莎, 聂泽宇, 姚笑颜等. 富营养化水体中光照对沉水植物的影响研究进展. 应用生态学报, 2013, 24(7): 2073-2080. DOI:10.13287/j.1001-9332.2013.0407] |
| [17] |
Cao T, Xie P, Ni LY et al. Carbon and nitrogen metabolism of an eutrophication tolerative macrophyte, Potamogeton crispus, under NH4+ stress and low light availability. Environmental and Experimental Botany, 2009, 66(1): 74-78. DOI:10.1016/j.envexpbot.2008.10.004 |
| [18] |
Larsson S, Wiren A, Lundgren L et al. Effects of light and nutrient stress on leaf phenolic chemistry in Salix dasyclados and susceptibility to Galerucella lineola (Coleoptera). Oikos, 1986, 47: 205-210. DOI:10.2307/3566047 |
| [19] |
Cronin G, Lodge DM. Effects of light and nutrient availability on the growth, allocation, carbon/nitrogen balance, phenolicchemistry, and resistance to herbivory of two freshwater macrophytes. Oecologia, 2003, 137(1): 32-41. DOI:10.1007/s00442-003-1315-3 |
| [20] |
Zhong AW, Cao T, Zhang M et al. Uptake of ammonium by Vallisneria natans and Myriophyllum spicatum under light and dark regimes. J Lake Sci, 2013, 25(2): 289-294. [钟爱文, 曹特, 张萌等. 光照和黑暗条件下苦草(Vallisneria natans)和穗花狐尾藻(Myriophyllum spicatum)对铵态氮的吸收. 湖泊科学, 2013, 25(2): 289-294. DOI:10.18307/2013.0217] |
| [21] |
Zhang M, Cao T, Ni LY et al. Carbon, nitrogen and antioxidant enzyme responses of Potamogeton crispus to both low-light and high-nutrient stresses. Environmental and Experimental Botany, 2010, 68(1): 44-50. DOI:10.1016/j.envexpbot.2009.09.003 |
| [22] |
Li HJ, Ni LY, Cao T et al. Responses of Vallisneria natans to reduced light availability and nutrient enrichment. Acta Hydrobiologica Sinica, 2008, 32(2): 225-230. [黎慧娟, 倪乐意, 曹特等. 弱光照和富营养对苦草生长的影响. 水生生物学报, 2008, 32(2): 225-230.] |
| [23] |
Morris K, Harrison KA, Bailey PCE et al. Domain shifts in the aquatic vegetation of shallow urban lakes:The relative roles of low light and anoxia in the catastrophic loss of the submerged angiosperm Vallisneria americana. Marine & Freshwater Research, 2004, 55(8): 749-758. DOI:10.1071/MF03193 |
| [24] |
Zhong AW, Cao T, Ni LY et al. Growth and membrane permeability of two submersed macrophytes in response to ammonium enrichment. Aquatic Biology, 2013, 19: 55-64. DOI:10.3354/ab00514 |
| [25] |
Ni LY. Effects of water column nutrient enrichment on the growth of Potamogeton maackianus A. Been. Journal of Aquatic Plant Management, 2001, 39: 83-87. |
| [26] |
Apudo AA, Cao Yu, Wakibia J et al. Physiological plastic responses to acute NH4+-N toxicity in Myriophyllum spicatum L. cultured in high and low nutrient conditions. Environmental and Experimental Botany, 2016, 130: 79-85. DOI:10.1016/j.envexpbot.2016.05.009 |
| [27] |
Zhou QY, Gao JQ, Zhang RM et al. Ammonia stress on nitrogen metabolism in tolerant aquatic plant-Myriophyllum aquaticum. Ecotoxicology and Environmental Safety, 2017, 143: 102-110. DOI:10.1016/j.ecoenv.2017.04.016 |
| [28] |
Gao J, Li L, Hu Z et al. Ammonia stress on the carbon metabolism of Ceratophyllum demersum. Environ Toxicol Chem, 2015, 34(4): 843-849. DOI:10.1002/etc.2866 |
| [29] |
Gao J, Li L, Hu Z et al. Effect of ammonia stress on nitrogen metabolism of Ceratophyllum demersum. Environ. Toxicol. Chem., 2016, 35(1): 205-211. DOI:10.1002/etc.3182 |
| [30] |
Song R, Jiang JL, Geng JJ et al. Physiological effect of Vallisneria natans L. under different concentrations of ammonia. Chinese Environment Science, 2011, 31(3): 448-453. [宋睿, 姜锦林, 耿金菊等. 不同浓度铵态氮对苦草的生理影响. 中国环境科学, 2011, 31(3): 448-453.] |
| [31] |
Cao T, Xie P, Ni LY et al. The role of NH4+ toxicity in the decline of the submersed macrophyte Vallisneria natans in lakes of the Yangtze River basin, China. Mar Freshwater Res, 2007, 58: 581-587. DOI:10.1071/MF06090 |
| [32] |
Li HJ, Cao T, Ni LY. Effects of ammonium on growth, nitrogen and carbohydrate metabolism of Potamogeton maackianus A. Benn. Fundamental and Applied Limnol (Arch Hydrobiol), 2007, 170(2): 141-148. DOI:10.1127/1863-9135/2007/0170-0141 |
| [33] |
Cao T, Xie P, Li ZQ et al. Physiological stress of high NH4+ concentration in water column on the submersed macrophyte Vallisneria natans L. Bulletin of Environmental Contamination and Toxicology, 2009, 82: 296-299. DOI:10.1007/s00128-008-9531-5 |
| [34] |
Guo HT, Cao T, Ni LY. Effects of different nutrient conditions on the growth of a submerged macrophyte, Vallisneria natans, in a mesocosm experiment. J Lake Sci, 2008, 20(2): 221-227. [郭洪涛, 曹特, 倪乐意. 中等实验规模下不同营养环境对苦草(Vallisneria natans)生长的影响. 湖泊科学, 2008, 20(2): 221-227. DOI:10.18307/2008.0214] |
| [35] |
Zhang M, Wang ZQ, Xu J et al. Ammonium, microcystins, and hypoxia of blooms in eutrophic water cause oxidative stress and C-N imbalance in submersed and floating-leaved aquatic plants in Lake Taihu, China. Chemosphere, 2011, 82(3): 329-339. DOI:10.1016/j.chemosphere.2010.10.038 |
| [36] |
Smolders AJP, den Hartog C, van Gestel CBL et al. The effects of ammonium on growth, accumulation of free amino acids and nutritional status of young phosphorus deficient Stratiotes aloides plants. Aquatic Botany, 1996, 53: 85-96. DOI:10.1016/0304-3770(95)01014-9 |
| [37] |
Smolders AJP, van RielMC, Roelofs JGM. Accumulation of free amino acids as an early indication for physiological stress (nitrogen overload) due to elevated ammonium levels in vital Stratiotes aloides L. Stands. Arch Hydrobiol, 2000, 150: 169-175. DOI:10.1127/archiv-hydrobiol/150/2000/169 |
| [38] |
Li KY, Liu ZW, Wang CZ et al. Effect of low dissolved oxygen on the growth of Vallisneria spiralis. Resources and Environment in the Yangtze Basin, 2006, 15(5): 670-673. [李宽意, 刘正文, 王春忠等. 低溶解氧对苦草生长的影响. 长江流域资源与环境, 2006, 15(5): 670-673.] |
| [39] |
Xiong BH, Li W. Ecological studies on Vallisneria L. in China. Journal of Wuhan Botanical Research, 2000, 18(6): 500-508. [熊秉红, 李伟. 我国苦草属(Vallisneria L.)植物的生态学研究. 武汉植物学研究, 2000, 18(6): 500-508.] |
| [40] |
Yan CZ, Zeng AY, Jin XC et al. Physiological effects of ammonia-nitrogen concentrations on Hydrilla verticillata. Acta Ecologica Sinica, 2007, 27(3): 1050-1055. [颜昌宙, 曾阿妍, 金相灿等. 不同浓度氨氮对轮叶黑藻的生理影响. 生态学报, 2007, 27(3): 1050-1055.] |
| [41] |
"Water and waste water monitoring and analysis method" editorial board of State EPA of China. Monitoring and analysis methods of Water and waste water. fourth edition. Beijing: China Environmental Science Press, 2002. [国家环境保护总局《水和废水监测分析方法》编委会. 水和废水监测分析方法: 第4版. 北京: 中国环境科学出版社, 2002.]
|
| [42] |
Yang ZC, He W, Mou ST et al. Plant growth and development of pepper seedlings under different photo periods and photon flux ratios of red and blue LEDs. Transactions of the Chinese Society of Agricultural Engineering, 2017, 33(17): 173-180. [杨振超, 何蔚, 牟孙涛等. 不同光周期和红蓝光质配比对辣椒幼苗生长发育的影响. 农业工程学报, 2017, 33(17): 173-180. DOI:10.11975/j.issn.1002-6819.2017.17.023] |
| [43] |
Lichtenthaler HK, Wellburn AR. Determinations of total carotenoids and chlorophylls a and b of leaf extracts in different solvents. Biochemical Society Transactions, 1983, 11(5): 591-592. DOI:10.1042/bst0110591 |
| [44] |
Lichtenthaler HK. Chlorophylls and carotenoids:pigments of photosynthetic biomembranes. Methods Enzymol, 1987, 148: 350-382. DOI:10.1016/0076-6879(87)48036-1 |
| [45] |
Yemm EW, Willis AJ. The estimation of carbohydrates in plant extracts by anthrone. Biochem J, 1954, 57: 508-514. DOI:10.1042/bj0570508 |
| [46] |
Yemm EW, Cocking EC, Ricketts RE. The determination of amino-acids with ninhydrin. Analyst, 1955, 80: 209-213. DOI:10.1039/an9558000209 |
| [47] |
Dirk LMA, Van der Krol AR, Vreugdenhil D et al. Galactomannan, soluble sugar and starch mobilization following germination of Trigonella foenum-graecum seeds. Plant Physiol Biochem, 1999, 37: 41-50. DOI:10.1016/S0981-9428(99)80065-5 |
 2018, Vol. 30
2018, Vol. 30 


