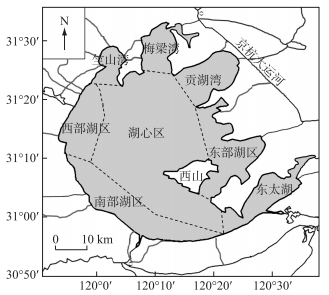
近年来,淡水湖泊水体富营养化以及随之而来的蓝藻水华暴发和藻毒素浓度升高已经成为全世界关注的重大环境问题之一[1-2].太湖位于中国经济最发达、人口最密集的长江流域下游地区[3],是我国第三大淡水湖,平均水深1.9 m,是典型的亚热带浅水湖泊.太湖水面面积2338 km2,湖湾包括竺山湾、梅梁湾、贡湖湾、胥口湾和东太湖等(图 1),流域人口逾6000万[4].
|
图 1 太湖地图 Fig.1 Map of Lake Taihu |
1960s以前,太湖水体处于贫营养的状态[5],随着流域内工农业生产发展和人类活动强度的增加,太湖水体营养盐水平不断上升. 1980s开始,太湖流域工农业现代化、城市化进程加快[6],大量氮、磷营养盐输入太湖,导致湖水由中营养逐渐向富营养状态过渡,1980s末已达到富营养化程度,1990s至2000年太湖富营养化程度日趋加剧,重度富营养状态从局部水体向主湖区扩张[7].太湖水体富营养导致蓝藻水华暴发面积不断扩大,2007年太湖蓝藻大暴发导致无锡市饮用水危机[8],太湖水环境质量与周边居民的生活息息相关,藻类产生的藻毒素对水生生物和人类健康造成潜在危害.因此,保障太湖水环境安全已成为环境保护的头等大事.如今,通过铁腕治污,太湖入湖氮、磷负荷得到有效削减,富营养化程度得到一定的控制[9],但蓝藻水华暴发的面积仍然较大,对太湖水质和生态系统安全造成巨大的威胁.
2 太湖蓝藻水华形成条件短短几十年间太湖水质从贫营养状态发展到富营养化状态,蓝藻水华不断暴发,引发了全世界科研工作者的广泛关注.蓝藻水华形成的条件主要包括蓝藻本身的生理特征,不同季节优势藻属的演替,水动力条件、气象、水体营养盐浓度和水生态系统结构转变等[10].
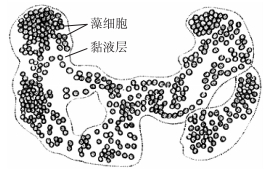
2.1 蓝藻自身的特征及优势种的演替蓝藻是一类光合自养的革兰氏阴性细菌,形态多样,分布广泛[11-12].太湖蓝藻种类多样,包括微囊藻属(Microcystis)、聚球藻属(Synechococcus)、蓝菌属(Cyanobium)、鱼腥藻属(Anabaena)等,太湖的蓝藻水华通常以微囊藻属为主[13].微囊藻细胞能够产生荚膜和黏液层(图 2),主要由胞外多糖组成,具有粘滞性[14],从而形成网状胶群体,以避免浮游动物摄食、病毒或细菌的侵染以及其他不良环境对细胞的伤害.胞外多糖在网状胶群体内能够形成细胞间空隙,与伪空胞共同提供浮力[15-16],从而使微囊藻群体能够上浮占据有利的生态位.它们对环境的适应能力强,藻细胞能够合成类菌孢素氨基酸(mycosporine-like amino acids)防止夏季强烈紫外线照射的伤害[17],在高温、低光强下也能够很好地生长[18].其中铜绿微囊藻(Microcystis aeruginosa)还具有适应氧化还原电位变化的生理性机制,低氧化还原电位胁迫消除后,藻细胞可以恢复到原来的生长状态[19].部分微囊藻能够产生微囊藻毒素,抑制其他藻类的生长[20],进一步诱发水生态系统藻类群落发生演替[21],藻细胞衰亡产生的藻毒素和氨氮使苦草、鱼类细胞活性氧自由基累积,产生氧化损伤[22],藻毒素还会改变浮游动物的生活史导致其存活和繁殖能力下降,诱发鱼类肝脏细胞代谢过程紊乱.微囊藻属具有浮力、团聚抵抗浮游动物摄食以及产生藻毒素和氨氮对大型水生植物产生毒性等特征,使得它相对于其他浮游植物和大型水生植物具有更强的竞争能力,成为优势类群并在水面上形成水华[23].
|
图 2 蓝藻水华微观结构 Fig.2 Microstructure of cyanobacterial bloom |
不同季节优势蓝藻之间的演替也是太湖蓝藻维持和发展的重要因素.聚球藻属为自养超微浮游植物,比表面积大使得它们能够更好地吸收和利用营养,但其时空分布上没有明显的变化.冬季和春季鱼腥藻属和蓝菌属是东太湖和南部沿岸区的优势蓝藻属,在富营养化水平较低时这类超微浮游植物在对营养盐的利用上更具优势.夏、秋季在高温、高营养盐水平下微囊藻属则处于统治地位,它不断繁殖并通过产生藻毒素抑制其他藻类生长而将其取代,在西部沿岸区、竺山湾和梅梁湾暴发蓝藻水华.不同季节不同物种之间的转换使得蓝藻能够长期处于优势地位[24].
2.2 太湖特定的地理、水文和气象特征太湖地处亚热带,冬季不会全湖封冻,利于蓝藻越冬.春季温度升高,蓝藻生物量不断增加,成为水体中的优势种,但它仍趋向均匀分布,水动力的输移使蓝藻大量聚集到特定区域,从而暴发蓝藻水华[25].湖流紊动动能、风向与湖湾夹角耦合是影响蓝藻水华输移和空间分布异质性的关键因素.在大型浅水湖泊太湖,风力驱动的紊动动能和势能的转化决定了蓝藻水华垂直分布的空间异质性,风在水面做功使水的紊动动能增加,一部分转化为水的势能,促进水体混合,表层蓝藻水华在垂直方向趋于混合均匀[26].值得注意的是,太湖风速超过7 m/s时,水柱中叶绿素a浓度在垂直方向混合均匀,蓝藻不在水面形成蓝藻水华;而低风速下(小于3 m/s),出现叶绿素a垂直分层,表层叶绿素a浓度高,形成蓝藻水华(图 3)[27].湖湾的主轴线方向与风向的夹角决定外源性蓝藻水华水平分布的空间异质性.孔繁翔等[18, 28]对太湖蓝藻水华遥感信息和太湖风玫瑰图的分析发现,不同季节的风况驱动蓝藻水华在太湖的空间分布,以夏季为例,太湖高频率的东南风与太湖主水流方向相反,风力作用使上浮蓝藻水华聚集在下风处,水体中悬浮藻类随水流走,二者相互分离,这种“淘洗作用”使得上浮的蓝藻成为优势种,在太湖西北、北部湖区堆积,形成蓝藻水华(图 4).

|
图 3 台风海葵期间平均风速、浊度和叶绿素a浓度随时间的变化[27] Fig.3 Temporal variations in the hourly mean wind speed, turbidity, and chlorophyll-a concentration during Typhoon Haikui |

|
图 4 太湖不同季节蓝藻水华分布[28] Fig.4 Seasonal distribution of cyanobacterial bloom in Lake Taihu |
除了水动力条件,温度和光照也是蓝藻生长和繁殖的主要控制因子.温度升高促进蓝藻生长,蓝藻的光合作用速率和生长速率在25℃以上显著增加[29],最适生长温度为27~37℃,而大多数其他浮游植物最适生长温度在20~25℃之间,如硅藻最适生长温度为17~22℃[30],因此,温度升高除了促进蓝藻生长外还提高了其与其他藻类的竞争力.利用生态学代谢理论中关于物种生长速率依赖于温度的原理,通过阿伦尼乌斯方程将活化能换算为生长速率值进行竞争优势比较,结果也显示与绿藻相比,蓝藻拥有更高的活化能,从而具有更快的生长速率[31].同时,高温可增强水柱层化,抑制湍流混合,在高辐照和低风速情况下[32],蓝藻利用伪空胞上浮到表层获得充足的光照,以此获得优势的生态位,限制其他藻类光合作用[33].因此,在夏季高温情况下蓝藻更具生长优势.全球气候变暖使太湖水体春季升温提前,秋季温度下降时间推迟,延长了蓝藻生长的时间.
2.3 太湖草型-藻型生态系统的转换不同水生态系统中营养盐赋存形态不同.清水-草型生态系统中随着氮、磷营养盐浓度增加,大型水生植物将其同化为水草的生物量,进入草型生态系统;而浊水-藻型生态系统中氮、磷营养盐会被浮游藻类利用,进而被浮游动物和鱼类摄食,进入藻型生态系统,这种吸收同化机制使两种生态系统中所测得的氮、磷营养盐浓度明显不同,藻型生态系统中氮、磷营养盐浓度高于草型生态系统[34].湖泊中大型水生植物与蓝藻相互竞争氮、磷营养盐及光能[35],一方面,大型水生植物能够分泌化感物质抑制浮游植物生长[36-37],同时能够遮光抑藻[38],控制富营养化水体中藻类的生长.但是,在另一方面,藻类生物量增加,水体透明度下降,同时藻毒素浓度增加,很大程度上对大型水生植物产生毒性[39-40],在一定的营养盐浓度区间内,原本生态系统在外界环境扰动(风浪、光抑制和鱼类牧食)下极易发生草-藻转换[41].太湖梅梁湾水域属于典型藻型生态系统,频繁暴发蓝藻水华,富营养化呈现加剧趋势;胥口湾水域属草型生态系统,由于水草打捞,近年来也受到水体富营养化的困扰,藻类数量不断增加,清水-草型生态系统失稳.这种转变过程可用较为流行的稳态转化理论解释[42],水体中营养盐浓度升高,超过大型水生植物吸收营养盐速率,能够快速吸收营养盐的浮游藻类生物量急剧增加,形成有机团聚体,附着微生物快速生长繁殖,水体中有机物的分解和矿化速率加快,同时水体浊度增加,大型水生植物退化,使得水体富营养化程度加剧,造成恶性循环,东太湖、胥口湾水体呈现向藻型生态系统转化的趋势[43-44].
2.4 高浓度营养盐的刺激氮、磷等营养盐过量输入是引起湖泊水体富营养化主要原因之一,其输入途径包括河流输入、大气干湿沉降、浅层地下水的渗滤、鸟类排泄和船舶等移动源排放等.太湖氮、磷营养盐主要来源于周边工农业生产废水和城镇农村的生活污水. 2009—2010年太湖河道氮素年输入总量约为7万t,总磷年输入量约为3756 t[45],较2001—2002年显著增加.
Ma等[46]通过太湖水添加氮、磷试验证实,添加氮可以促进所有浮游植物的生长,使微囊藻群体的大小保持不变的同时提高微囊藻在所有浮游植物生物量中所占的比例.添加磷会使得微囊藻形成更小的群体,但对其生长和占总浮游植物生物量的比例没有影响,同时添加氮和磷比单独添加氮更能明显地促进浮游植物的生长.水体中氮、磷营养盐不仅影响到蓝藻水华发生的规模与持续时间,而且会对蓝藻的团聚形态产生影响[47-48]. Wilhelm等通过太湖南北向的大面积观测研究发现[49]:太湖中总氮和总磷浓度与蓝藻的生物量有着强烈的相关性. Xu等通过现场取样和原位营养盐添加测定蓝藻水华生物量变化得出浮游植物生长的营养阈值和不同季节营养盐限制的区别[50],研究发现,氮、磷营养盐的比值季节性变化显著,冬季和春季TN:TP比值在30~80:1之间,TDN:TDP比值在52~212:1之间,这些比值在夏季均降至20:1以下,表明春季和冬季浮游植物的生长主要受到磷限制,磷浓度升高能够显著提高浮游植物的生物量和生长速率;而夏、秋季蓝藻水华发生时,氮是主要限制因子,磷是次要限制因子.值得注意的是,太湖蓝藻水华暴发导致反硝化脱氮能力增强,氮素成为藻类生长的限制因子是蓝藻水华暴发的结果,而不是夏季入湖氮素减少的结果.因此,在控制太湖富营养化和蓝藻水华暴发的过程中,尽管减少磷负荷很重要,但夏季要控制蓝藻水华发生规模和持续时间,控制氮素的输入亦是关键.
2.5 太湖水体营养盐四重循环是蓝藻水华暴发的强化机制水生态系统具有一定的稳定性,湖泊水体一旦形成藻型生态系统,需要强大的外部干预才能转化为草型生态系统,藻型生态系统具有的自我强化特性是蓝藻水华难于控制的原因所在.水体氮、磷营养盐的四重循环是太湖藻型生态系统自我强化机制.
从细菌学角度来说,蓝藻细胞之间存在营养盐循环,蓝藻通过形成聚磷颗粒实现磷酸盐的超累积,以供群体持续增长,衰亡蓝藻释放出大量颗粒态氮、磷营养盐,又可以被其他蓝藻所吸收,实现蓝藻-蓝藻之间氮、磷循环,有利于蓝藻持续增殖[51-52].蓝藻细胞内部和细胞之间这种氮、磷代谢模式使得水体中滞留大量氮、磷,在水体中氮、磷停留时间远远大于水体交换周期,有利于蓝藻水华暴发.
蓝藻生长形成团聚体,为附生细菌提供了更多的空间,附生细菌吸收衰亡蓝藻中的氮、磷,作为一种临时储库,这部分氮、磷可以被蓝藻再利用,实现蓝藻与附生细菌之间氮、磷循环[53-54].
微生物活动可以加快沉积物中氮、磷形态转化,并促进底泥氮、磷的释放,为蓝藻水华颗粒增加了氮、磷供给,同时,蓝藻水华颗粒能泵取沉积物中氮、磷而生长;衰亡的蓝藻水华颗粒分解矿化后又回到沉积物中,从而实现沉积物与蓝藻水华颗粒之间的氮、磷循环[55-59].
太湖不同湖区之间存在着水体的交换,太湖主要入湖河道在西部,出湖河道在东南部,氮、磷营养盐随水流向东南湖区输送,而夏季在东南风的驱动下蓝藻水华向西北和北部湖区运移,通过这种“淘洗”作用,以蓝藻水华颗粒为载体的氮、磷营养盐在不同湖区之间发生循环[60-61],延长了氮、磷营养盐在湖体中的停留时间.
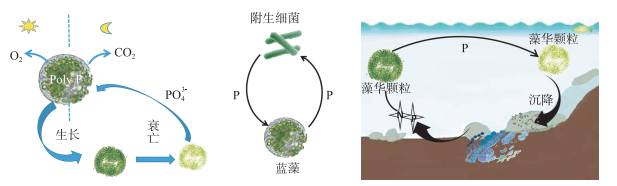
以上蓝藻-蓝藻、蓝藻-附生细菌、藻华-沉积物和湖区-湖区循环构成了太湖氮、磷营养盐的四重循环(图 5),这四重循环链正是太湖蓝藻水华持续暴发的原因所在,因此,太湖水体一旦暴发蓝藻水华,就难于消除.
|
图 5 太湖水体中氮、磷营养盐的四重循环示意图 Fig.5 Cycles of nitrogen and phosphorus nutrients in Lake Taihu |
太湖湖体氮、磷营养盐浓度影响蓝藻水华暴发强度,蓝藻水华对氮、磷营养盐的变化也存在反馈机制. 2017年太湖虽然外源氮、磷输入量变化不大,但太湖蓝藻的快速生长导致其从底泥中泵取大量磷,使得水体中颗粒态磷含量增加,水体与沉积物之间的磷平衡被打破,大量磷由沉积物进入水体.衰亡的蓝藻细胞会释放出大量的絮体态氮、磷营养盐,由于采用通常的过滤方法无法去除水体中絮体藻类,导致水体中磷浓度升高,死亡蓝藻细胞的降解使得水体溶解氧水平降低,加速了沉积物中磷酸盐的释放[62],水体磷含量的增加又为蓝藻生长提供了物质基础,太湖水体中磷含量与蓝藻生长形成不断放大的正向反馈.这也进一步印证了藻华与沉积物之间存在营养盐的四重循环.因此,2017年太湖水体平均总磷偏高极有可能是蓝藻大面积暴发的结果.
2016年和2017年度太湖水体夏季总氮浓度下降也与蓝藻水华暴发相关. 2016年由于太湖地区大范围高强度暴雨导致大量氮、磷营养盐输入太湖,蓝藻快速生长并在湖滨带堆积使得水体中溶解氧含量下降[63],加之太湖水体中氮素主要以硝态氮形态存在,有利于反硝化细菌的生长.同时蓝藻水华颗粒衰亡使得水体中有机物浓度增加[64],为太湖水体反硝化细菌提供了大量碳源,反硝化细菌大量繁殖,硝态氮通过反硝化转化为氮气,夏季较高的温度提高了反硝化的速率,测定结果表明,太湖水体反硝化脱氮能削减太湖输入总氮量的30 % ~40 % [65],因此,导致近年夏季太湖水体总氮浓度不断下降.夏季太湖蓝藻水华大规模暴发,水体总氮浓度下降是蓝藻水华大规模暴发的结果,这是水生态系统中生物控制自身繁殖速率的一种负反馈调节机制.
4 太湖蓝藻水华控制对策在太湖蓝藻水华暴发的众多影响因素之中,蓝藻自身的生理生化特性、太湖的地理、气候特征等物理因素是无法改变的.水文过程可以通过建立多参数的水动力学模型,从而获得合适的生态调水时机和调水量[66],通过调水达到改变太湖水生态环境和初级生产者类型的目的.但不管调水方式如何,总调水量相对于河道入湖水量而言还是较少,对于缩短太湖换水周期作用十分有限.
蓝藻水华暴发是人类向湖泊中排放过量氮、磷营养物质所引发的,因此,降低水体中氮、磷营养盐浓度是控制水体富营养化的关键所在[67].减少水体中营养物质首先要减少其输入,这是目前最直接的控制方法,相较于其他方法,控制外源输入更易于操作,也是现阶段富营养化湖泊治理最主要、常用的手段.面源污染的控制需要多方的努力,例如,要控制农业生产带来的面源污染,必须制定并实施更严格的土地政策,控制化肥的使用或在流域尺度上添加土壤的改良剂[68].控制氮、磷输入总量的同时,还应注意氮磷比值的调节.水体中氮磷质量比≥23时,藻类生物含氮量大于或等于反硝化脱氮量,则水体为磷限制;氮磷质量比≤9时,藻类生物含氮量小于等于反硝化脱氮量,则为氮限制;其他情况下,氮、磷营养盐协同控制浮游植物的生长[69].氮磷比不仅可以用来判断水体蓝藻生长是氮限制还是磷限制,还可以用来区分湖泊中蓝藻是否处于主导地位[70-71],当TN:TP < 29:1时,蓝藻在与其他浮游植物的竞争中更具有优势,反之则蓝藻不处于主导地位.
太湖蓝藻水华控制策略已从湖泊流域氮、磷污染控制为主转入到湖内、湖外氮、磷污染控制并重,实施疏堵结合的方针,在有效控制太湖外源氮、磷污染输入的同时,应加强湖内氮、磷污染的去除.改变湖泊水生态系统结构有利于抑制蓝藻生长,在富营养化得到一定程度控制的前提下,采用生态调控的方法,在东太湖、东部湖区以及贡湖湾恢复湖滨湿地,增加湖体浮叶植物和沉水植物面积[18],提高贝类、鱼类等水生动物数量,通过调控水生态系统结构,使适合的湖区从浊水-藻型生态系统向清水-草型生态系统演替,减轻蓝藻水华暴发强度.控源与生态恢复并举是未来一段时间内太湖蓝藻水华控制的策略.除了恢复水生植被为水生态系统初级生产者主要组成部分,增强湖泊污染自净作用外,还可在水华暴发较为严重的梅梁湾、竺山湾划分出一定的水域,使用其他物理化学方法强化湖泊内氮、磷营养盐的去除,以期建立良性循环的湖泊水生态系统.
生态调控是恢复湖泊水生态系统健康的关键所在,在区域控污的同时,环保、农业、水利和渔业等多部门必须协调统一,调整太湖管理模式,才能有效控制太湖富营养化,遏制蓝藻水华暴发规模,实现太湖管理思路实现从控源截污为主向控源截污与湖泊生态调控并重的重大转变.
5 结论与展望近年关于太湖蓝藻水华持续暴发机制虽有一定的认识,但具体到各个因子的定量耦合关系仍存在诸多未解之谜.研究者们已建立许多模型预测太湖蓝藻水华的暴发过程,但仍没有一个公认的可以准确预测蓝藻水华暴发的模型.太湖水华暴发的主体是蓝藻,蓝藻作为一种细菌,可以考虑从细菌学角度对蓝藻生长、繁殖、暴发的环境因素进行研究,能更一步揭示湖泊蓝藻水华持续暴发成灾机理.
湖泊水生态系统是一个有机系统,湖泊富营养化是水生态系统演替的结果.蓝藻水华暴发的原因是蓝藻独特的生理生化特征,太湖所处的亚热带浅水型湖泊为蓝藻的生长提供了合适的温度和水动力条件,加之太湖流域内人类活动造成的氮、磷营养盐大量排放,因此,“天时、地利和人为”综合作用导致太湖成为蓝藻水华暴发的重灾区.历史上太湖都有面积不等的蓝藻水华暴发,蓝藻是藻型生态系统正常的初级生产者,因此,控制太湖蓝藻水华大面积暴发不可能一蹴而就,要在不断控制营养盐输入的前提下进行大型水生植物修复,在适宜的湖区实现水生态系统向清水-草型系统演替.我们对于适宜进行大型水生植物修复的营养盐浓度阈值、水动力学条件等尚不清楚,盲目对水体进行大型水生植物修复往往得不到预期的效果,因此,弄清营养盐浓度、水文状况与大型水生植物和藻类竞争生长的耦合机制十分重要,是太湖蓝藻水华控制未来需解决的科学问题之一.
| [1] |
Paerl HW, Otten TG. Harmful cyanobacterial blooms:causes, consequences, and controls. Microbial Ecology, 2013, 65(4): 995-1010. DOI:10.1007/s00248-012-0159-y |
| [2] |
Singh S, Rai PK, Chau R et al. Temporal variations in microcystin-producing cells and microcystin concentrations in two fresh water ponds. Water Research, 2015, 69: 131-142. DOI:10.1016/j.watres.2014.11.015 |
| [3] |
Liu EF, Yang XD, Shen J et al. Environmental response to climate and human impact during the last 400 years in Taibai Lake catchment, middle reach of Yangtze River, China. Science of the Total Environment, 2007, 385(1/2/3): 196-207. DOI:10.1016/j.scitotenv.2007.06.041 |
| [4] |
Yang L, Ding JH. A measurement of population's driving effects on water resources consumption in the progress of urbanization:A case study of Taihu basin. South China Population, 2014, 29(2): 72-80. [杨亮, 丁金宏. 城镇化进程中人口因素对水资源消耗的驱动作用分析——以太湖流域为例. 南方人口, 2014, 29(2): 72-80. DOI:10.3969/j.issn.1004-1613.2014.02.009] |
| [5] |
Zhang YD, Su YL, Liu ZW et al. Sedimentary lipid biomarker record of human-induced environmental change during the past century in Lake Changdang, Lake Taihu basin, Eastern China. Science of the Total Environment, 2017, 613: 907-918. DOI:10.1016/j.scitotenv.2017.09.185 |
| [6] |
Deng JC, Wang YS, Liu X et al. Spatial distribution and risk assessment of heavy metals and As pollution in the sediments of a shallow lake. Environmental Monitoring and Assessment, 2016, 188: 296. DOI:10.1007/s10661-016-5301-8 |
| [7] |
Wu YY, Zhang GF. Water environment changes of Taihu Basin since the 1950s and its driving factors. Economic Geography, 2014, 34(11): 151-157. [吴月芽, 张根福. 1950年代以来太湖流域水环境变迁与驱动因素. 经济地理, 2014, 34(11): 151-157.] |
| [8] |
Qin BQ, Zhu GW, Gao G et al. A drinking water crisis in Lake Taihu, China:linkage to climatic variability and lake management. Environmental Management, 2010, 45(1): 105-112. DOI:10.1007/s00267-009-9393-6 |
| [9] |
Dai XL, Qian PQ, Ye L et al. Changes in nitrogen and phosphorus concentrations in Lake Taihu, 1985-2015. J Lake Sci, 2016, 28(5): 935-943. [戴秀丽, 钱佩琪, 叶凉等. 太湖水体氮、磷浓度演变趋势(1985-2015年). 湖泊科学, 2016, 28(5): 935-943. DOI:10.18307/2016.0502] |
| [10] |
Paerl HW, Otten TG. Harmful cyanobacterial blooms:causes, consequences, and controls. Microbial Ecology, 2013, 65(4): 995-1010. DOI:10.1007/s00248-012-0159-y |
| [11] |
Paerl HW, Paul VJ. Climate change:Links to global expansion of harmful cyanobacteria. Water Research, 2012, 46: 1349-1363. DOI:10.1016/j.watres.2011.08.002 |
| [12] |
Knoll AH. Cyanobacteria and earth history. In: Herrero A, Flores E eds. The Cyanobacteria: Molecular biology, genomics, and evolution. Norfolk, UK: Caister Academic Press, 2008: 484.
|
| [13] |
Gorham T, Jia Y, Shum CK et al. Ten-year survey of cyanobacterial blooms in Ohio's waterbodies using satellite remote sensing. Harmful Algae, 2017, 66: 13-19. DOI:10.1016/j.hal.2017.04.013 |
| [14] |
Su CD. Investigation on the exopolysaccharide from marine Cyanothece sp. 133[Dissertation]. Qingdao: Ocean University of China, 2005. [苏传东.蓝杆藻113菌株(Cyanothece sp.113)胞外多糖的研究[学位论文].青岛: 中国海洋大学, 2005. http://med.wanfangdata.com.cn/Paper/Detail?id=DegreePaper_Y989717 ]
|
| [15] |
Zhang YS, Li HY, Kong FX et al. Role of colony intercellular space in the Cyanobacteria bloom-forming. Environmental Science, 2011, 32(6): 1602-1607. [张永生, 李海英, 孔繁翔等. 群体细胞间空隙在微囊藻水华形成过程中的浮力调节作用. 环境科学, 2011, 32(6): 1602-1607. DOI:10.13227/j.hjkx.2011.06.002] |
| [16] |
Zhang M, Kong FX, Tan X et al. Biochemical, morphological, and genetic variations in Microcystis aeruginosa due to colony disaggregation. World Journal of Microbiology and Biotechnology, 2007, 23: 663-670. DOI:10.1007/s11274-006-9280-8 |
| [17] |
Balskus EP, Walsh CT. The genetic and molecular basis for sunscreen biosynthesis in Cyanobacteria. Science, 2010, 329: 1653-1656. DOI:10.1126/science.1193637 |
| [18] |
Kong FX, Ma HR, Gao JF et al. The theory and practice of prevention, forecast and warning on cyanobacteria bloom in Lake Taihu. J Lake Sci, 2009, 21(3): 314-328. [孔繁翔, 马荣华, 高俊峰等. 太湖蓝藻水华的预防、预测和预警的理论与实践. 湖泊科学, 2009, 21(3): 314-328. DOI:10.18307/2009.0302] |
| [19] |
Wang J, Zhou TY, Gao WC et al. Growth inhibition and recovery from low oxidation reduction potential to Microcystis aeruginosa. J Lake Sci, 2012, 24(4): 528-534. [王健, 周天艺, 高文程等. 低氧化还原电位对铜绿微囊藻(Microcystis aeruginosa)生长的抑制及恢复的影响. 湖泊科学, 2012, 24(4): 528-534. DOI:10.18307/2012.0404] |
| [20] |
Gan NQ, Wei N, Song LR. Recent progress in research of the biological function of microcystins. J Lake Sci, 2017, 29(1): 1-8. [甘南琴, 魏念, 宋立荣. 微囊藻毒素生物学功能研究进展. 湖泊科学, 2017, 29(1): 1-8. DOI:10.18307/2017.0101] |
| [21] |
Liu GF, Han SQ, Liu XZ et al. The environmental effects of algae bloom cluster:Impact on the antioxidant enzyme activities of water hyacinth (Eichharnia crassipes). J Lake Sci, 2016, 28(1): 31-39. [刘国锋, 韩士群, 刘学芝等. 藻华聚集的环境效应:对漂浮植物水葫芦(Eichharnia crassipes)抗氧化酶活性的影响. 湖泊科学, 2016, 28(1): 31-39. DOI:10.18307/2016.0104] |
| [22] |
Sun HJ, Lu K, Minter Ewan JA et al. Combined effects of ammonia and microcystin on survival, growth, antioxidant responses, and lipid peroxidation of bighead carp Hypophthalmythys nobilis larvae. Journal of Hazardous Materials, 2012, 221/222(4): 213-219. DOI:10.1016/j.jhazmat.2012.04.036 |
| [23] |
Yang Z, Zhang M, Shi XL et al. Nutrient reduction magnifies the impact of extreme weather on cyanobacterial bloom formation in large shallow Lake Taihu (China). Water Research, 2016, 103: 302-310. DOI:10.1016/j.watres.2016.07.047 |
| [24] |
Feng LJ, Liu SY, Wu WX et al. Dominant genera of cyanobacteria in Lake Taihu and their relationships with environmental factors. Journal of Microbiology, 2016, 54(7): 468-476. DOI:10.1007/s12275-016-6037-4 |
| [25] |
Li W, Qin BQ, Zhu GW. Forecasting short-term cyanobacterial blooms in Lake Taihu, China, using a coupled hydrodynamic-algal biomass model. Ecohydrology, 2014, 7(2): 794-802. DOI:10.1002/eco.1402 |
| [26] |
Zhang Y, Lin S, Qian X et al. Temporal and spatial variability of chlorophyll a concentration in Lake Taihu using MODIS time-series data. Hydrobiologia, 2011, 661(1): 235-250. DOI:10.1007/s10750-010-0528-9 |
| [27] |
Wu TF, Qin BQ, Brookes J et al. The influence of changes in wind patterns on the areal extension of surface cyanobacterial blooms in a large shallow lake in China. Science of the Total Environment, 2015, 518: 24-30. DOI:10.1016/j.scitotenv.2015.02.090 |
| [28] |
Shi K, Zhang Y, Zhou Y et al. Long-term MODIS observations of cyanobacterial dynamics in Lake Taihu:Responses to nutrient enrichment and meteorological factors. Scientific Reports, 2017, 7: 40326. DOI:10.1038/srep40326 |
| [29] |
Visser PM, Verspagen JMH, Sandrini G. How rising CO2 and global warming may stimulate harmful cyanobacterial blooms. Harmful Algae, 2016, 54: 145-159. DOI:10.1016/j.hal.2015.12.006 |
| [30] |
Paerl HW. Mitigating harmful cyanobacterial blooms in a human-and climatically-impacted world. Life, 2014, 4(4): 988-1012. DOI:10.3390/life4040988 |
| [31] |
Brown JH, Gillooly JF, Allen AP et al. Toward a metabolic theory of ecology. Ecology, 2004, 85(7): 1771-1789. DOI:10.1890/03-9000 |
| [32] |
Peeters F, Straile D, Lorke A et al. Earlier onset of the spring phytoplankton bloom in lakes of the temperate zone in a warmer climate. Global Change Biology, 2007, 13(9): 1898-1909. DOI:10.1111/j.1365-2486.2007.01412.x |
| [33] |
Wagner C, Adrian R. Cyanobacteria dominance:quantifying the effects of climate change. Limnology and Oceanography, 2009, 54: 2460-2468. DOI:10.4319/lo.2009.54.6_part_2.2460 |
| [34] |
Zeng J, Yang LY, Xiao L et al. Biogeochemical cycling of nitrogen in lakes and the role of microorganisms in conversion of nitrogen compounds. J Lake Sci, 2007, 19(4): 382-389. [曾巾, 杨柳燕, 肖琳等. 湖泊氮素生物地球化学循环及微生物的作用. 湖泊科学, 2007, 19(4): 382-389. DOI:10.18307/2007.0405] |
| [35] |
Wu YS, Yu GR. Purification of Dianchi Lake by radical submerged hydrophyte (Potamogeton crispus). Acta Scientiae Circumstantiae, 1991, 11(4): 411-416. [吴玉树, 余国荣. 根生沉水植物菹草(Potamogeton crispus)对滇池水体的净化作用. 环境科学学报, 1991, 11(4): 411-416.] |
| [36] |
Sun WH, Yu ZW, Yu SW. The harness of eutrophic water body by water-hyacinth. Acta Scientiae Circumstantiae, 1989, 9(2): 188-195. [孙文浩, 俞子文, 余叔文. 城市富营养化水域的生物治理和风眼莲抑制藻类生长的机理. 环境科学学报, 1989, 9(2): 188-195.] |
| [37] |
Li FM, Hu HY. Allelopathy and inhibitory effect of extracts from macrophytes on algae growth. China Water & Wastewater, 2004, 11: 18-21. [李锋民, 胡洪营. 大型水生植物浸出液对藻类的化感抑制作用. 中国给水排水, 2004, 11: 18-21.] |
| [38] |
Jin SD, Li YH, Ni CH et al. Uptake by Potamogeton crispus of nitrogen and phosphorus from water and some affecting factors. Acta Ecologica Sinic, 1994, 14(2): 168-173. [金送笛, 李永函, 倪彩虹等. 菹草对水中氮磷的吸收及若干影响因素. 生态学报, 1994, 14(2): 168-173. DOI:10.3321/j.issn:1000-0933.1994.02.019] |
| [39] |
Körner S. Loss of submerged macrophyte in shallow lakes in North-Eastern Germany. Int Rev Hydrobiol, 2002, 87: 375-384. DOI:10.1002/1522-2632(200207)87:4<375::AID-IROH375>3.0.CO;2-7 |
| [40] |
Best EPH, De Vries D, Reins A. The macrophyte in the Loosdrecht Lakes:A story of their decline in the course of eutrophication. VerhInt Verein Limnol, 1984, 22: 868-875. |
| [41] |
Guo HC, Wang XY, Yi X. Study on eutrophication control strategy based on the succession of water ecosystem in the Dianchi Lake. Geographical Research, 2013, 32(6): 998-1006. [郭怀成, 王心宇, 伊璇. 基于滇池水生态系统演替的富营养化控制策略. 地理研究, 2013, 32(6): 998-1006.] |
| [42] |
Qin BQ, Gao G, Zhu GW et al. Lake eutrophication and its ecosystem response. Chin Sci Bull, 2013, 58(10): 855-864. [秦伯强, 高光, 朱广伟等. 湖泊富营养化及其生态系统响应. 科学通报, 2013, 58(10): 855-864. DOI:10.1007/s11434-012-5560-x] |
| [43] |
Scheffer M, Hosper SH, Meijer ML et al. Alternative equilibria in shallow lakes. Trends in Ecology and Evolution, 1993, 8(8): 275-279. DOI:10.1016/0169-5347(93)90254-M |
| [44] |
Qin BQ. Progress and prospect on the eco-environmental research of Lake Taihu. J Lake Sci, 2009, 21(4): 445-455. [秦伯强. 太湖生态与环境若干问题的研究进展及其展望. 湖泊科学, 2009, 21(4): 445-455. DOI:10.18307/2009.0401] |
| [45] |
Chen XF. Investigation of the regional differences and nitrogenous cycling in China's lakes[Dissertation]. Nanjing: Nanjing University, 2012. [陈小锋.我国湖泊富营养化区域差异性调查及氮素循环研究[学位论文].南京: 南京大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10284-1014324130.htm ]
|
| [46] |
Ma JR, Qin BQ, Wu P. Controlling cyanobacterial blooms by managing nutrient ratio and limitation in a large hyper-eutrophic lake:Lake Taihu, China. Journal of Environmental Sciences, 2015, 27: 80-86. DOI:10.1016/j.jes.2014.05.042 |
| [47] |
Yamamoto Y, Shiah FK, Chen YL. Importance of large colony formation in bloom-forming cyanobacteria to dominate in eutrophic ponds. Ann Limnol-Int J Lim, 2011, 47: 167-173. DOI:10.1051/limn/2011013 |
| [48] |
Ma JR, Brookes JD, Qin BQ. Environmental factors controlling colony formation in blooms of the cyanobacteria Microcystis spp. in Lake Taihu, China. Harmful Algae, 2014, 31: 136-142. DOI:10.1016/j.hal.2013.10.016 |
| [49] |
Wilhelm SW, Farnsley SE, Lecleir GR. The relationships between nutrients, cyanobacterial toxins and the microbial community in Taihu (Lake Tai), China. Harmful Algae, 2011, 10(2): 207-215. DOI:10.1016/j.hal.2010.10.001 |
| [50] |
Xu H, Paerl HW, Qin BQ. Nitrogen and phosphorus inputs control phytoplankton growth in eutrophic Lake Taihu, China. Limnology and Oceanography, 2010, 55(1): 420-432. DOI:10.4319/lo.2010.55.1.0420 |
| [51] |
Chuai XM, Ding W, Chen XF et al. Phosphorus release from cyanobacterial blooms in Meiliang Bay of Lake Taihu, China. Ecological Engineering, 2011, 37(6): 842-849. DOI:10.1016/j.ecoleng.2011.01.001 |
| [52] |
Shi XL, Yang LY, Niu XJ et al. Intracellular phosphorus metabolism of Microcystis aeruginosa under various redox potential in darkness. Microbiological Research, 2003, 158(4): 345-352. DOI:10.1078/0944-5013-00214 |
| [53] |
Jiang LJ, Yang LY, Xiao L et al. Quantitative studies on phosphorus transference occuring between Microcystis aeruginosa and its attached bacterium (Pseudomonas sp.). Hydrobiologia, 2007, 581: 161-165. DOI:10.1007/s10750-006-0518-0 |
| [54] |
Yuan L, Zhu W, Xiao L et al. Phosphorus cycling between the colonial cyanobacterium Microcystis aeruginosa and attached bacteria, Pseudomonas. Aquatic Ecology, 2009, 43(4): 859-866. DOI:10.1007/s10452-008-9227-2 |
| [55] |
Zeng J, Yang LY, Li JY et al. Vertical distribution of bacterial community structure in the sediments of two eutrophic lakes revealed by denaturing gradient gel electrophoresis (DGGE) and multivariate analysis techniques. World Journal of Microbiology & Biotechnology, 2009, 25(2): 225-233. DOI:10.1007/s11274-008-9883-3 |
| [56] |
Zhao XQ, Yang LY, Yu ZY et al. Characterization of depth-related microbial communities in lake sediment by denaturing gradient gel electrophoresis of amplified 16S rRNA fragments. Journal of Environmental Sciences, 2008, 20(2): 224-230. DOI:10.1016/S1001-0742(08)60035-2 |
| [57] |
Zhang TX, Wang XR, Jin XC et al. Variations of alkaline phosphatase activity and P fractions in sediments of a shallow Chinese eutrophic lake (Lake Taihu). Environmental Pollution, 2007, 150(2): 288-294. DOI:10.1016/j.envpol.2007.01.007 |
| [58] |
Geng JJ, Niu XJ, Jin XC et al. Simultaneous monitoring of phosphine and of phosphorus species in Taihu Lake sediments and phosphine emission from lake sediments. Biogeochemistry, 2005, 76(2): 283-298. DOI:10.1007/s10533-005-5422-6 |
| [59] |
Niu XJ, Geng JJ, Wang XR et al. Temporal and spatial distributions of phosphine in Taihu Lake, China. Science of the Total Environment, 2004, 323(1/2/3): 169-178. DOI:10.1016/j.scitotenv.2003.10.017 |
| [60] |
Wang S, Qian X, Han BP et al. Effects of local climate and hydrological conditions on the thermal regime of a reservoir at Tropic of Cancer, in southern China. Water Research, 2012, 46(8): 2591-2604. DOI:10.1016/j.watres.2012.02.014 |
| [61] |
Zhang RB, Qian X, Li HM. Selection of optimal river water quality improvement programs using QUAL2K:A case study of Taihu Lake Basin, China. Science of the Total Environment, 2012, 431: 278-285. DOI:10.1016/j.scitotenv.2012.05.063 |
| [62] |
Zhu MY, Zhu GW, Zhao LL et al. Influence of algal bloom degradation on nutrient release at the sediment-water interface in Lake Taihu, China. Environmental Science and Pollution Research, 2013, 20(3): 1803-1811. DOI:10.1007/s11356-012-1084-9 |
| [63] |
Zhu W, Tan YQ, Wang RC et al. The trend of water quality variation and analysis in typical area of Lake Taihu, 2010-2017. J Lake Sci, 2018, 30(2): 296-305. [朱伟, 谈永琴, 王若辰等. 太湖典型区2010-2017年间水质变化趋势及异常分析. 湖泊科学, 2018, 30(2): 296-305. DOI:10.18307/2018.0202] |
| [64] |
Zhu MY, Zhu GW, Nurminen L et al. The influence of macrophytes on sediment resuspension and the effect of associated nutrients in a shallow and large lake (Lake Taihu, China). PLoS One, 2015, 10(6). DOI:10.1371/journal.pone.0127915 |
| [65] |
Chen XF, Chuai XM, Zeng J et al. Nitrogenous fluxes and its self-purification capacity in Lake Taihu. Environmental Science, 2012, 33(7): 2309-2314. [陈小锋, 揣小明, 曾巾等. 太湖氮素出入湖通量与自净能力研究. 环境科学, 2012, 33(7): 2309-2314. DOI:10.13227/j.hjkx.2012.07.032] |
| [66] |
Liu Z, Qian X, Gao HL et al. The effect of water transfer in the ecological restoration Zone of the Taihu Lake by the allocation of submerged community. Jiangsu Agricultural Sciences, 2016, 44(5): 480-483. [刘喆, 钱新, 高海龙等. 沉水植物群落配置对太湖贡湖生态修复区的调水效果. 江苏农业科学, 2016, 44(5): 480-483.] |
| [67] |
Schindler DW. Recent advances in the understanding and management of eutrophication. Limnology and Oceanography, 2006, 51: 356-363. DOI:10.4319/lo.2006.51.1_part_2.0356 |
| [68] |
Carpenter SR. Eutrophication of aquatic ecosystems:bistability and soil phosphorus. PNAS, 2005, 102: 1002-1005. DOI:10.1073/pnas.0503959102 |
| [69] |
Paerl HW, Scott JT, McCarthy MJ et al. It takes two to tango:When and where dual nutrient (N & P) reductions are needed to protect lakes and downstream ecosystems. Environmental Science & Technology, 2016, 50(20): 10805-10813. DOI:10.1021/acs.est.6b02575 |
| [70] |
Smith VH. Low nitrogen to phosphorus ratios favor dominance by blue-green algae in lake phytoplankton. Science, 1983, 221(4611): 669-671. DOI:10.1126/science.221.4611.669 |
| [71] |
Smith VH. Responses of estuarine and coastal marine phytoplankton to nitrogen and phosphorus enrichment. Limnology and Oceanography, 2006, 51: 377-384. DOI:10.4319/lo.2006.51.1_part_2.0377 |
 2019, Vol. 31
2019, Vol. 31 
