(2: 国家海洋环境监测中心, 大连 116023)
(3: 国家海洋局海域管理技术重点实验室, 大连 116023)
(4: 江西鄱阳湖南矶湿地国家级自然保护区管理局, 南昌 330038)
(5: 中国科学院大学, 北京 100049)
(2: National Marine Environmental Monitoring Center, Dalian 116023, P.R.China)
(3: Key Laboratory of Sea Field Management Technology, State Oceanic Administration, Dalian 116023, P.R.China)
(4: Nanji Wetland National Nature Reserve Agency, Nanchang 330038, P.R.China)
(5: University of Chinese Academy of Sciences, Beijing 100049, P.R.China)
湿地水鸟是指在生态上依赖于湿地栖息、取食、繁殖和越冬,即某一生活史阶段依赖于湿地,且在形态和行为上对湿地形成适应特征的鸟类[1].大多数水鸟是在全球范围内长距离迁徙的候鸟,是湿地生态系统的重要组分,对维护湿地生态系统平衡以及湿地物质和能量流动等方面起着非常关键的作用[2].迁徙水鸟往往栖息在湿地地区并形成大型水鸟集群,数量庞大水鸟群的取食和排泄活动对它们所栖息的湿地环境[3]和湿地植物有着十分深远的影响[4],特别是鸟类粪便为它们栖息的环境增加了大量外部营养来源[3, 5],它们会加速湿地食物网流动进程从而加快湿地碳、氮、磷的循环速率[6].然而,关于湿地水鸟在这方面的定量研究并不多见.
湿地鸟类粪便营养物的加入会导致湿地植物枯落物分解和养分释放过程的变化[7],从而影响新生湿地植物有效营养物的数量[8],然后通过影响植物的萌发、生长、物种的丰度和地上生物量来影响植物群落的构建和种群间对繁殖地的竞争[9].而植物枯落物分解是调控湿地养分生物地球化学循环的关键环节,也是维持湿地生态系统能量流动、物质循环和养分平衡的重要生态过程[10].但是目前关于湿地枯落物分解的研究主要集中在分解过程中物质组分变化速率[11-12]、元素释放动态[12-14]以及对全球变化的响应[15]等方面.关于湿地植物枯落物分解调控机制的研究大部分也只涉及到植物群落类型、枯落物本身的理化质量特征[16]、分解环境中的水文状况[17-18]、温度状况、微生物状况[19]等条件,只有极少数的研究涉及到水鸟粪便对湿地植物分解过程的影响[7],关于水鸟粪便在湿地植物枯落物分解过程中的作用还知之甚少.
鄱阳湖湿地是东亚—澳大利亚西亚候鸟迁飞路线上最重要的越冬地,是多种候鸟迁徙的必经之路与重要栖息地[20-21].水鸟调查数据表明,每年在鄱阳湖越冬的水鸟平均在40万只以上[22],其中植食性雁鸭类的种类多,数量也是越冬水鸟中最大的,约占越冬候鸟总数的50 %以上[23].数量庞大的水鸟在鄱阳湖湿地进行取食、排泄以及栖息等越冬活动,每年冬天都会向湿地洲滩排泄大量的粪便.这些粪便在鄱阳湖湿地洲滩上分解过程有怎样的特征?鸟粪的加入对湿地洲滩植物枯落物的分解过程又有什么样的影响?这些十分值得研究的问题在鄱阳湖湿地中的研究还比较罕见.然而,研究越冬的植食水鸟对湿地碳、氮、磷生物地球化学循环过程的影响具有重要的科学理论意义,对鄱阳湖湿地乃至长江中下游流域湖泊湿地保护与管理实践具有重要的实际意义.
因此,本文的目的是:1)研究植食水鸟粪便分解过程和鄱阳湖湿地洲滩薹草分解过程的差异及碳、氮、磷释放动态特征;2)研究植食水鸟粪便的加入对鄱阳湖湿地薹草枯落物分解过程的影响.
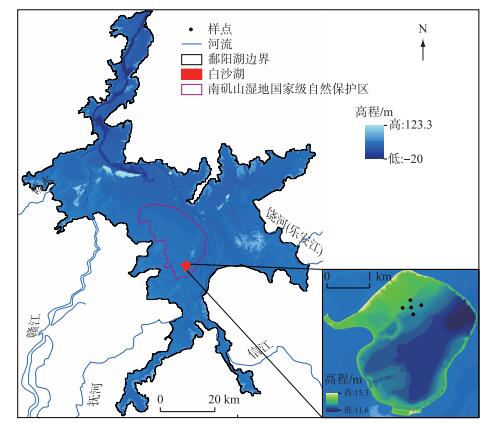
1 材料和方法 1.1 研究区域概况本研究区域分布在鄱阳湖湿地的南矶山湿地国家级自然保护区典型的碟形湖泊白沙湖内(图 1).保护区位于鄱阳湖主湖区南部,地处赣江北支、中支和南支汇入鄱阳湖开放水域冲积形成的三角洲前缘,海拔在12~16 m(吴淞)之间[24].属亚热带暖湿型季风气候,夏季炎热多雨,冬季低温少雨.受鄱阳湖季节性周期性水文变化的影响,保护区内有明显的丰水期和枯水期.丰水期内(4—9月),保护区除总面积不足4 km2的南山岛和矶山岛两个人居岛屿外其他草洲均被洪水淹没,处于典型的湖相水文状态.枯水期内(10月至次年3月)湖水消退归入河道和一些碟形洼地,区内大小河流纵横,碟形湖泊星罗棋布,不同高程洲滩相继出露,整个三角洲地区呈现河、湖、洲交错的景观[24].这种特殊的水文节律使得保护区内形成了大量土壤肥沃、水热条件充裕的洲滩和浅滩,发育了丰富的湿生植物和水生植物,多样性极其丰富,其中以薹草(Carex cinerascens)、南荻(Triarrhena lutarioriparia)、芦苇(Phragmites australis)等为优势种[25].薹草是鄱阳湖湿地草洲分布面积最广的湿生植物,也是鄱阳湖湿地的优势植物,分布遍及从湖岸到湖心水线之间全部洲滩[25],因此本研究将灰化薹草作为洲滩湿地植物的代表.每年9月水退后薹草“秋草”在洲滩上萌生,一直生长到12月至次年3月,冬季地上部分逐渐开始枯萎分解;1月份过后在“秋草”尚未全部死亡之前薹草“春草”再次萌生,一直生长到4月才逐渐被湖水淹没,然后在水下休眠、死亡直至地上部分全部分解消失[26].这种特殊的情况为多种越冬珍禽和水鸟提供了良好的栖息地和食物来源,使得鄱阳湖湿地成为亚洲最重要的珍禽越冬场所,被誉为“白鹤王国”和“候鸟乐园”.因此,鄱阳湖湿地是开展本研究的绝佳天然试验场.
|
图 1 样点在鄱阳湖湿地中的位置 Fig.1 Position of sampling area in Lake Poyang Wetland |
本研究于2017年1月下旬在调查湿地植物和水鸟栖息地分布规律的基础上,在白沙湖内选择人为干扰相对较少、植食性水鸟集聚频率较高的、鸟粪分布密集、植物群落发育良好的离湖心水线约200 m的洲滩建立5块固定试验样地,样地中间约间隔50 m,样地内的优势植物为灰化薹草(Carex cinerascens Kükenth),盖度在80 % ~90 %之间,高度为40~60 cm,薹草根部周围的土壤上或者薹草植株上分布有许多鸟粪.在每个样地内选取一个点作为本次分解时间实验的5个重复样点(图 1).
分解模拟实验采用分解袋法.选择100目(孔径为0.15 mm)、规格为15 cm×20 cm的白色网孔的尼龙网袋作为分解袋.这种网袋既能够避免分解袋中分解残体的非分解损失,也能保证分解作用不限制.在所设样地附近小范围收割衰老薹草的叶片带回实验室用去离子水冲洗干净,剪成10 cm长小段后混合均匀(消除尺寸对分解的影响)装入牛皮纸信封内,置于烘箱120℃杀青1 h后再60℃烘干至恒重.同时在研究样地内收集新鲜的越冬雁类粪便(排泄在24 h内,以下简称鸟粪),分批装入牛皮纸信封内,置于60℃烘箱内烘至恒重.分别取10.00 g烘干的6个样品重复测量其初始养分含量(表 1).再将剩下的样品称量10 g分别装入尼龙网袋中.分解袋内的样品有3种形式:第1种形式是只装10 g烘干的鸟粪,第2种形式是只装10 g烘干的薹草枯落物样品,第3种形式是装有5 g烘干鸟粪和5 g烘干薹草枯落物的样品(以下简称薹草+鸟粪).将制作好的105个分解袋带到样地用PVC管固定在预先设置的5个样点上,每个样点各放置7个3种不同形式的样品袋(不破坏地表原有枯落物结构),将样品袋用短绳绑在插入泥土中的PVC管底部可以保证每个样品袋都充分地接触地表且相互不挤压.分别于实验开始后第5、15、30、60、90、120和150天从各样点取回分解袋.试验终止于6月是因为洪水淹没了样地, 改变了分解环境的水文条件.
| 表 1 薹草枯落物和鸟粪样品初始养分含量 Tab. 1 Abundances of C, N, P in initial Carex litter and birds' droppings |
将取回的分解袋带回实验室,除去泥土、藻类以及吸附物等杂物,再将薹草+鸟粪样品袋中的薹草残留物单独挑出作为一类样品,然后将所有样品装到有编号的牛皮信封中,置于60℃烘箱中烘干至恒重,称量其残余干物质质量后用球磨仪器将样品碾成粒径为0.06 μm的粉末,然后分别密封于有编号的聚乙烯样品袋中待测.样品全碳(TC)和全氮(TN)含量使用元素分析仪(Vario Max CN Analyzer, Elementar Analysensysteme GmbH, Germany)测定;全磷(TP)使用电感耦合等离子体发射光谱仪(Inductively Coupled Plasma Optical Emission Spectrometer(ICP-OES), Optima 5300DV, Perkin-Elmer, America)测定.
1.3 数据处理与统计分析干物质损失率(the percentage of dry mass loss, Lt)计算公式为[13]:
| $ {L_t} = \frac{{{M_0} - {M_t}}}{{{M_0}}} \times 100\% $ | (1) |
式中,Lt表示时间t时枯落物的损失率,Mt表示时间t时枯落物干物质重量,M0表示初始干物质重量,t为枯落物分解进行的时间(下文中含义相同).
干物质残留率(the dry mass remaining, rt)计算公式为:
| $ {r_t} = 100 - {L_t} $ | (2) |
干物质瞬时分解速率(the instantaneous loss rate of dry mass, k)用Olson负指数衰减模型[27]计算:
| $ {M_t} = {M_0}{{\rm{e}}^{ - kt}} $ | (3) |
式中,k值越大表示枯落物的分解速度越快(下文中含义相同).
干物质残余率(y)用负指数衰减模型[28]Levenberg Marquardt算法进行模拟:
| $ y = a \cdot {{\rm{e}}^{ - kt}} $ | (4) |
式中,y为枯落物残留率,a为拟合参数,e为自然底数.
相对养分归还指数(relative return index,RRI)计算公式为[13]:
| $ RR{I_t} = \frac{{{M_0} \cdot {C_0} - {M_t} \cdot {C_t}}}{{{M_0} \cdot {C_0}}} \times 100\% $ | (5) |
式中,Ct为t时刻枯落物中某元素的浓度,C0为枯落物中某元素的初始浓度.用CRRI表示碳的相对归还指数(carbon relative return index),NRRI表示氮的相对归还指数(nitrogen relative return index),用PRRI表示磷的相对归还指数(phosphorus relative return index).当RRI为正数时表示枯落物分解过程中元素发生了净释放,当RRI为负数时则表示发生了净积累.
数据使用Excel 2016统计分析,用Origin9.0制图,在SPSS 19.0软件中进行单因素方差分析(ANOVA)和LSD多重比较的差异显著性检验.
2 结果与分析 2.1 3种样品干物质损失率、残留率和分解速率的分异特征分解时间对薹草枯落物干物质损失率的影响十分显著(F=102.931,P < 0.0001, 组间df=6,组内df=98),薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品干物质损失率都随分解天数的增加而逐渐增大(表 2).
| 表 2 薹草枯落物、薹草+鸟粪中薹草和鸟粪样品分解过程中干物质损失率的动态变化 Tab. 2 Dynamics of the percentage of dry mass loss during decomposition progress |
分解5~150天薹草枯落物、薹草+鸟粪中薹草和鸟粪的干物质损失率具有极显著的差异性(5天:F=35.179,P < 0.0001;15天:F=21.930,P < 0.0001;30天:F=63.261,P < 0.0001;60天:F=7.869,P < 0.005;90天:F=26.354,P < 0.0001;120天:F=34.880,P < 0.0001;15天:F=27.309,P < 0.0001).在分解的每个阶段总是薹草+鸟粪中薹草损失率最高,薹草样品次之,鸟粪样品损失率最小.分解150天后薹草+鸟粪中薹草、薹草和鸟粪的干物质损失率依次为34.40 %、29.64 %和26.20 % (表 2).
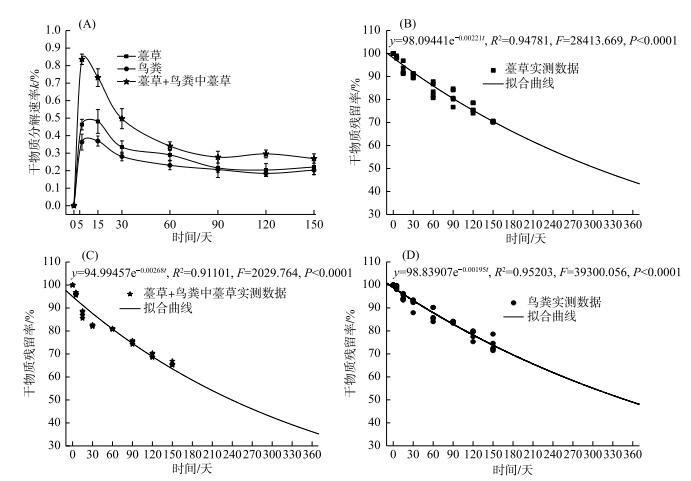
通过Olson负指数衰减模型计算出每个分解时间点的瞬时衰减系数k,结果表明:不同的分解时间对薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品分解速率的影响极其显著(F=9.634,P < 0.0001).瞬时衰减系数都表现出0~15天内先快速增加至最大值,其最大值分别为0.48、0.88和0.37,在30~60天内瞬时衰减系数都快速减小,60~150天内十分缓慢地减小直至稳定.统计检验发现3种样品之间的瞬时衰减系数在0~150天内的差异性极为显著(5天:F=35.660,P < 0.0001;15天:F=22.271,P < 0.0001;30天:F=68.244,P < 0.0001;60天:F=8.807,P=0.006;90天:F=27.215,P < 0.0001;120天:F=37.234,P < 0.0001;150天:F=30.949,P < 0.0001).此外,在每个分解时间点上瞬时衰减系数都是薹草+鸟粪中薹草最高,薹草样品次之,鸟粪样品最小(图 2A).
|
图 2 薹草枯落物、薹草+鸟粪中薹草和鸟粪样品分解速率(A)和干物质损失率(B、C和D)动态 Fig.2 Dynamics of decay rate (A) and the percentage of dry mass loss(B, C and D) during decomposition progress |
将实测数据计算出来的干物质残留率用Olson负指数衰减模型的Levenberg Marquardt算法进行拟合,发现拟合效果非常好,拟合系数R2均在0.90以上,拟合方程的各参数如图 2B、C、D与表 3所示.通过拟合方程预测出薹草枯落物、薹草+鸟粪中薹草和鸟粪样品分解完成50 %所需的时间大约依次为314、259和355天,分解完成95 %所需的时间依次为1356天(约3.7年)、1118天(约3.1年)和1536天(约4.2年),并且3种样品的平均分解速率差异极显著(P < 0.0001),分别为0.00221、0.00268和0.00195.
| 表 3 薹草枯落物、薹草+鸟粪中薹草和鸟粪样品分解过程Olson时间衰减模型拟合* Tab. 3 Fitting parameters of Olson decay model for samples during decomposition progress |
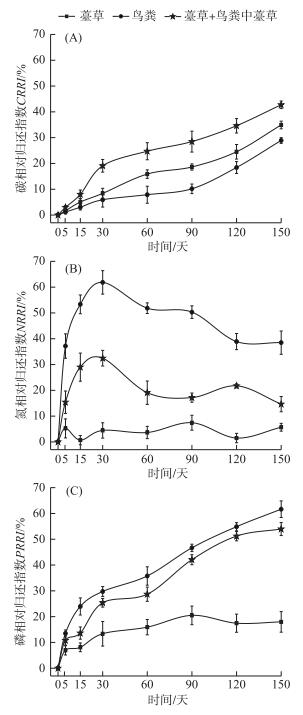
在整个分解过程中薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品的碳、氮、磷元素都表现为净释放模式(RRI>0;图 3),未出现积累的情况.分解0~150天3种样品的CRRI值差异性并不显著(P>0.005),但是每个分解阶段薹草+鸟粪样品中薹草的CRRI值最高,薹草样品次之,鸟粪样品最小.随着时间的推移CRRI持续增大.到第150天时薹草+鸟粪中薹草、薹草和鸟粪3种样品的CRRI值次约为42.73 %、34.91 %和28.90 % (图 3A).
|
图 3 3种样品分解过程中碳(A)、氮(N)和磷(C)相对归还指数动态 Fig.3 Variations of CRRI(A), NRRI(B) and PRRI(C) during decomposition progress |
分解0~150天3种样品的NRRI值差异性极其显著(F为17.316~56.662,P < 0.005).每个分解时间点的NRRI值均为鸟粪样品最高,薹草+鸟粪中薹草次之,薹草样品最小.但是随着时间的推移NRRI值并不是一直都升高,而是波动起伏的.薹草的样品的NRRI值变化幅度很小,最大值只有7.44 %,并且一直处于小范围波动状态;薹草+鸟粪中薹草和鸟粪样品的NRRI值在0~30天内快速升高至最大值,而后再缓慢减小,最大值分别出现在薹草+鸟粪中薹草样品(32.45 %)和鸟粪样品(61.84 %),中间也偶尔有较小的起伏(图 3B).
分解0~60天3种样品的PRRI值差异性并不显著(P>0.005),但是90~150天其差异性非常显著(F为8.992~38.223,P < 0.05).每个分解阶段PRRI值都是鸟粪样品最高,薹草+鸟粪中薹草次之,薹草样品最小.薹草+鸟粪中薹草和鸟粪样品的PRRI值相差不大,但是都比薹草的要高出很多.随着时间的推移3种样品的PRRI都持续升高,直到第150天时鸟粪、薹草+鸟粪中薹草和薹草样品的PRRI值分别为61.63 %、53.95 %和17.96 % (图 3C).
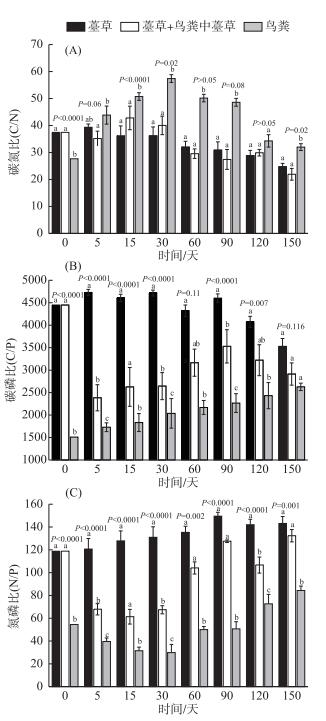
2.3 3种样品碳、氮、磷化学计量学分异特征薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品的化学计量学性状动态变化十分明显(图 4).总的来看,在分解的起始阶段,不同样品的碳氮比值(C/N)大小为:鸟粪样品(约27.68) < 薹草样品(约37.46)=薹草+鸟粪中薹草(约37.46).随着分解的进行,在5~150天内鸟粪的C/N比一直比其他两种样品高很多,而分解5~50天左右薹草+鸟粪中薹草的C/N一直高于薹草样品的,但从60天以后,薹草的C/N就一直高于薹草+鸟粪中薹草的.从样品种类来看,薹草样品的C/N在分解开始的前5天有小幅度的先上升后缓慢下降趋势,到第150天时下降至24.71,比初始值低约34.03 %;薹草+鸟粪中薹草的C/N在0~5天内迅速小幅度下降后又迅速升高,在第15天时达到最大值(约42.81),而后逐渐缓慢下降,到第150天时下降到21.92,比初始值低约36.94 %;鸟粪样品的C/N在0~30天持续升高到最大值(约71.17),然后持续下降,到第150天时变为31.99,仍然比初始值高约15.57 % (图 4A).
|
图 4 样品分解过程中碳、氮、磷的化学计量比动态 Fig.4 Variations of C/N(A), C/P(B) and N/P(C) during decomposition progress |
3种样品的碳磷比值(C/P)在0~90天内存在十分显著的差异性(P < 0.0001).在分解的起始阶段,不同样品的C/P为鸟粪样品(约1509) < 薹草样品(约4441)=薹草+鸟粪中薹草样品(约4441).在分解后的5~150天内三者的关系一直保持为鸟粪样品 < 薹草+鸟粪中薹草样品 < 薹草样品.薹草样品的C/P虽在局部有起伏,但总体呈缓慢下降趋势,到第150天时比初始值低约20.56 %;薹草+鸟粪中薹草的C/P在0~5天迅速下降至最小值(约2385),之后在5~90天内缓慢上升至最大值(3529),但仍未超过初始值,之后又缓慢下降至2913;鸟粪样品的C/P呈逐渐缓慢升高的趋势,到第150天升高了约70.09 % (图 4B).
3种样品的氮磷比值(N/P)在0~150天内都存在十分显著的差异性(P < 0.0001).在分解的起始阶段,不同样品的C/P为鸟粪样品(约54.51) < 薹草样品(约118.56)=薹草+鸟粪中薹草(约118.56).在分解后的5~150天内三者的关系也一直是鸟粪样品 < 薹草+鸟粪中薹草 < 薹草样品.薹草样品N/P从分解一开始就总体呈缓慢上升趋势,到第90天时达到最大值(约149.50),增幅约为25.86 %,之后逐渐缓慢下降,到第150天时其值约为143.14;薹草+鸟粪中薹草N/P在前15天一直下降到最小值(约61.31),之后快速上升,在第150天时达到最大值(132.39),比初始值增加了约11.46 %;鸟粪样品的N/P一开始呈逐渐缓慢下降的趋势,到第30天时达到最小值(29.85),降幅约为45.24 %,之后又快速地上升,到第150天时已上升至84.34,比初始值高54.72 % (图 4C).
3 讨论 3.1 鸟粪的添加对湿地优势植物薹草枯落物分解过程的影响本研究结果表明不同的分解时间段内薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品的干物质损失率和分解速率的差异性都十分显著(P < 0.001).干物质损失率都是随着分解时间的增加而不断升高,而分解速率在分解的前0~15天内急速升高到最大值后开始缓慢降低至趋于稳定.这与大多数湿地枯落物的分解过程是一致的[7, 11, 16].这可能是由于湿地环境中水分比较充足,使得分解前期3种样品中的可溶解成分快速淋溶,水溶成分和非木质素碳水化合物优先分解,且分解速率非常快[12],而分解中后期已木质化的未分解碳水化合物与原有木质素在微生物作用下同时降解,这个过程就比较缓慢,直到最后木质素含量趋于稳定,残余物质逐渐腐殖化,分解速率较小且几乎不变[29].
本研究结果还表明,鸟粪添加对薹草枯落物分解过程有很大的影响,无论是干物质损失率还是分解速率在3种样品之间都有非常显著的差异性.在整个分解过程中二者数值都表现为薹草+鸟粪中薹草样品>薹草样品>鸟粪样品,用模型模拟也得到了相同的结果(表 3).这说明鸟粪添加改变了枯落物的成分,能够加速薹草枯落物的分解进程.这与Lee等[7]在水稻田开展的控制试验研究结果类似,他们发现添加80 g鸟粪处理水稻秸秆的分解率显著高于添加40 g鸟粪处理,而添加40 g鸟粪处理的分解速率又高于对照组(未添加鸟粪)的.这可能是由于水鸟粪便的加入增加了额外的营养物质, 对薹草枯落物的分解产生了积极的刺激作用[8],这种刺激作用又进一步增加了分解环境中有效养分的供应.分解环境中养分供应会影响异养分解者对营养物质的可获得性,通常被认为是控制分解速率的一个重要因素[30].一般情况下,枯落物分解过程中,枯落物营养含量不足以满足异养生物分解者活动对营养物质的需求量[31].所以本研究推测鸟粪添加一方面给分解环境中带来额外的营养物质可能成为了枯落物中微生物分解者的重要营养补给,使薹草+鸟粪样品中分解者微生物的数量、种类以及活性增强.另一方面,可能是鸟粪的增加刺激产生了一系列降解酶,如木质素酶、纤维素酶、蔗糖酶等, 胞外酶数量和活性增加,从而导致出苔草+鸟粪样品中的苔草分解速率更高.
薹草枯落物的分解速率高于鸟粪可能与分解过程C/N变化有关.在湿地环境中,C/N一般被认为是表征分解速率的最重要指标[12],大量研究表明C/N较高的枯落物分解速率较低[13, 16-17].本研究中,在分解的起始阶段,鸟粪样品的C/N比薹草样品的低,但是随着分解的进行,在5~150天内鸟粪样品的C/N一直比薹草样品的要高出很多(图 4A),直接减缓了鸟粪的分解速率.在C/N>30的时候,N将成为分解过程中的限制性因素,微生物分解活动也会因C/N的增高而变慢[32].这个现象的另外一个原因可能是水鸟在取食薹草后将一些易分解的成分消化利用,将难分解的成分留在鸟粪之中,不过这个原因有待进一步研究验证.
3.2 鸟粪添加对湿地优势植物薹草枯落物分解过程中碳、氮、磷释放的影响本研究结果表明,薹草枯落物、薹草+鸟粪中薹草和鸟粪3种样品分解过程中碳、氮、磷的释放动态差异非常明显,并且在整个分解阶段都表现为净释放模式.在整个分解过程中,3种样品的CRRI值都持续升高,并且表现为薹草+鸟粪中薹草样品>薹草样品>鸟粪样品(图 3A);NRRI值是高低波动起伏的,并且整体表现为鸟粪样品>薹草+鸟粪中薹草样品>薹草样品(图 3B);PRRI均持续升高,并且整体表现为鸟粪样品>薹草+鸟粪中薹草样品>薹草样品(图 3C).这与Zhao等[13]在滨海湿地、Sun等[17]在三江平原沼泽湿地、Lan等[16]在白洋淀湿地以及张广帅等[14]在鄱阳湖湿地枯落物分解中养分释放动态模式相似.
一般情况下,碳归还指数变化整体包含快速增加和缓慢增加两个过程[13].在淋溶过程中溶解性碳水化合物快速发生淋溶,碳归还指数会快速升高[16],后面受外部环境因子的激发作用或者外源营养元素输入的影响,分解速率加快,土壤微生物数量变多、活力增强,分解残留物中剩余木质素、纤维素和单宁等难分解物质开始逐渐被微生物所利用,此时碳归还指数的增加速度开始减缓甚至开始降低[12].前文已经叙及鸟粪的加入促进了薹草枯落物的分解,这可能是造成薹草+鸟粪中薹草C释放速度比薹草枯落物高的关键原因.
然而,在本研究中对于氮归还指数来说,在整个分解过程中并不是一直呈升高的趋势,而是有升有降,但整体表现为净释放模式.尽管在淋溶过程中氮会由于含氮盐的流失而快速减少,但是氮素多以复杂且不易被淋溶的大分子蛋白质存在,并且其分解主要受微生物的影响,微生物在分解这些大分子蛋白质时对氮需求的增加会导致氮固定,氮的归还指数升高会减缓甚至会大幅下降[33],微生物固氮作用是分解过程中氮元素积累的主要原因[34].可能由于鸟粪结构比较松散,可溶性氮含量较高,容易受湿地水分淋溶的影响,所以鸟粪样品氮的释放速度一直比其他两种样品要快,并且这种N淋溶的速度远远抵消了薹草分解速率较快所增加的氮释放量.但是薹草+鸟粪中薹草氮的释放速度比薹草枯落物高很多可能主要还是分解速率较高造成的.
磷的归还变化受物理和生物双重因素的影响,分解初期磷的淋溶作用比较强,分解残留物中磷归还速度非常高,当释放到一定程度时,归还速度就趋于稳定[35],这可能是因为在植物组织中的磷主要以磷酸根或化合物的形式存在而容易发生淋溶损失.而分解后期微生物降解过程中,当微生物的营养需求不受磷限制时,过量的磷会限制微生物的活性[8, 36].鸟粪中磷的含量远远高于薹草枯落物中磷的含量,但是鸟粪结构十分松散,磷的淋溶流失速率远远要高于薹草枯落物的,所以分解速率所带来的磷释放的增加量已经被快速的淋溶量所抵消,因此造成了鸟粪的PRRI值比薹草枯落物的要高很多的现象.但是薹草+鸟粪中薹草磷的释放速度比薹草枯落物高还可能仍然是由分解速率较高引起的.
4 结论在鄱阳湖湿地枯水期植食越冬候鸟粪便和典型湿地植物薹草枯落物模拟分解试验得到以下结论:
1) 鄱阳湖湿地枯水期植食越冬候鸟粪便的加入对典型湿地植物枯落物的分解有显著促进作用,分解150天后薹草+鸟粪中薹草、薹草和鸟粪样品干物质损失率依次为34.40 %、29.64 %和26.20 %. Olson负指数衰减模型得出鸟粪的加入使薹草的平均分解速率提升了21.23 %左右.本研究推测鸟粪添加给分解环境带来额外的营养物质,使分解者微生物数量、种类、活性增加以及鸟粪刺激产生了一系列降解酶,如木质素酶、纤维素酶、蔗糖酶等, 胞外酶数量和活性增加,是鸟粪促进薹草分解的关键因素,而样品中初始养分含量以及分解过程碳、氮、磷化学计量比的变化是造成其分解速率和养分释放显著性差异的主要原因.
2) Olson负指数衰减模型的Levenberg Marquardt算法能很好地拟合3种样品的分解过程,拟合系数R2均在0.90以上.通过该模型预测显示,在分解水文条件不变的情况下薹草+鸟粪中薹草、薹草枯落物和鸟粪样品分解完成50 %所需的时间分别为259、314和355天左右,分解完成95 %所需的时间依次约为3.1、3.7和4.2年.
3) 薹草+鸟粪中薹草、薹草枯落物和鸟粪样品分解过程中的碳、氮、磷都表现为净释放模式,随着分解过程的进行RRI整体在持续升高,并且其养分的RRIs之间差异也十分显著. CRRI值表现为薹草+鸟粪中薹草>薹草>鸟粪,NRRI和PRRI值均表现为鸟粪>薹草+鸟粪中薹草>薹草.本研究推测样品中的初始养分含量以及分解过程碳、氮、磷化学计量比的变化是造成其分解速率和养分释放差异显著的重要原因.
致谢: 感谢江西鄱阳湖南矶湿地国家级自然保护区管理局及相关工作人员对本研究野外工作的配合与支持;感谢南昌大学生命科学研究院流域生态学研究所的金松斌老师、兰志春博士、沈瑞昌博士在室内试验中提供的便利与帮助;感谢南昌大学张欢老师、孟竹剑同学、吴申浩同学和王鑫同学、江西师范大学研究生饶滴滴同学在野外样地布设、取样以及作图过程中的帮助;感谢荷兰瓦格宁根大学(Wageningen University and Research)窦月含博士对英文摘要的润色修改.
| [1] |
Nisbet ICT. Waterbird population estimates: fourth edition. Waterbirds, 2013, 31(1): 152-153. |
| [2] |
Sekercioglu CH. Increasing awareness of avian ecological function. Trends in Ecology & Evolution, 2006, 21(8): 464-471. |
| [3] |
Manny BA, Johnson WC, Wetzel RG. Nutrient additions by waterfowl to lakes and reservoirs: Predicting their effects on productivity and water quality. Hydrobiologia, 1994, 279/280(1): 121-132. DOI:10.1007/BF00027847 |
| [4] |
Tomassen HBM, Smolders AJP, Lamers LPM et al. How bird droppings can affect the vegetation composition of ombrotrophic bogs. Canadian Journal of Botany, 2005, 83(8): 1046-1056. DOI:10.1139/b05-051 |
| [5] |
Chaichana RRL, Moss B. Birds as eutrophicating agents: a nutrient budget for a small lake in a protected area. Hydrobiologia, 2010, 646(1): 111-121. DOI:10.1007/s10750-010-0166-2 |
| [6] |
Bauer HSS, Klaassen M. Quantification of allochthonous nutrient input into freshwater bodies by herbivorous waterbirds. Freshwater Biology, 2010, 53(1): 181-193. |
| [7] |
Lee GM, Kim HT, Kim JG. Effects of wintering waterfowl's feces on nutrient dynamics of paddy fields and rice growth. Journal of Ecology & Environment, 2012, 35(4): 291-299. |
| [8] |
Elwood J, Newbold J, Trimble A et al. Limiting role of phosphorus in a woodland stream ecosystem: Effects of P enrichment on leaf decomposition and primary producers. Ecology, 1981, 62(1): 146-158. DOI:10.2307/1936678 |
| [9] |
Xiong SJ, Nilsson C. The effects of plant litter on vegetation: a meta-analysis. Journal of Ecology, 1999, 87(6): 984-994. DOI:10.1046/j.1365-2745.1999.00414.x |
| [10] |
Mitsch WJ, Gosselink JG. Wetlands: 5th edition. United States: John Wiley & Sons, Inc, 2015.
|
| [11] |
Zhang GW, Yu XB, Gao Y et al. Effects of water table on cellulose and lignin degradation of Carex cinerascens in a large seasonal floodplain. Journal of Freshwater Ecology, 2018, 33(1): 311-325. DOI:10.1080/02705060.2018.1459324 |
| [12] |
Iii SED, Corronado-Molina C, Childers DL et al. Temporally dependent C, N, and P dynamics associated with the decay of Rhizophora mangle L. leaf litter in oligotrophic mangrove wetlands of the southern everglades. Aquatic Botany, 2003, 75(3): 199-215. DOI:10.1016/S0304-3770(02)00176-6 |
| [13] |
Zhao QQ, Bai JH, Liu PP et al. Decomposition and carbon and nitrogen dynamics of Phragmites australis litter as affected by flooding periods in coastal wetlands. Clean-Soil, Air, Water, 2015, 43(3): 441-445. DOI:10.1002/clen.v43.3 |
| [14] |
Zhang GS, Yu XB, Liu Y et al. Accumulation effect of litter decomposition and water level on carbon and nitrogen in shallow lake water of Lake Poyang. J Lake Sci, 2018, 30(3): 668-679. [张广帅, 于秀波, 刘宇等. 鄱阳湖碟形湖泊植物分解和水位变化对水体碳、氮浓度的叠加效应. 湖泊科学, 2018, 30(3): 668-679. DOI:10.18307/2018.0309] |
| [15] |
Peter M, Schile-Beers LM, Mozdzer TJ et al. Global-change effects on early-stage decomposition processes in Tidal Wetlands-Implications from a global survey using standardized litter. Biogeosciences, 2018, 15(10): 3189-3202. DOI:10.5194/bg-15-3189-2018 |
| [16] |
Lan Y, Cui BS, You ZY et al. Litter decomposition of six macrophytes in a eutrophic shallow lake (Baiyangdian Lake, China). Clean-Soil, Air, Water, 2012, 40(10): 1159-1166. DOI:10.1002/clen.201200056 |
| [17] |
Sun ZG, Mou XJ, Liu JS. Effects of flooding regimes on the decomposition and nutrient dynamics of Calamagrostis angustifolia litter in the Sanjiang Plain of China. Environmental Earth Sciences, 2012, 66(8): 2235-2246. DOI:10.1007/s12665-011-1444-7 |
| [18] |
Langhans SD, Tockner K. The role of timing, duration, and frequency of inundation in controlling leaf litter decomposition in a river-floodplain ecosystem (Tagliamento, Northeastern Italy). Oecologia, 2006, 147(3): 501-509. DOI:10.1007/s00442-005-0282-2 |
| [19] |
Verónica F, Chauvet E. Synergistic effects of water temperature and dissolved nutrients on litter decomposition and associated fungi. Global Change Biology, 2011, 17(1): 551-564. DOI:10.1111/gcb.2010.17.issue-1 |
| [20] |
Ding XS. Protection and use of ecotourism resource of Poyang Lake Nature Reserve. Jiangxi Forestry Science and Technology, 2003, 30(6): 30-34. [丁贤生. 鄱阳湖自然保护区湿地生态旅游资源的保护与利用. 江西林业科技, 2003, 30(6): 30-34. DOI:10.3969/j.issn.1006-2505.2003.06.013] |
| [21] |
Xia SX, Liu GH, Yu XB et al. Importance assessment of wintering habitats for migratory waterfowl in Lake Poyang. J Lake Sci, 2015, 27(4): 719-726. [夏少霞, 刘观华, 于秀波等. 鄱阳湖越冬水鸟栖息地评价. 湖泊科学, 2015, 27(4): 719-726. DOI:10.18307/2015.0421] |
| [22] |
Li FS. Ecological study on wetlands and waterbirds in Poyang Lake. Beijing: Popular Science Press, 2011. [李凤山. 鄱阳湖湿地和水鸟的生态研究. 北京: 科学普及出版社, 2011.]
|
| [23] |
Tu YG, Yu CH, Huang XF et al. Distribution and population of the overwintering anatidae waterfowl in the Poyang Lake. Acta Agriculturae Universitatis Jiangxiensis, 2009, 31(4): 760-764. [涂业苟, 俞长好, 黄晓凤等. 鄱阳湖区域越冬雁鸭类分布与数量. 江西农业大学学报, 2009, 31(4): 760-764. DOI:10.3969/j.issn.1000-2286.2009.04.035] |
| [24] |
Liu XZ, Hu BH. Comprehensive and scientific survey of Jiangxi Nanjishan Wetland Nature Reserve. Beijing: China Forestry Publishing House, 2005. [刘信中, 胡斌华. 江西南矶山湿地自然保护区综合科学考察. 北京: 中国林业出版社, 2005.]
|
| [25] |
Zhang QJ, Yu XB, Qian JX et al. Distribution characteristics of plant communities and soil organic matter and main nutrients in the Poyang Lake Nanji Wetland. Acta Ecologica Sinica, 2012, 32(12): 3656-3669. [张全军, 于秀波, 钱建鑫等. 鄱阳湖南矶湿地优势植物群落及土壤有机质和营养元素分布特征. 生态学报, 2012, 32(12): 3656-3669.] |
| [26] |
Zhang QJ, Yu XB, Hu BH. Research on the characteristics of plant communities in the Poyang Nanji Wetlands. Resources Science, 2013, 35(1): 42-49. [张全军, 于秀波, 胡斌华. 鄱阳湖南矶湿地植物群落分布特征研究. 资源科学, 2013, 35(1): 42-49. DOI:10.3969/j.issn.1672-1810.2013.01.007] |
| [27] |
Olson JS. Energy storage and the balance of producers and decomposers in ecological systems. Ecology, 1963, 44(2): 322-331. DOI:10.2307/1932179 |
| [28] |
Lang WGE. A critique of the analytical methods used in examining decomposition data obtained from litter bags. Ecology, 1982, 63(6): 1636. DOI:10.2307/1940104 |
| [29] |
Kalbitz K, Kaiser K, Bargholz J et al. Lignin degradation controls the production of dissolved organic matter in decomposing foliar litter. European Journal of Soil Science, 2006, 57(4): 504-516. DOI:10.1111/ejs.2006.57.issue-4 |
| [30] |
Debusk WF, Reddy KR. Litter decomposition and nutrient dynamics in a phosphorus enriched everglades marsh. Biogeochemistry, 2005, 75(2): 217-240. DOI:10.1007/s10533-004-7113-0 |
| [31] |
Enríquez S, Duarte CM, Sand-jensen K. Patterns in decomposition rates among photosynthetic organisms: the importance of detritus C:N:P content. Oecologia, 1993, 94(4): 457-471. DOI:10.1007/BF00566960 |
| [32] |
Atkinson RB, Cairns J. Plant decomposition and litter accumulation in depressional wetlands: functional performance of two wetland age classes that were created via excavation. Wetlands, 2001, 21(3): 354-362. DOI:10.1672/0277-5212(2001)021[0354:PDALAI]2.0.CO;2 |
| [33] |
Wu HT, Lv XG, Yang Q et al. Early-stage litter decomposition and its influencing factors in the wetland of the Sanjiang Plain, China. Acta Ecologica Sinica, 2007, 27(10): 4027-4035. [武海涛, 吕宪国, 杨青等. 三江平原典型湿地枯落物早期分解过程及影响因素. 生态学报, 2007, 27(10): 4027-4035. DOI:10.3321/j.issn:1000-0933.2007.10.010] |
| [34] |
Aber JD, Melillo JM. Litter decomposition: measuring relative contributions of organic matter and nitrogen to forest soils. Can J Bot, 1980, 58(4): 416-421. DOI:10.1139/b80-046 |
| [35] |
Wrubleski DA, Murkin HR, Valk AGVD et al. Decomposition of emergent macrophyte roots and rhizomes in a Northern Prairie Marsh. Aquatic Botany, 1997, 58(2): 121-134. DOI:10.1016/S0304-3770(97)00016-8 |
| [36] |
Xie YH, Yu D, Ren B. Effects of nitrogen and phosphorus availability on the decomposition of aquatic plants. Aquatic Botany, 2004, 80(1): 29-37. DOI:10.1016/j.aquabot.2004.07.002 |
 2019, Vol. 31
2019, Vol. 31 


