(2: 北京林果业生态环境功能提升协同创新中心, 北京 102206)
(3: 南方科技大学环境科学与工程学院, 深圳 518055)
(2: Beijing Collaborative Innovation Center for Eco-Environmental Improvement with Forestry and Fruit Trees, Beijing 102206, P. R. China)
(3: School of Environmental Science and Engineering, Southern University of Science and Technology, Shenzhen 518055, P. R. China)
近年来,湖泊沉积物的重金属污染问题日趋严重[1],尤以铜、铅的污染问题最为突出[2].已有研究数据显示中国湖泊底泥中的重金属含量在0.01~2208 mg/kg,且随着现代物质文明水平的提升,污染物负荷量在逐年递增[3-4],滇池、巢湖、太湖等主要湖泊均不同程度地受到了铜、铅、锌、镉等重金属元素的污染[5-6].其中铜、铅的被检出频次最高[7],是主要的重金属污染元素,具有较高的潜在生态风险[8],其致毒性与食物链放大性等特征严重威胁着水生生物与人类的健康安全[9-10].因此,急需加强对湖泊沉积物中铜、铅的污染控制.
当前,原位覆盖技术作为一种生态环保且投入成本低的污染沉积物原位修复技术而受到广泛关注.在原位覆盖技术中,以生物炭作为覆盖材料的修复方法,因来源广泛、操作简便,具有高稳定性等特点而逐渐成为研究热点[11-13].物理、化学及生物等改性技术的应用,使得改性生物炭的比表面积、孔隙度与表面官能团种类不同程度增加,强化了其吸附性能[14-16],以致其可以更好地控制重金属污染物的迁移. Zhang等[17]报道了在毛竹生物炭原位覆盖下铜、铅等污染沉积物中重金属的生物有效性急剧下降. Qin等[18]在修复Cd(Ⅱ)污染沉积物的研究中得出MgCl2改性生物炭较原始生物炭的吸附量显著提升.周志云等[19]向土壤中施用磷酸改性生物炭发现有效态铅含量大幅降低. Liu等[20]利用化学活化法和微波辅助活化法下的改性生物炭原位修复沉积物中的镉具有良好效果.将氨基负载到生物炭上不仅能提升生物炭对重金属离子的络合吸附能力,还有助于其他官能团的锚定,研究表明氨基改性生物炭可对废水中Cu(Ⅱ)的吸附能力提高5~8倍[21],具有广阔的开发应用潜力.
沉积物中重金属的形态会影响到重金属的生物有效性进而影响到生态环境.研究表明,与重金属总量及其他形态的重金属含量相比,可移动态重金属含量更能真实反映自然环境状态下重金属生物可利用的程度,是衡量重金属生物有效性的重要指标[22],因此,合理控制可移动态重金属的迁移,对控制重金属污染沉积物的风险和保障水生态安全至关重要.传统的主动采样方法在测定过程中容易扰动和破坏沉积环境,影响对沉积物中重金属释放特征和规律的认识,进而干扰对污染控制效果的判断.随着梯度扩散薄膜技术(DGT)的开发与应用[23-25],原位监测重金属可移动态的变化成为可能,其可以更加真实、有效地模拟沉积物中重金属离子的动态反应过程,也可以使重金属在沉积物与水体界面间迁移机制的研究更为深入.本研究基于湖泊沉积物中普遍存在的铜、铅污染问题,选取对重金属吸附固持能力更强的氨基生物炭作为覆盖材料,结合DGT技术,研究上覆水不同pH及水流扰动条件下可移动态Cu(Ⅱ)、Pb(Ⅱ)在沉积物-水界面的原位释放特征与规律,以期为湖泊重金属污染沉积物的原位修复提供理论和技术支撑,对湖泊环境中重金属的生物有效性研究及环境风险控制具有重要意义.
1 材料与方法 1.1 样品的制备 1.1.1 氨基生物炭的制备生物炭是用安徽省淮南市郊区农村产出的稻壳作为生物质原料经过热解技术制成,其制备方法基于许士鹏的研究[26]:首先将去离子水洗净后的稻壳放置于60℃的干燥箱中烘干至恒重,然后在平底瓷轴中装入烘干好的稻壳,放入管式炉中,在通N2(2 mL/min)的条件下以5℃/min升温至500℃,并保持2 h后将热解产物用超纯水洗涤,去除灰分,最后在真空干燥箱里以60℃干燥24 h后研磨、过20目筛,保存于棕色试剂瓶中.
氨基生物炭的制备方法参考杨广西的实验方案[27],具体步骤为在冰水浴条件下,向圆底烧瓶中缓慢加入浓硫酸和浓硝酸,不断搅拌10 min后加入生物炭,并继续搅拌2 h,待冷却至室温后抽滤,用超纯水和乙醇反复洗涤直至中性.将得到的固体在75℃条件下烘干至恒重,称取一定量的上述硝化生物炭放入500 mL烧杯中,同时加入2.9 mol/L氨水和去离子水不断搅拌,再加入硫代硫酸钠持续搅拌1 h,随后加入冰醋酸,加热至80℃,升温回流数小时,最后再次抽滤,用超纯水和乙醇反复洗涤至中性,将得到的固体冷冻干燥2~3天后所得的样品即为氨基生物炭.
1.1.2 污染沉积物的制备采集北京农学院校内荷花池0~10 cm表层沉积物,模拟湖泊水环境沉积物.取回的沉积物样品自然风干后研磨,过60目的筛后保存于棕色试剂瓶备用.为探究氨基生物炭应用于4000~8000 mg/kg重金属高污染沉积物[28-29]中的实际修复效果及湖泊环境中重金属离子的释放规律与特征,研究将沉积物的重金属污染浓度控制在5000 mg/kg,即在2.2 kg的沉积物样品中缓慢加入32.3 g的硝酸铜溶液与17.6 g的硝酸铅溶液,搅拌混合12 h,使其充分混匀.待自然风干、陈化2 d后,测定污染前后沉积物样品中的铜、铅含量,测定方法参见GB 17378.5-1998.研究测得加标前沉积物中铜和铅含量分别为9.6和12.1 mg/kg,低于我国淡水湖泊沉积物的铜、铅含量背景值(32和31.2 mg/kg)[30],加标后沉积物中铜和铅含量分别为3940.8和5410.8 mg/kg,位于国内外高污染湖泊沉积物中重金属的实际浓度范围区间[31-32],可以较好地模拟湖泊沉积物重金属污染的控制研究.
1.2 氨基修饰前后生物炭理化性质测定使用元素分析仪(EA,Vario EL,Elementar,德国)测定氨基修饰前后生物炭的C、H、O、N、S含量;使用扫描电子显微镜(SEM,S250MK3,Cambridge,英国)对修饰前后生物炭的表面结构进行成像分析;使用比表面积分析仪(BET,ASAP 2020,Micromeritics,美国)通过GB/T 19587-2004气体吸附BET法[33]分析得出生物炭样品的比表面积及孔容度.
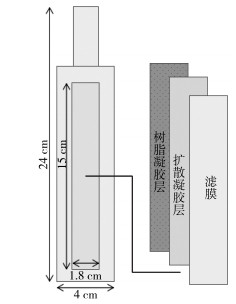
1.3 原位覆盖实验 1.3.1 DGT技术原理本研究采用的梯度扩散薄膜技术(DGT),是一种基于Fick第一扩散定律所开发的污染物原位研究技术,其由最内侧的Chelex-100树脂吸附膜、覆盖于其上具有特定厚度的聚丙烯酰胺扩散膜及起保护作用的聚醚砜滤膜组成[34-35],装置简图如图 1所示.为确保不同环境介质间的连续性和测定结果的准确性,将插入烧杯中的DGT探针定期取出后依据不同覆盖厚度,对其于玻璃板上进行0.5、1、2 cm宽度的切割分层,可对容器中所模拟的湖泊水环境下不同界面内的可移动态重金属离子的释放量进行测定.将切割后的吸附膜置于5 mL离心管中,加入2 mL 1 mol/L的HNO3,确保吸附膜被HNO3完全浸没,放置24 h后用无菌注射器抽取1 mL吸附膜溶液,稀释10倍后保存于15 mL离心管,并用原子吸收分光光度计(AAS,AA-6300,Shimadzu,日本)进行测定,按照如下公式计算测量期间内DGT与沉积物界面的平均浓度[36]:
| $ {{C}_{\text{DCT}}}=\frac{M\cdot \Delta g}{{{D}_{\text{d}}}\cdot A\cdot T} $ | (1) |
|
图 1 梯度扩散薄膜技术装置简图 Fig.1 Schematic diagram of the diffusive gradients in thin-films |
式中,M是被DGT吸附的离子总量,μg;A是DGT的开口面积,cm2;Δg是扩散膜和滤膜的总厚度,cm;T是DGT装置的测量时间,s;Dd是待测元素在扩散膜里的扩散系数,cm2/s,不同元素的扩散系数可以通过对照温度与扩散系数表获得[37].
1.3.2 原位覆盖实验设置预实验结果表明,未覆盖氨基生物炭的沉积物在100 r/min水流扰动、pH=7的上覆水环境中释放的重金属铜、铅总量分别为0.785和1.015 μg/mL,而1.81 kg/m2的氨基生物炭覆盖强度下,上覆水中的铜、铅总量(0 μg/mL和0 μg/mL)位于地表水环境质量标准(GB 3838-2002)以下,原位修复效果显著.
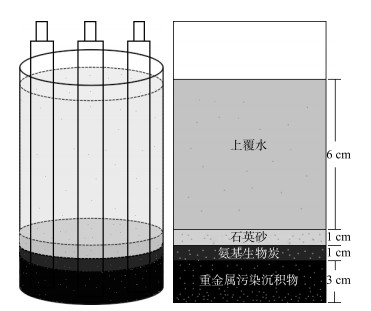
依据Zhang等[38]的研究,本研究的原位覆盖实验设置以六联电动搅拌器为主要操作平台.实验前,用稀释10倍的次氯酸钠消毒剂将六联电动搅拌器的螺旋桨和实验所需的玻璃器皿浸泡20 min,以杀死细菌和微生物,浸泡的玻璃器皿清洗后,再用去离子水重复冲洗2次,并在90℃下烘干6 h.具体操作步骤如下:首先在1000 mL烧杯的底部平铺厚度为3 cm(覆盖强度为36.15 kg/m2)的污染沉积物,然后缓慢加入50 mL去离子水浸润沉积物;其次在沉积物上均匀平铺厚度约为0.74±0.05 cm(覆盖强度为1.81 kg/m2)的氨基生物炭,然后缓慢加入20 mL去离子水,以防止沉积物和生物炭的扬起或漂浮;最后在生物炭上面平铺厚度约为1.12±0.05 cm(覆盖强度为20.79 kg/m2)的石英砂,压实、固定沉积物与氨基生物炭覆盖层,然后缓慢加入约730 mL去离子水,使上覆水液面距沉积物底层的平均高度约为11 cm,并在每个烧杯中插入3个DGT探针,具体实验示意图如图 2所示.由于氨基生物炭对重金属的吸附受时间、上覆水pH及水流扰动等因素影响,且重金属在0~3、3~10、10~20天的释放状态不同[38-39],因此,在六联电动搅拌器启动后,每24 h测定一次上覆水pH,发现与目标pH有显著差异后使用0.01 mol/L的NaOH与HNO3调节pH,并将实验组的扰动速度设定为100 r/min,对照组的扰动速度设定为0 r/min.自实验起始日起的第3、10和19天的同一时间点取出DGT,原位测定各填充层内的可移动态重金属离子浓度.
|
图 2 实验示意图及填充容器纵向剖面图 Fig.2 Experimental schematic diagram and longitudinal section of filled vessel |
研究使用的DGT装置购自南京维申环保科技有限公司,DGT装置扩散层厚度Δg为0.092 cm,窗口面积A为27 cm2.上述每个实验均设置2个平行,结果取平均值,数据采用Excel进行分析,Origin Pro 2015软件作图.
2 结果与讨论 2.1 氨基修饰前后生物炭的性质分析氨基生物炭修饰前后的理化性质测定结果如表 1所示[40],生物炭经过氨基修饰改性后,其比表面积增大了61 %,孔容度增大了6.5倍左右.这是由于生物炭在氨基修饰过程中,表面的灰分被浓硫酸及浓硝酸去除,并在其表面发生了明显的刻蚀作用,使得其比表面积和孔容度显著增大,吸附性能增强[41].氨基修饰改性前后的生物炭元素分析表明,修饰后生物炭的O、N、S元素含量分别增加了10.18 %、2.51 %和3.36 %,而C、H元素含量分别减少了6.23 %和0.1 %,对比氨基修饰前后生物炭的各原子比率得出,N/C值7倍的提高说明氨基官能团和硫基官能团已被成功负载到了原始生物炭上,使得原始生物炭单一的表面性质得到了一定程度的改善;O/C值1.93倍的增加说明生物炭表面极性官能团含量及亲水性增强;H/C值0.07倍的增加说明改性后生物炭的芳香性较原始生物炭小幅加强;(O+C)/N值2.12倍的增加说明在化学改性的作用下氨基修饰生物炭的极性变大[42-43].
| 表 1 修饰前后生物炭的理化性质 Tab. 1 Physicochemical properties of biochar before and after modification |
图 3为扫描电子显微镜下修饰前后生物炭的形貌特征图,对比形貌特征图发现氨基修饰生物炭的表面较原始生物炭更加平整,且具有明显的孔隙结构,这与表 1中表面积和孔容度的变化结果一致.

|
图 3 氨基修饰前后生物炭的扫描电镜图:a为原始生物炭,b为氨基生物炭 Fig.3 SEM images of biochar and amino biochar: a is the original biochar; b is the amino biochar |
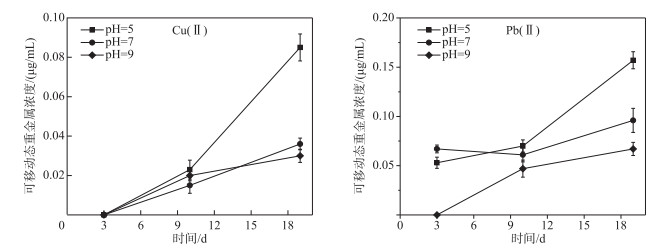
环境酸碱度是原位覆盖实验的一个重要影响因素,不同酸碱度下,重金属离子的存在形态不同,且对覆盖材料氨基生物炭的活性位点具有重要影响. 图 4所示为不同pH上覆水中重金属浓度的时间变化趋势,实验第3天的数据显示,在pH=5、7、9的不同酸碱度环境中均无Cu(Ⅱ)检出(0 μg/mL),而Pb(Ⅱ)之间的差异则较大,具体表现为中性条件下的浓度最高(0.067 μg/mL),酸性次之(0.053 μg/mL),碱性最小(0 μg/mL).第10天时,Cu(Ⅱ)在酸性环境中的浓度最高(0.023 μg/mL),碱性次之(0.020 μg/mL),中性最小(0.015 μg/mL);Pb(Ⅱ)以酸性环境中居多(0.070 μg/mL),中性次之(0.061 μg/mL),碱性最小(0.047 μg/mL).第19天时,酸性条件下的Cu(Ⅱ)、Pb(Ⅱ)分别达到了0.085和0.157 μg/mL,均明显高于中性(0.036和0.096 μg/mL)及碱性环境,其中以碱性环境浓度最低(0.030、0.067 μg/mL).综上所述,在酸性水环境中,重金属离子浓度最高,这是因为在pH=5的酸性条件下,水溶液中大量的H+容易使生物炭表面发生质子化反应而带正电,导致其与重金属离子产生同性电荷排斥作用,影响了氨基生物炭对重金属离子的吸附[44-45].在碱性水环境中,重金属离子浓度最低,这表明在pH=9的碱性条件下,氨基生物炭的吸附能力增强,但溶液中的Cu(Ⅱ)、Pb(Ⅱ)易与OH-发生络合沉淀反应,形成的络合物可能抑制氨基生物炭的吸附能力,也会干扰对氨基生物炭实际吸附效果的正确判断[46-47].在中性水环境中,氨基生物炭的吸附能力最稳定,这是因为在pH=7的中性条件下,水中富含的大量Cu(Ⅱ)、Pb(Ⅱ)既不会与过量的H+竞争氨基生物炭的吸附位点,也不会与OH-发生络合沉淀,原位覆盖的修复效果最佳[41].关于自然水体中铜和铅的存在形态已有大量研究[48-49],当pH < 6时主要以Cu2+和Pb2+的形态存在;6 < pH < 12时主要以Cu(OH)+、Cu3(OH)42+、Cu(OH)2和Pb(OH)+、Pb3(OH)42+、Pb(OH)2的形态存在,且pH>7.7时,Cu(OH)2和Pb(OH)2开始形成;pH>12时主要以Cu(OH)3-和Pb(OH)3-的形态存在.这意味着氨基生物炭可能会与水中的OH-和H+相结合,进而影响沉积物中重金属离子的释放速率和浓度.此外,由于大多数湖泊水环境的pH接近为中性及弱碱性[30, 50],因此,基于pH为7的上覆水模拟自然湖泊水环境,可以有效避免pH值对水环境中重金属离子赋存形态与氨基生物炭吸附能力的影响.
|
图 4 不同pH上覆水中可移动态重金属浓度的时间变化趋势 (100 r/min扰动强度,1.81 kg/m2生物炭覆盖强度,25±0.5℃条件下) Fig.4 Time-varying trend of mobile heavy metal concentrations in overlying water at different pH values (The condition is 100 r/min hydrodynamic, 1.81 kg/m2 bio-carbon cover, 25±0.5℃) |
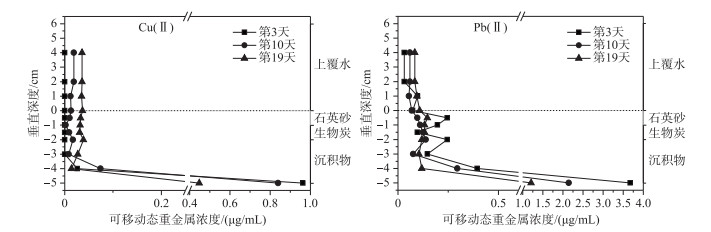
根据湖泊沉积物-水模拟环境中不同介质层的覆盖厚度将烧杯中的DGT探针切割为10段,以石英砂-水界面为零点,上方0~6 cm为上覆水层,下方1 cm深度以石英砂覆盖层为主,1~2 cm深度以氨基生物炭覆盖层为主,2~5 cm深度主要为沉积物覆盖层.模拟环境中重金属离子浓度的垂直分布如图 5所示,在氨基生物炭阻隔、吸附的作用下,距离氨基生物炭覆盖层较近的表层沉积物与底层沉积物中的重金属含量有明显差异,实验的第3、10、19天,Cu(Ⅱ)浓度分别相差0.963、0.831、0.420 μg/mL,Pb(Ⅱ)浓度分别相差3.526、2.070、1.102 μg/mL.氨基生物炭-石英砂-上覆水界面的重金属浓度变化则较为平缓,上覆水中的Cu(Ⅱ)保持在0~0.037 μg/mL,Pb(Ⅱ)保持在0.031~0.108 μg/mL,始终处于较低水平.以上结果表明,氨基修饰生物炭具有较强的重金属吸附能力,以其为覆盖材料的原位修复技术具有良好的修复效果.就整体分布而言,Pb(Ⅱ)在不同环境介质的过渡段会出现不稳定的释放,Cu(Ⅱ)相对平稳,这种现象可能是由于Pb(Ⅱ)与Cu(Ⅱ)之间存在竞争吸附,而Cu(Ⅱ)与氨基官能团形成的外球络合作用更有利于氨基生物炭对Cu(Ⅱ)的稳定吸附[27],其对Pb(Ⅱ)的吸附稳定性则相对较弱,在过渡界面间外界因素的作用下极易导致Pb(Ⅱ)的解吸释放.随着时间的推移,沉积物底层中的Cu(Ⅱ)浓度由0.963 μg/mL降低到0.447 μg/mL,Pb(Ⅱ)浓度由3.673 μg/mL降低到1.207 μg/mL,上覆水表层中的Cu(Ⅱ)浓度随时间的变化由0 μg/mL增加到0.036 μg/mL,Pb(Ⅱ)浓度由0.031 μg/mL增加到0.084 μg/mL,这表明沉积物-水界面间的浓度梯度使得沉积物层的重金属离子有不断向上覆水中扩散的趋势[51],但由于氨基生物炭的吸附作用,使得大多数重金属离子被吸附固定在生物炭表面,从而大大降低了上覆水中的重金属浓度,起到了污染迁移控制的作用.氨基生物炭对湖泊沉积物中重金属离子的吸附固化机理可解释为,其表面结构与重金属离子发生的物理吸附,其表面官能基团、矿物质成分、电荷及电离质子与环境介质中的重金属离子发生的络合沉淀反应、静电作用及离子交换反应综合作用而成[52-53].
|
图 5 填充层中可移动态重金属浓度的垂直分布 (100 r/min扰动强度,1.81 kg/m2生物炭覆盖强度,上覆水pH=7,25±0.5℃条件下) Fig.5 Vertical distribution of mobile heavy metal concentrations in filling layer (The condition is 100 r/min hydrodynamic, 1.81 kg/m2 bio-carbon cover, overlying water pH=7, 25±0.5℃) |
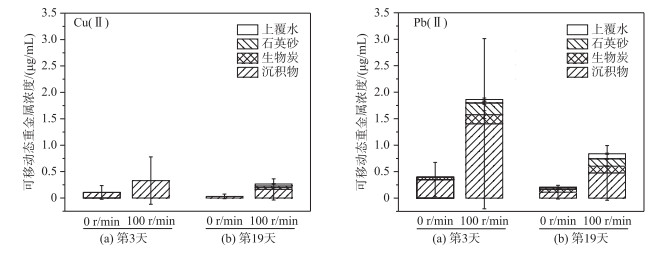
风浪或航运等原因引起的水体扰动易导致沉积物的大量悬浮,促进污染物从泥沙颗粒相中的解吸释放,对水生生态系统具有潜在威胁,是影响湖泊沉积物-水界面反应的重要物理因素[54-55].已有研究表明,水流扰动模拟实验过程中不同介质内的污染物浓度在大约第3天达到初始稳定状态,大约第20天达到释放平衡状态[38, 56].如图 6所示在两种不同释放状态时0 r/min或100 r/min扰动强度对可移动态Cu(Ⅱ)、Pb(Ⅱ)释放的特征分析表明,同一时间的不同扰动强度下,动水条件(100 r/min)较静水条件(0 r/min)环境中的重金属浓度高;相同扰动强度在不同时间下,沉积物层的重金属浓度随时间变化逐渐降低,有明显向其他介质(石英砂、生物炭、上覆水)迁移的现象;从初始稳定状态到释放平衡状态,0 r/min扰动条件下的上覆水中Cu(Ⅱ)、Pb(Ⅱ)均为0 μg/mL;100 r/min扰动条件下的Cu(Ⅱ)、Pb(Ⅱ)在上覆水中的含量均随时间的变化逐渐升高,具体表现由0、0.067 μg/mL升高至0.036、0.096 μg/mL,因此,静水条件下氨基生物炭覆盖的原位修复效果较好,而动水条件下的原位修复效果被削弱.产生这种结果的原因可能是由于在物理扰动的作用下,沉积物、生物炭和石英砂等颗粒物发生再悬浮,颗粒态重金属得到释放,上覆水中的重金属含量增加[57].此外,上覆水体中的紊动扩散代替了分子扩散,扩散强度得到了很大提高,沉积物中的间隙水与上覆水得到了充分混合,促进了沉积物中Cu(Ⅱ)与Pb(Ⅱ)的释放,降低了间隙水中的重金属离子浓度,提高了上覆水中的重金属离子浓度[58-59].研究证明,水流的扰动将会造成上层覆盖材料的扬起和浮动,对原位覆盖的处理效果造成不利影响,削弱覆盖材料对重金属的吸附固持能力.这与雷阳等[60]对Ni和Cd等重金属的释放速率和最大释放量同水流扰动强度的增大而增大,以及华祖林等[61]在水动力作用下发现水体中氧化还原条件的改变,将使得重金属的形态和分布发生变化,并与盐离子之间产生竞争吸附效应,从而导致重金属从悬浮颗粒物上解吸的研究结果相一致.
|
图 6 不同扰动强度下可移动态重金属释放量的时间变化趋势 (上覆水pH=7,1.81 kg/m2生物炭覆盖强度,25±0.5℃条件下) Fig.6 Time-varying trend of mobile heavy metal release under different hydrodynamic (The condition is overlying water pH=7, 1.81 kg/m2 bio-carbon cover, 25±0.5℃) |
湖泊是重要的淡水资源及水生生态系统,沉积物作为其中的主要组成部分之一,对水生生物的生存具有重要影响.近年来,随着人类现代化进程加快,工业化和城市化给湖泊水生态系统造成了严重污染,大量的重金属污染物通过交通排放、废水输入、大气沉降和农业活动等途径进入水体环境,富集到沉积物中,导致水质下降并产生不同程度的污染,对水体生态系统造成严重危害[62-63].
由于大多数湖泊水环境的pH接近为中性及弱碱性[30, 50],且中性条件下的原位修复效果最佳,故本研究针对高浓度重金属污染的沉积物及pH为7的上覆水环境,通过公式F=M/(A ·T)对DGT测量重金属的通量进行了计算[64],式中,M是DGT的吸附离子总量,μg;A是DGT的开口面积,cm2;T是DGT的测量时间,s.
由表 2所知,当氨基生物炭覆盖强度为1.81 kg/m2时,其可以安全地确保在持续19天0 r/min或100 r/min水动力作用下的上覆水表层中Cu(Ⅱ)、Pb(Ⅱ)释放通量较沉积物底层明显下降.在沉积物底层至上覆水表层的过程中,0 r/min下Cu(Ⅱ)的释放通量降低率为95 %,明显高于Pb(Ⅱ)的89 %,而在100 r/min下,Cu(Ⅱ)与Pb(Ⅱ)的释放通量降低率相差不大,分别为92 %和93 %.结果表明以氨基生物炭为覆盖材料的原位覆盖修复技术可以通过吸附、沉淀、络合等方式抑制沉积物中重金属离子的释放,从而降低上覆水中可移动态重金属离子的浓度,减小重金属污染对水体生态系统的危害风险,但不同离子之间的离子强度与竞争效应会对吸附过程产生较大影响,吸附效果有所差异[65].
| 表 2 不同环境介质中的可移动态重金属的释放通量(pg/(cm2 ·s)) Tab. 2 The release flux of mobile heavy metal in different environmental medium |
1) 与原始生物炭相比,氨基改性生物炭的比表面积增大了61 %,孔容度增大了6.5倍,各原子比率均在不同程度上有所提高,其表面的含氧官能团及吸附点位明显增多,对污染物的吸附能力明显增强.
2) 氨基生物炭原位覆盖的修复效果为中性(pH=7)>碱性(pH=9)>酸性(pH=5),静水(0 r/min)>动水(100 r/min);当上覆水pH为中性、静水条件时,氨基生物炭原位覆盖的修复效果最佳.
3) 在模拟环境下的自然湖泊水中,沉积物-氨基生物炭-石英砂-上覆水界面内的有效态重金属离子有不断由沉积物向其他介质扩散的趋势.氨基生物炭在1.81 kg/m2覆盖强度下,其阻隔、吸附作用可有效降低沉积物底层至上覆水表层的Cu(Ⅱ)、Pb(Ⅱ)释放通量,减小重金属的潜在生态风险.
| [1] |
Álvarez MS, Gutiérrez E, Rodríguez A et al. Environmentally benign sequential extraction of heavy metals from marine sediments. Industrial & Engineering Chemistry Research, 2014, 53(20): 8615-8620. DOI:10.1021/ie500927q |
| [2] |
Dong DM, Lu YZ, Li Y et al. The distribution of heavy metals in the surface sediments in parts of rivers and lakes in Jilin province. Journal of Jilin University: Earth Science Edition, 2005, 35(1): 91-96. [董德明, 路永正, 李鱼等. 吉林省部分河流与湖泊表层沉积物中重金属的分布规律. 吉林大学学报:地球科学版, 2005, 35(1): 91-96.] |
| [3] |
Bing HJ, Wu YH, Liu EF et al. The accumulation and potential ecological risk evaluation of heavy metals in the sediment of different lakes with in the middle and lower reaches of Yangtze River. J Lake Sci, 2010, 22(5): 675-683. [邴海健, 吴艳宏, 刘恩峰等. 长江中下游不同湖泊沉积物中重金属污染物的累积及其潜在生态风险评价. 湖泊科学, 2010, 22(5): 675-683. DOI:10.18307/2010.0508] |
| [4] |
Wang W, Fan XK, Huang CG et al. Monitoring and comparison analysis of heavy metals in the five great lakes in Jiangsu Province. J Lake Sci, 2016, 28(3): 494-501. [王伟, 樊祥科, 黄春贵等. 江苏省五大湖泊水体重金属的监测与比较分析. 湖泊科学, 2016, 28(3): 494-501. DOI:10.18307/2016.0304] |
| [5] |
Liu X, Jiang Y, Gao JF et al. Pollution characteristics of heavy metals and the risk assessment for the surface sediments from Lake Chaohu and its main tributary rivers. J Lake Sci, 2016, 28(3): 502-512. [刘新, 蒋豫, 高俊峰等. 巢湖湖区及主要出入湖河流表层沉积物重金属污染特征及风险评价. 湖泊科学, 2016, 28(3): 502-512. DOI:10.18307/2016.0305] |
| [6] |
Jiang HM, Zheng XP, Li W. Source and risk assessment of heavy metal in sediment of China. China Population, Resources and Environment, 2018, 28(S1): 108-112. [姜会敏, 郑显鹏, 李文. 中国主要湖泊重金属来源及生态风险评估. 中国人口·资源与环境, 2018, 28(S1): 108-112.] |
| [7] |
Hua LP, Hua L, Gao J et al. Heavy metal pollution of sediments of lakes in China. Soils, 2006(4): 366-373. [滑丽萍, 华珞, 高娟等. 中国湖泊底泥的重金属污染评价研究. 土壤, 2006(4): 366-373. DOI:10.3321/j.issn:0253-9829.2006.04.003] |
| [8] |
Jiao W, Lu SY, Li GD et al. Heavy metals pollution and potential ecological risk assessment of inner lakeside belt of Lake Dianchi. Journal of Agro-Environment Science, 2010, 29(4): 740-745. [焦伟, 卢少勇, 李光德等. 滇池内湖滨带重金属污染及其生态风险评价. 农业环境科学学报, 2010, 29(4): 740-745.] |
| [9] |
Yi YJ, Wang ZY, Zhang K et al. Sediment pollution and its effect on fish through food chain in the Yangtze River. International Journal of Sediment Research, 2008, 23(4): 338-347. DOI:10.1016/s1001-6279(09)60005-6 |
| [10] |
Ji B, Hang XS, Liang B et al. Advances in heavy metals contamination of lake sediment. Pollution Control Technology, 2013(5): 33-40. [季斌, 杭小帅, 梁斌等. 湖泊沉积物重金属污染研究进展. 污染防治技术, 2013(5): 33-40.] |
| [11] |
Jiang YY, Hu XM, Jin WB. Advances on absorption of heavy metals in the waste water bybiochar. Hubei Agricultural Sciences, 2013, 52(13): 2984-2988. [蒋艳艳, 胡孝明, 金卫斌. 生物炭对废水中重金属吸附研究进展. 湖北农业科学, 2013, 52(13): 2984-2988. DOI:10.3969/j.issn.0439-8114.2013.13.003] |
| [12] |
Guo SH. Effects of biochar on lead or zinc contaminated soil[Dissertation]. Changsha: Hunan University of Science and Technology, 2015. [郭素华.生物炭对铅、锌污染土壤的修复作用[学位论文].长沙: 湖南科技大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10534-1015812448.htm ]
|
| [13] |
Qu RJ. Preparation of metal ion adsorbing materials ·Structure ·Properties. Beijing: Chemical Industry Press, 2009. [曲荣君. 金属离子吸附材料制备·结构·性能. 北京: 化学工业出版社, 2009.]
|
| [14] |
Yu ZH, Qiu WW, Wang F et al. Effects of manganese oxide-modified biochar composites on arsenic speciation and accumulation in an indica rice (Oryza sativa L.) cultivar. Chemosphere, 2017, 168(2): 341-349. DOI:10.1016/j.chemosphere.2016.10.069 |
| [15] |
Wang SJ, Guo W, Gao F et al. Characterization and Pb(Ⅱ) removal potential of corn straw- and municipal sludge-derived biochars. Royal Society Open Science, 2017, 4(9): 170402. DOI:10.1098/rsos.170402 |
| [16] |
Ji HY, Wang YY, Liu YX et al. Research progress in preparation and application of biochar and modified biochar. Journal of Nuclear Agricultural Sciences, 2018, 32(11): 2281-2287. [计海洋, 汪玉瑛, 刘玉学等. 生物炭及改性生物炭的制备与应用研究进展. 核农学报, 2018, 32(11): 2281-2287. DOI:10.11869/j.issn.100-8551.2018.11.2281] |
| [17] |
Zhang C, Shan BQ, Zhu YY et al. Remediation effectiveness of Phyllostachys pubescens biochar in reducing the bioavailability and bioaccumulation of metals in sediments. Environmental Pollution, 2018, 242(7): 1768-1776. DOI:10.1016/j.envpol.2018.07.091 |
| [18] |
Tao Q, Li B, Li QQ et al. Simultaneous remediation of sediments contaminated with sulfamethoxazole and cadmium using magnesium-modified biochar derived from Thalia dealbata. Science of the Total Environment, 2019, 659(4): 1448-1456. DOI:10.1016/j.scitotenv.2018.12.361 |
| [19] |
Zhou ZY, Ma WL, Zhou Z et al. Effects of phosphoric-acid-modified biochar combined with chlorine on soil lead form and lead absorption in wheat. Journal of Agro-Environment Science, 2018, 37(5): 899-906. [周志云, 马文连, 周振等. 磷酸改性生物炭和氯混施对土壤铅形态及小麦铅吸收的影响. 农业环境科学学报, 2018, 37(5): 899-906. DOI:10.11654/jaes.2018-0067] |
| [20] |
Liu SJ, Liu YG, Tan XF et al. The effect of several activated biochars on Cd immobilization and microbial community composition during in-situ remediation of heavy metal contaminated sediment. Chemosphere, 2018, 208(6): 655-664. DOI:10.1016/j.chemosphere.2018.06.023 |
| [21] |
Yang GX, Jiang H. Amino modification ofbiochar for enhanced adsorption of copper ions from synthetic wastewater. Water Research, 2014, 48(1): 396-405. DOI:10.1016/j.watres.2013.09.050 |
| [22] |
Sun XY, Luo LQ. Research progress on the application bioavailability of heavy metals to evaluate ecological risk in mining area. Conservation and Utilization of Mineral Resources, 2019, 39(1): 100-108. [孙晓艳, 罗立强. 重金属生物有效性在矿山环境评价中应用研究进展. 矿产保护与利用, 2019, 39(1): 100-108.] |
| [23] |
Degryse F, Smolders E, Zhang H et al. Predicting availability of mineral elements to plants with the DGT technique: a review of experimental data and interpretation by modelling. Environmental Chemistry, 2009, 6(6): 198-218. DOI:10.1071/EN09010 |
| [24] |
Nolan AL, Zhang H, Mclaughlin MJ. Prediction of zinc, cadmium, lead, and copper availability to wheat in contaminated soils using chemical speciation, diffusive gradients in thin films, extraction, and isotopic dilution techniques. Journal of Environmental Quality, 2005, 34(2): 496-507. DOI:10.2134/jeq2005.0496 |
| [25] |
Zhang H, Zhao FJ, Zhao FJ et al. A new method to measure effective soil solution concentration predicts copper availability to plants. Environmental Science & Technology, 2001, 35(12): 2602-2607. DOI:10.1021/es000268q |
| [26] |
Xu SP. Preparation ofbiochar adsorbent and study on the adsorption properties to heavy metals in aqueous solution[Dissertation]. Jinan: University of Jinan, 2015. [许世鹏.生物炭吸附剂研制及对废水中重金属的吸附特性研究[学位论文].济南: 济南大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10427-1015447800.htm ]
|
| [27] |
Yang GX. Chemical modification ofbiochar and its adsorption toward copper (Ⅱ)[Dissertation]. Hefei: University of Science and Technology of China, 2014. [杨广西.生物炭的化学改性及其对铜的吸附研究[学位论文].合肥: 中国科学技术大学, 2014. http://d.wanfangdata.com.cn/Thesis/Y2589992 ]
|
| [28] |
Li HB, Cao MH, Wu DS et al. Stabilization efficiency and mechanism of heavy metals in contaminated lake sediments by ferrous sulfide. Chinese Journal of Environmental Engineering, 2017, 11(5): 3258-3263. [李海波, 曹梦华, 吴丁山等. 硫化亚铁稳定化修复重金属污染湖泊底泥的效率及机理. 环境工程学报, 2017, 11(5): 3258-3263. DOI:10.12030/j.cjee.201609184] |
| [29] |
Chen Y, Chen BH, Zou Q et al. Distribution and influencing factors of heavy metals in water-sediments in Dabaoshan mine, northern Guangdong Province. Acta Scientiae Circumstantiae, 2018, 38(1): 133-141. [陈莹, 陈炳辉, 邹琦等. 粤北大宝山AMD水-表层沉积物的重金属分布特征及其影响因素. 环境科学学报, 2018, 38(1): 133-141. DOI:10.13671/j.hjkxxb.2017.0121] |
| [30] |
Li M, Cheng HX, Li K. Geochemical background of freshwater lake sediments: a constraint on the establishment of sediment quality guidelines in China. Earth Science Frontiers, 2018, 25(4): 276-284. [李敏, 成杭新, 李括. 中国淡水湖泊沉积物地球化学背景与环境质量基准建立的思考. 地学前缘, 2018, 25(4): 276-284. DOI:10.13745/j.esf.yx.2017-5-9] |
| [31] |
Gosar M, Miler M. Anthropogenic metal loads and their sources in stream sediments of the Meza River catchment area (NE Slovenia). Applied Geochemistry, 2011, 26(11): 1855-1866. DOI:10.1016/j.apgeochem.2011.06.009 |
| [32] |
Atibu EK, Lacroix P, Sivalingam P et al. High contamination in the areas surrounding abandoned mines and mining activities: An impact assessment of the Dilala, Luilu and Mpingiri Rivers, Democratic Republic of the Congo. Chemosphere, 2017, 191(10): 1008-1020. DOI:10.1016/j.chemosphere.2017.10.052 |
| [33] |
Liu A, Ba XW, Liu Y et al. Solid specific surface area measurement with BET capacity method. Journal of Changchun University of Techology, 2012, 33(2): 197-199. [柳翱, 巴晓微, 刘颖等. BET容量法测定固体比表面积. 长春工业大学学报, 2012, 33(2): 197-199. DOI:10.3969/j.issn.1674-1374-B.2012.02.018] |
| [34] |
Davlson W, Zhang H. In situ speciation measurements of trace components in natural waters using thin-film gels. Nature, 1994, 367(6463): 546-548. DOI:10.1038/367546a0 |
| [35] |
Zhou CY, Guan DX, Han YH et al. Pollution characteristics of metals and nutrients in different regions of lake Taihu based on diffusive gradients in thin-films technique. Journal of Agricultural Environmental Science, 2016, 35(6): 1144-1152. [周春羊, 管冬兴, 韩永和等. 基于梯度扩散薄膜技术的太湖金属和营养盐区域污染特征分析. 农业环境科学学报, 2016, 35(6): 1144-1152. DOI:10.11654/jaes.2016.06.017] |
| [36] |
Luo J, Wang XR, Zhang H et al. Theory and application of diffusive gradients in thin films in soils. Journal of Agricultural Environmental Science, 2011, 30(2): 205-213. [罗军, 王晓蓉, 张昊等. 梯度扩散薄膜技术(DGT)的理论及其在环境中的应用Ⅰ:工作原理、特性与在土壤中的应用. 农业环境科学学报, 2011, 30(2): 205-213.] |
| [37] |
Scally S, Davison W, Zhang H. Diffusion coefficients of metals and metal complexes in hydrogels used in diffusive gradients in thin films. Analytica Chimica Acta, 2006, 558(1/2): 222-229. DOI:10.1016/j.aca.2005.11.020 |
| [38] |
Zhang S, Tian K, Jiang SF et al. Preventing the release of Cu(Ⅱ) and 4-CP from contaminated sediments by employing a biochar capping treatment. Industrial & Engineering Chemistry Research, 2017, 56(27): 7730-7738. DOI:10.1021/acs.iecr.7b01548 |
| [39] |
黄廷林, 沈晋. 环境化学条件对水体沉积物中重金属释放影响的研究述评. 西安理工大学学报, 1993(4): 285-292. |
| [40] |
Wang SJ, Guo W, Shi JH et al. Adsorption kinetics of uranium(Ⅵ) from aqueous solution by amino modified rice husk biochar. Research of Environmental Sciences, 2019, 32(2): 347-355. [王淑娟, 郭伟, 史江红等. 氨基修饰稻壳生物炭对水溶液中铀的吸附动力学特性. 环境科学研究, 2019, 32(2): 347-355.] |
| [41] |
Wang SJ. The removal of lead, copper and uranium by amino modified magneticbiochar from aqueous solutions[Dissertation]. Beijing: North China Electric Power University, 2018. [王淑娟.氨基磁化生物炭对水中铅、铜、铀的吸附性能研究[学位论文].北京: 华北电力大学, 2018. http://cdmd.cnki.com.cn/Article/CDMD-11412-1018238817.htm ]
|
| [42] |
Schmidt MWI, Noack AG. Black carbon in soils and sediments: analysis, distribution, implications, and current challenges. Global Biogeochemical Cycles, 2000, 14(3): 777-793. DOI:10.1029/1999GB001208 |
| [43] |
Chuan Y, Sheng GY, Chiou CT et al. Compositions and sorptive properties of crop residue-derived chars. Environmental Science & Technology, 2004, 38(17): 4649-4655. DOI:10.1021/es035034w |
| [44] |
Lin XY, Jing YD, Gong C et al. Research progress on the sorption of heavy metals by biochar. Environmental Pollution & Control, 2014, 36(5): 83-87. [林雪原, 荆延德, 巩晨等. 生物炭吸附重金属的研究进展. 环境污染与防治, 2014, 36(5): 83-87. DOI:10.3969/j.issn.1001-3865.2014.05.017] |
| [45] |
Kadirvelu K, Kavipriya M, Karthika C et al. Mercury (Ⅱ) adsorption by activated carbon made from sago waste. Carbon, 2004, 42(4): 745-752. DOI:10.1016/j.carbon.2003.12.089 |
| [46] |
Li L, Lu YC, Liu Y et al. Adsorption mechanisms of cadmium(Ⅱ) on biochars derived from corn straw. Journal of Agro-Environment Science, 2012(11): 2277-2283. [李力, 陆宇超, 刘娅等. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究. 农业环境科学学报, 2012(11): 2277-2283.] |
| [47] |
Han LJ, Li YF, Liu X et al. Review of biochar as adsorbent for aqueous heavy metal removal. Transactions of the Chinese Society for Agricultural Machinery, 2017, 48(11): 1-11. [韩鲁佳, 李彦霏, 刘贤等. 生物炭吸附水体中重金属机理与工艺研究进展. 农业机械学报, 2017, 48(11): 1-11. DOI:10.6041/j.issn.1000-1298.2017.11.001] |
| [48] |
Mohan D, Singh P, Sarswat A et al. Lead sorptive removal using magnetic and nonmagnetic fast pyrolysis energy cane biochars. Journal of Colloid and Interface Science, 2015, 448(6): 238-250. DOI:10.1016/j.jcis.2014.12.030 |
| [49] |
Yuan F. Investigation of the mechanisms of the heavy metal speciation and removal as a function of pH viamicellar enhanced ultrafiltration[Dissertation]. Changsha: Hunan University, 2016. [袁方.不同pH值下重金属的形态及MEUF法对其去除机理的研究[学位论文].长沙: 湖南大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10532-1016242627.htm ]
|
| [50] |
Zhang XY, Sun XM, Yuan GF et al. Primary analysis of water pH and salinity monitoring data on Chinese Ecosystem Research Network (CERN). Advances in Earth Science, 2009, 24(9): 1042-1050. [张心昱, 孙晓敏, 袁国富等. 中国生态系统研究网络水体pH和矿化度监测数据初步分析. 地球科学进展, 2009, 24(9): 1042-1050. DOI:10.3321/j.issn:1001-8166.2009.09.011] |
| [51] |
Wang XQ, Zheng LP, Sun WM. The distribution characteristics of heavy metal elements in the pore water of sediment, Dianshan Lake. China Environmental Science, 2004(4): 17-21. [王小庆, 郑乐平, 孙为民. 淀山湖沉积物孔隙水中重金属元素分布特征. 中国环境科学, 2004(4): 17-21.] |
| [52] |
Ahmad M, Rajapaksha AU, Lim JE et al. Biochar as a sorbent for contaminant management in soil and water: A review. Chemosphere, 2014, 99(3): 19-33. DOI:10.1016/j.chemosphere.2013.10.071 |
| [53] |
Li SY, Hu ZQ, Chen Q et al. Adsorption effect of modified biochar on the heavy metals in wastewater. Industrial Water Treatment, 2018, 38(7): 7-12. [李仕友, 胡忠清, 陈琴等. 改性生物炭对废水中重金属的吸附. 工业水处理, 2018, 38(7): 7-12.] |
| [54] |
Wang P, Li QQ, Cai YJ. Effect of sediment resuspension on BPA adsorption in Taihu lake. Water Resources Protection, 2015, 31(5): 35-41. [王鹏, 李琼琼, 蔡赟杰. 太湖沉积物再悬浮对双酚A吸附性能的影响. 水资源保护, 2015, 31(5): 35-41.] |
| [55] |
Kiratli N, Ergin M. Partitioning of heavy metals in surface Black Sea sediments. Applied Geochemistry, 1996, 11(6): 775-788. DOI:10.1016/S0883-2927(96)00037-6 |
| [56] |
Cheng HM, Hua ZL. Distribution, release and removal behaviors of tetrabromobisphenol A in water-sediment systems under prolonged hydrodynamic disturbances. Science of the Total Environment, 2018, 636(4): 402-410. DOI:10.1016/j.scitotenv.2018.04.276 |
| [57] |
Wang PF, Hu Y, Wang C et al. Analysis on mobility of heavy metals between sediment-water under different hydrodynamic conditions. Journal of Civil, Architectural & Environmental Engineering, 2012, 34(3): 151-158. [王沛芳, 胡燕, 王超等. 动水条件下重金属在沉积物水之间的迁移规律. 土木建筑与环境工程, 2012, 34(3): 151-158.] |
| [58] |
Tang HL. Experimental study on the heavy metals release from the sediments in theliyun River[Dissertation]. Nanjing: Hohai University, 2006. [汤红亮.里运河底泥重金属释放实验研究[学位论文].南京: 河海大学, 2006. http://cdmd.cnki.com.cn/Article/CDMD-10294-2006077191.htm ]
|
| [59] |
Jiao L, Qi PS, Gong KY et al. Impacting factors of heavy metal release from sediments of Songhua River. Environmental Protection Science, 2016, 42(2): 85-89. [焦龙, 祁佩时, 宫凯悦等. 松花江底泥沉积物中重金属释放影响因素的研究. 环境保护科学, 2016, 42(2): 85-89.] |
| [60] |
Lei Y, Wang PF, Wang C et al. The effect of submerged plants on the release of heavy metal from sediment under different hydrodynamic disturbances. Chinese Journal of Hydrodynamics, 2015, 30(3): 245-250. [雷阳, 王沛芳, 王超等. 不同水动力扰动下沉水植物对沉积物重金属释放的影响. 水动力学研究与进展, 2015, 30(3): 245-250.] |
| [61] |
Hua ZL, Wang Y. Advance on the release of pollutants in river and lake sediments under hydrodynamic conditions. Journal of Hohai University: Natural Sciences, 2018, 46(2): 95-105. [华祖林, 王苑. 水动力作用下河湖沉积物污染物释放研究进展. 河海大学学报:自然科学版, 2018, 46(2): 95-105.] |
| [62] |
Jia GN. Harm and defence of heavy metals. Non-Ferrous Mining and Metallurgy, 2004, 20(1): 39-42. [贾广宁. 重金属污染的危害与防治. 有色矿冶, 2004, 20(1): 39-42. DOI:10.3969/j.issn.1007-967X.2004.01.013] |
| [63] |
Li XH, Zheng GZ. Soil heavy metal pollution and human health. Environment and Development, 2016, 28(1): 122-124. [李向宏, 郑国璋. 土壤重金属污染与人体健康. 环境与发展, 2016, 28(1): 122-124.] |
| [64] |
Song NN, Wang FL, Tang SR et al. Assessment of lead bioavailability by Diffusive Gradients in Thin Films(DGT) in mulberry fields of Guangxi Huanjiang River Basin, China. Journal of Agricultural Environmental Science, 2012, 31(7): 1317-1323. [宋宁宁, 王芳丽, 唐世荣等. 基于梯度薄膜扩散技术的广西环江流域桑田土壤中铅的生物有效性研究. 农业环境科学学报, 2012, 31(7): 1317-1323.] |
| [65] |
Zhang XL, Qiao YH, Li HF. Adsorption of different heavy metal ions in solution system by corn stalk-based biochar. Journal of China Agricultural University, 2018, 23(5): 15-21. [张小玲, 乔玉辉, 李花粉. 玉米秸秆生物炭对溶液体系中不同重金属离子的吸附特性. 中国农业大学学报, 2018, 23(5): 15-21.] |
 2020, Vol. 32
2020, Vol. 32 

