(2: 中国科学院大学, 北京 100049)
(2: University of Chinese Academy of Sciences, Beijing 100049, P. R. China)
溶解性有机质(DOM)是指能通过某一特定孔径滤膜(0.10 ~0.45 μm)的有机物质,其来源主要有藻源(浮游植物的生长代谢)和陆源(陆地和大气输入)两种[1-2]. DOM在自然水体中广泛存在,其在海水中浓度约为0.2~3.6 mg/L,而在河流和湖泊等表层水体中可高达2~42 mg/L[3-5]. 近年来,由于人类活动以及水体点源/非点源污染负荷增加,环境水体中DOM浓度有逐渐升高趋势,严重影响水体水质生态健康[6-7]. 此外,在饮用水处理过程中,DOM与氯消毒剂反应生成的三氯甲烷、卤代乙腈等消毒副产物危害居民饮水健康[8]. 由于DOM的高活性和多基团特征,其在水体中具有吸附/解吸、分散/团聚、稳定/降解等环境行为,其中光降解是其转化过程中的重要途径[9-11]. DOM在光照条件下产生活性氧自由基,可显著影响污染物的化学形态和生物可利用性[12]. 因此,环境水体DOM的光降解特性研究是水环境领域的热点问题.
DOM可吸收光子直接光解,也可与由其他光活性物质吸光后产生的光活性中间产物发生间接光解. 环境水体中DOM以胶体或纳米颗粒为介导的光解是典型的间接光解. 近年来,人工纳米胶体颗粒(如TiO2、ZnO)的广泛使用及沉积物再悬浮等过程使水体中含有大量的胶体/纳米颗粒(< 100 nm)[13-14],从而影响DOM的光降解行为及效率. 一方面胶体颗粒粒径小、比表面积大,可通过表面吸附位点和基团吸附作用抑制DOM降解[15];另一方面,光照条件下胶体颗粒界面自身会产生大量的活性氧物质,从而提高DOM的光降解效率[16]. 上述研究均是将DOM样品作为“整体”来考虑,没有考虑DOM分子量不同而引起的环境效应差异. 虽然已有关于分子量的光降解研究,但是由于缺乏系统的分级分离方法,并未区分DOM样品的胶体态(0.45 μm~1 kDa)和真溶态(< 1 kDa),故无法解释DOM样品中胶体态和真溶态组分显著不同的环境行为和效益[17]. 所以,开展基于分子量差异的环境水体DOM光降解特性研究,可加深理解环境水体DOM的归趋效应及行为过程,也可为污染水体高效修复和净化技术研发提供理论指导.
本文选取湖泊蓝藻新陈代谢过程中释放的藻源有机质(algal-derived organic matter,AlgOM)和国际腐殖质协会提供的Suwannee河天然有机质(natural organic matter,NOM)为典型藻源和陆源有机质样品[18-19],选取纳米级TiO2为胶体颗粒的代表,采用切向超滤技术将初始DOM样品分为低分子量(low molecular weight, LMW, < 1 kDa)和高分子量(high molecular weight, HMW, 1 kDa~0.45 μm)组分. 采用总有机质分析仪、紫外-可见吸收光谱仪和荧光光谱分析仪测定光降解过程中有机质含量和组分变化,结合拟一级动力学模型,阐明基于分子量差异的不同来源DOM的光降解特性.
1 材料与方法 1.1 实验材料于2019年10月份在太湖(30°55′40″~31°32′58″N,119°52′32″~120°36′10″E)采集蓝藻水样,低温保存并于6 h内运至实验室,采用热-离心法获得AlgOM样品[20],4℃低温储存待用. NOM购买于国际腐殖质协会,产品型号为2R101N. 胶体TiO2颗粒购于南京先丰纳米材料科技有限公司,纯度>99 %,平均粒径为10 nm.
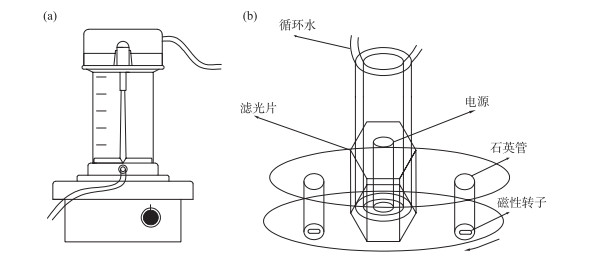
1.2 DOM的分子量分级采用切向超滤设备(默克公司,搅拌式超滤杯)对DOM进行分子量分级(图 1a). 为消除背景污染,超滤前先用0.05 mol/L NaOH和0.02 mol/L HCl清洗滤芯,再用超纯水多次冲洗设备. 选用孔径为1 kDa的超滤膜(默克公司,PLAC07610)以获取不同分子量DOM. 将DOM原样(Bulk-DOM)倒入搅拌室中连续搅拌(150 r/min),同时设置氮气压力和浓缩系数分别为345 kPa和40[21]. 透过超滤膜的渗透液为LMW-DOM(< 1 kDa),而截留在滤膜上的有机质稀释至初始体积,则为HMW-DOM(1 kDa~0.45 μm)[22],收集LMW-DOM和HMW-DOM样品于4℃低温储存待用.
|
图 1 搅拌式超滤杯(a)和XPA-1型旋转式光化学反应仪(b) Fig.1 Stirring ultrafiltration cell(a) and XPA-1 rotary photochemical reactor(b) |
为考察不同DOM来源(藻源和陆源)、不同分子量(Bulk、HMW和LMW)及有无TiO2胶体颗粒条件下DOM的光降解特性,DOM的光降解实验在XPA-1型旋转式光化学反应仪(南京胥江机电厂)中进行(图 1b). 选择300 W中压汞灯并配置290 nm滤光片为实验光源,光解溶液中心平均辐照度为1317 μW/cm2. 无胶体颗粒条件下,直接将DOM反应溶液置于光化学反应仪进行光降解,分别于0、0.5、1、2、4、8、12、24 h采集样品并低温储存;然而对于有胶体颗粒条件下(TiO2:0.3 g/L[23]),先将胶体颗粒与DOM溶液在黑暗条件下混合反应2 h,确保不同分子量DOM在胶体颗粒表面达到吸附平衡后进行光降解,且采集的样品需过0.45 μm的滤膜去除团聚的胶体颗粒. 在黑暗条件下,DOM与胶体颗粒的吸附过程在10 min内达到平衡[23],因此胶体颗粒存在下的吸附实验时间设定为2 h. 每个处理组设3个平行实验.
1.4 分析方法采用总有机质分析仪(TOC-400,Shimadzu,日本)测定DOM中溶解有机碳(DOC)含量. 采用紫外-可见吸收光谱仪(Agilent 8453,美国)测定DOM的吸收光谱(以Mill-Q水空白),扫描范围为200~800 nm,间隔波长1 nm. 本文采用254 nm波长下的单位吸光度值SUVA(254)表征DOM的芳香性,SUVA(254)按公式(1)~(2)进行计算[24]:
| $ \begin{aligned} a(254)=2.303 A(254) / L \end{aligned} $ | (1) |
| $ S U V A(254)=A(254) / D O C $ | (2) |
式中,a(254)是254 nm处的吸收系数(m-1),A(254)为254 nm处的吸光度,L为0.01 m,DOC为DOM的有机碳浓度(mg/L).
采用日立F-7000荧光光谱分析仪(Hitachi,日本)测定DOM的三维荧光光谱. 激发波长(Ex)和发射波长(Em)的扫描区间分别为200~450和250~550 nm,步长分别为10和2 nm,扫描速度为1400 nm/min,激发和发射单色仪的带宽裂缝分别为10和5 nm. 扫描光谱进行仪器自动校正,以Mill-Q水为空白.
采用拟一级动力学模型计算DOM的光降解速率[25]:
| $ \ln \left(C_{t} / C_{0}\right)=-k \cdot t+A $ | (3) |
式中,Ct为t时刻DOM浓度(以DOC和a(254)表示),C0为0 h时DOM浓度,t为光照时间(h),k为一级动力学常数(h-1),A为常数.
根据以下公式计算胶体颗粒存在时吸附(R吸附)、光解吸(R光解吸)和光降解(R光降解、R净光降解)所占的百分比[26]:
| $ \begin{gathered} R_{\text {吸附 }}=100\left(C_{0}-C_{\text {ads }}\right) / C_{0} \end{gathered} $ | (4) |
| $ R_{\text {光解吸 }}=100\left(C_{\text {des }}-C_{\text {ads }}\right) /\left(C_{0}-C_{\text {ads }}\right) $ | (5) |
| $ R_{\text {光降解 }}=\left(C_{\text {ads }}-C_{\mathrm{e}}\right) / C_{0} $ | (6) |
| $ R_{\text {净光降解 }}=\left(C_{\mathrm{ads}}-C_{\mathrm{e}}\right) / C_{\mathrm{ads}} $ | (7) |
式中,Cads是吸附过程结束时DOM的浓度,Cdes是最大光解吸时DOM的浓度,Ce是光降解结束时DOM的浓度,R光降解为胶体颗粒存在下DOM的光降解效率,R净光降解为扣除吸附影响后DOM的光降解效率.
1.5 统计分析运用SPSS 22软件进行均值、标准差、组件方差等数据统计分析,使用Origin 2018软件绘图并对样品进行一级动力学拟合,并绘制三维荧光光谱.
2 结果和讨论 2.1 基于分子量差异的不同来源DOM的丰度和组成无胶体颗粒时,不同来源DOM的有机质浓度与分子量分布如图 2a所示. AlgOM样品中LMW组分的DOC占比为55.3 % ±0.30 %,NOM样品中LMW组分的DOC占比为57.8 % ±0.50 %. 说明AlgOM和NOM有机质相对较多地分布在 < 1 kDa的低分子相(真溶态)中,这与福克斯河(~60 %)、密歇根湖(60 % ~70 %)和墨西哥北部湾(70 % ~80 %)等水生生态系统中DOM的有机质分布结果基本一致[21].

|
图 2 基于分子量差异的不同来源DOM的DOC浓度分布(a)和经DOC归一化的紫外-可见吸收光谱a(b)及三维荧光光谱(c) (a为了避免不同分子量DOM的初始浓度不同对结果比较造成影响,对吸收系数进行DOC归一化: a(λ)/DOC,a(λ)为λ波长下的吸收系数) Fig.2 The DOC concentration distribution(a), DOC normalized UV-visible absorbance spectrum a(b) and EEM(c) of DOM with different source based on molecular weight fractionation |
紫外-可见吸收光谱结果表明,无论是LMW还是HMW组分,NOM的SUVA(254)值均大于AlgOM(图 2b). NOM含有大量腐殖质及木质素类结构物质,而AlgOM则以多糖和蛋白质为主[27],因此NOM比AlgOM具有更高的芳香性. 此外,不管是AlgOM还是NOM,SUVA(254)值的高低顺序均为HMW>Bulk>LMW,表明HMW组分比Bulk和LMW组分具有更高的芳香性.
为表征不同来源DOM中荧光物质的类别及其在不同分子量的分布规律,对不同来源DOM的三维荧光光谱(图 2c)进行特征分析. 结果发现,AlgOM样品包括5个荧光峰,分别为2个类蛋白峰[Ex/Em=(220~250)/(280~380) nm, (250~280)/(280~380) nm]和3个类腐殖峰[Ex/Em=(230~250)/(400~500) nm, (250~280)/(400~500) nm, (320~350)/(400~500) nm][28-30],而NOM样品仅含有2个类腐殖峰[Ex/Em=(220~280)/(400~500 nm), (300~350)/(400~500) nm)][31-32]. 因此AlgOM富含类蛋白和类腐殖物质,而NOM只含有类腐殖物质. 此外,不同分子量DOM的三维荧光光谱表明,类蛋白物质主要分布于HMW组分,而类腐殖物质则主要分布于LMW组分.
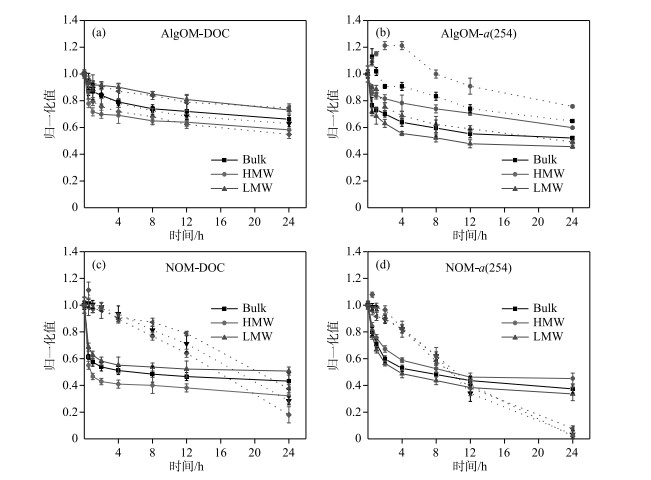
2.2 光降解过程中DOC的变化 2.2.1 TiO2胶体颗粒对DOM光降解效率的影响DOM含有大量的光吸收基团,具有光敏性特征,因此即使在无胶体颗粒条件下,不同分子量AlgOM和NOM的有机质含量均有所下降(图 3a和c). 根据表 1可知,在无胶体颗粒条件下,不同分子量AlgOM有机质的光降解效率为26.92 % ~41.73 %,而NOM有机质的光降解效率为49.30 % ~67.85 %;拟一级动力学模型结果显示,各分子量AlgOM有机质的光降解速率为0.32~1.22 h-1(R2>0.85),而NOM有机质的光降解速率为1.98~2.45 h-1(R2>0.96),NOM有机质的光降解速率明显高于AlgOM,这是NOM和AlgOM的光敏性不同所导致的. 有研究表明,NOM的有机质具有更高的光敏性[18],故NOM表现出更高的光降解效率和速率.
|
图 3 不同分子量AlgOM和NOM的光降解曲线((a)和(c)为AlgOM和NOM归一化b后的DOC曲线,(b)和(d)为AlgOM和NOM归一化后a(254)的曲线(实线表示无胶体颗粒,虚线表示有胶体颗粒)) (b为避免不同分子量DOM的初始浓度差异对实验结果造成影响,对DOC和a(254)值进行归一化:Ct/C0) Fig.3 The photodegradation curves of AlgOM and NOM with different molecular weights during the photodegradation process((a) and (c) are the normalized DOC curves of AlgOM and NOM, (b) and (d) are the normalized a(254) curves of AlgOM and NOM(The solid line represented no colloidal particles, and the dotted line represented colloidal particles) |
| 表 1 无TiO2胶体颗粒条件下不同分子量AlgOM和NOM的光降解效率及速率 Tab. 1 Photodegradation efficiency and rate of AlgOM and NOM with different molecular weights in the absence of TiO2 colloidal particles |
在胶体颗粒存在情况下,各分子量AlgOM有机质的R光降解为21.78 % ~27.92 %,同样低于NOM的R光降解(56.96 % ~63.12 %). 由于胶体颗粒的影响,AlgOM有机质的R光降解相比于无胶体颗粒存在时有所降低,而NOM有机质的R光降解有所提高. 以Bulk-DOM为例,在无胶体颗粒时,Bulk-AlgOM中有机质R光降解为33.81 %,加入胶体颗粒后Bulk-AlgOM中有机质总去除率为52.42 %,其中R吸附和R光降解分别为24.50 % 和27.92 %,Bulk-AlgOM有机质的R光降解明显降低,说明胶体颗粒对AlgOM有机质的吸附作用抑制了其光降解. 而在无胶体颗粒时,NOM中有机质R光降解为56.85 %;加入胶体颗粒后,Bulk-NOM有机质的总去除率为74.91 %,其中R吸附和R光降解分别为11.79 % 和63.12 %,Bulk-NOM有机质的R光降解明显增大,说明胶体颗粒促进了NOM有机质的光降解. 已有研究表明AlgOM中类蛋白组分在胶体颗粒表面上的吸附能力强于类腐殖质物质[33],本研究AlgOM中被吸附组分在光降解阶段未发生光解吸,也证明其具有更强的吸附性能. 因此,胶体颗粒通过吸附作用抑制了AlgOM有机质的光降解. TiO2胶体颗粒对AlgOM吸附作用减小其微孔表面积,不利于形成电子-空穴对,从而降低羟基自由基对AlgOM的攻击效率[34-35]. NOM主要是类腐殖物质吸附在胶体颗粒表面,在光降解初始阶段出现光解吸现象,且该过程不符合一级动力学模型,说明其在胶体颗粒表面呈现弱吸附特性. 所以,NOM有机质光降解效率的提高归因于胶体颗粒的催化作用,胶体颗粒表面的光致电子和空穴分别有强还原和氧化能力,产生的羟基自由基能够通过脱氢和加成反应光催化降解有机物[36].
2.2.2 DOM分子量对光降解效率的影响无胶体颗粒条件下,不管是AlgOM还是NOM,HMW组分的光降解效率明显高于LMW和Bulk组分,且HMW有机质的光降解主要集中在初始阶段4 h内(图 3a, c). 拟一级动力学模型拟合结果表明,不同分子量有机质的光降解速率顺序为HMW>Bulk>LMW(表 1),说明HMW有机组分优先降解. 胶体颗粒存在条件下不同分子量DOM的R光降解顺序为HMW>Bulk>LMW,与无胶体颗粒存在下光降解顺序一致,表明胶体颗粒的存在并没有影响各分子量DOM光降解效率的顺序. 不同分子量DOM在胶体颗粒表面的吸附量顺序为HMW>Bulk>LMW(表 2). 与LMW有机质相比,AlgOM中HMW有机质含有的大分子类蛋白物质优先吸附在胶体颗粒表面;NOM中无类蛋白物质,主要是具有高疏水性和多官能团的HMW有机质竞争胶体颗粒表面吸附位点[37]. 吸附在胶体颗粒表面的HMW-NOM有机质不仅能被胶体颗粒表面产生的光生空穴直接氧化分解,还可通过电荷转移产生具有强氧化能力的羟基自由基间接分解,因此部分被吸附的HMW-NOM有机质在光降解初级阶段不完全矿化,从胶体颗粒表面解吸,但随着光照时间增加迅速降解.
| 表 2 TiO2胶体颗粒存在条件下不同分子量AlgOM和NOM的吸附、光降解、光解吸及总去除率 Tab. 2 Adsorption, photodegradation, photo-desorption and total removal efficiency of AlgOM and NOM with different molecular weights in the presence of TiO2 colloidal particles |
UV254是表征DOM中芳香性物质含量的重要指标,a(254)为其换算后的吸收系数[38-39]. 无胶体颗粒存在条件下,Bulk-AlgOM中芳香性物质的光降解效率和速率均大于Bulk-NOM(表 1),说明Bulk-AlgOM中的芳香性物质具有更高的光敏性. 胶体颗粒的存在明显降低Bulk-AlgOM中芳香性物质的光降解效率,却明显提高Bulk-NOM中芳香性物质的光降解效率(图 3b,d). 表 2显示Bulk-AlgOM芳香性物质的总去除率为66.65 %,其中R吸附和R光降解分别为42.55 % 和24.12 %,说明胶体颗粒对AlgOM芳香性物质的吸附作用抑制了其光降解. 而Bulk-NOM的总去除率为93.97 %,其中R吸附和R光降解分别为14.62 % 和79.35 %,说明胶体颗粒对NOM芳香性物质的催化作用促进其光降解,这与基于DOC的分析结果一致.
当扣除胶体颗粒吸附影响后,NOM基于a(254)计算的R净光降解(92.22 % ~98.02 %)比基于DOC分析结果(62.51 % ~82.03 %)高(表 3). 说明与非芳香性物质相比,DOM中芳香性物质具有更强的光吸收能力. 此外,实验过程中还发现,不管是AlgOM还是NOM,光降解初始阶段HMW-DOM的a(254)均略有升高,这与基于DOC的分析结果(图 3c)和其他已有研究结果一致[40]. 其原因可能是光降解初始阶段部分大分子芳香性物质在胶体颗粒表面分解为小分子亲水性芳香族化合物,使得溶液中芳香性物质含量短暂升高.
| 表 3 扣除TiO2胶体颗粒吸附影响后不同分子量AlgOM和NOM的净光降解效率 Tab. 3 Photodegradation efficiency of AlgOM and NOM with different molecular weights after the reduction of the effect of TiO2 colloidal particles adsorption |
进一步研究发现,无胶体颗粒条件下,不同分子量AlgOM和NOM芳香性物质的光降解效率和速率顺序均为LMW>Bulk>HMW,表明低分子量芳香性物质在光照条件下优先降解. 胶体颗粒存在条件下,不同分子量AlgOM中的芳香性物质光降解效率顺序与无胶体颗粒时一致,而NOM芳香性物质的光降解效率顺序则变为HMW->Bulk->LMW-NOM,表明胶体颗粒的存在可改变不同分子量NOM中芳香性物质的光降解效率顺序. 上述结果表明,环境水体中不同分子量DOM中芳香性物质的光降解顺序与DOM来源和有无TiO2胶体颗粒存在密切关系.
2.4 光降解过程中不同荧光物质的变化根据不同类型有机质三维荧光光谱特征(图 1c),选取AlgOM样品的类腐殖荧光峰[(Ex/Em=(250~280)/(280~380) nm)]、以及NOM样品的类腐殖荧光峰[Ex/Em=(220~280)/(400~500) nm]为代表性藻源和陆源类腐殖质荧光组分,比较其在不同光降解过程中荧光强度的变化. 无胶体颗粒存在条件下,藻源类腐殖物质的光降解效率和速率分别40.59 % ~67.81 % 和0.19~0.30 h-1,陆源类腐殖物质的光降解效率和速率分别60.73 % ~63.68 % 和0.84~0.92 h-1(表 4). 陆源类腐殖质物质的光降解效率和速率明显高于藻源类腐殖质,说明陆源类腐殖质更易光降解. 在此条件下,无论是藻源还是陆源类腐殖质,不同分子量的光降解效率和速率顺序均为LMW>Bulk>HMW,表明LMW类腐殖质具有较高的光敏性并具有优先降解特性.
| 表 4 不同来源类腐殖物质荧光峰强减少效率及速率 Tab. 4 Efficiency and rate of reduction of fluorescence peak intensity of humic-like substances from different sources |
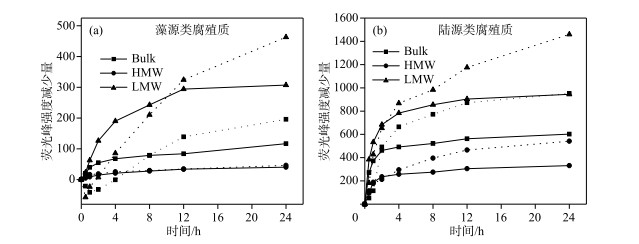
根据图 4可知,胶体颗粒存在下,无论是Bulk-藻源还是陆源类荧光峰强减少量都有所增加,说明胶体颗粒能够促进藻源和陆源类腐殖质的光降解. 其中,不同分子量陆源类腐殖质荧光峰强减少97.92 % ~99.21 % (表 4),说明陆源类腐殖质物质几乎完全光降解. 此外,不同分子量藻源和陆源类腐殖质荧光峰降低量顺序为LMW>Bulk>HMW,同样表明低分子量类腐殖质更易光降解.
|
图 4 藻源类腐殖质(a)和陆源类腐殖质(b)荧光峰强减少量(实线表示无胶体颗粒,虚线表示有胶体颗粒) Fig.4 Reduction of fluorescence peak intensity of humic substances from algal-derived humus-like substances(a), and terrestrial humus-like substances(b) (The solid line represented no colloidal particles, and the dotted line represented colloidal particles) |
虽然关于DOM的吸附和光降解研究已有大量报道,但是本文关注胶体颗粒存在条件下不同来源及不同分子量DOM的光降解差异,这在已有研究中鲜有关注,且本文的研究结果具有明显的环境意义. 例如,与深水湖泊相比,浅水湖泊由于易受风浪湖流扰动和沉积物再悬浮影响,故浅水湖泊水体往往含有高浓度的胶体颗粒[13]. 本文的研究结果表明,胶体颗粒存在时可显著改变DOM的光降解效率和组成,因此浅水湖泊与深水湖泊水体中DOM的光降解效率和组成也具有显著差异性. 此外,本研究结果还发现,藻源DOM与陆源DOM的吸附和光降解过程也存在显著差异,因此可以推测富营养化湖泊(藻源DOM为主)与贫富营养湖泊(非藻源DOM为主)水体中DOM具有显著不同的环境行为(如吸附、光降解特征).
环境水体中DOM可与金属离子发生络合作用形成金属-DOM络合物,改变金属的形态并进而影响金属离子的迁移转化途径和生物有效性[41]. 但是,这些研究仅关注特定的DOM样品,没有关注DOM不同分子量信息,也没有考虑不同来源DOM的光降解对金属吸附影响. 而本研究发现胶体颗粒的存在可通过催化作用促进NOM中有机质及芳香性物质的光降解,通过吸附作用抑制AlgOM中有机质及芳香性物质的光降解. 故胶体颗粒的存在可能会促进NOM-金属络合物中金属离子的释放,而对AlgOM-金属络合物中金属离子的释放无显著影响. 所以,胶体颗粒的存在除影响DOM的光降解特征外,可能还会影响水体其他污染物的环境行为及效应.
4 结论1) NOM比AlgOM具有更高的芳香性并含有更多的类腐殖物质. 不管是NOM还是AlgOM,虽然LMW组分有机质含量约占有机质总量的50 % ~60 %,但HMW组分具有更高的芳香性;另外,类蛋白物质主要分布于HMW中,而类腐殖物质主要分布于LMW中.
2) 基于DOC分析,无胶体颗粒条件下,NOM的有机质比AlgOM的有机质具有更高的光敏性;无论是NOM还是AlgOM,不同分子量有机质的光降解效率和速率顺序均为HMW>Bulk>LMW. 虽然胶体颗粒的存在不改变不同分子量有机质的光降解顺序,但其通过吸附作用抑制AlgOM中有机质的光降解,而通过催化作用促进NOM中有机质的光降解.
3) 基于a(254)分析,无胶体颗粒条件下,AlgOM的芳香性物质比NOM的芳香性物质具有更高的光敏性;无论是NOM还是AlgOM,不同分子量芳香性物质的光降解效率和速率均为LMW>Bulk>HMW. 胶体颗粒的存在不改变不同分子量AlgOM中芳香性物质的光降解顺序,但通过吸附作用抑制其光降解;胶体颗粒的存在不仅改变不同分子量NOM芳香性物质的光降解顺序,还通过催化作用促进其光降解.
4) 通过三维荧光光谱分析,无胶体颗粒存在条件下,陆源类腐殖物质比藻源类腐殖物质更易光降解;无论是藻源还是陆源,不同分子量类腐殖物质的光降解效率和速率均为LMW>Bulk>HMW. 此外,胶体颗粒的存在可促进不同分子量藻源和陆源类腐殖质物质的光降解.
| [1] |
Chin WC, Orellana MV, Verdugo P. Spontaneous assembly of marine dissolved organic matter into polymer gels. Nature, 1998, 391(6667): 568-572. DOI:10.1038/35345 |
| [2] |
He W, Bai ZL, Li YL et al. Advances in the characteristics analysis and source identification of the dissolved organic matter. Acta Scientiae Circumstantiae, 2016, 36(2): 359-372. [何伟, 白泽琳, 李一龙等. 溶解性有机质特性分析与来源解析的研究进展. 环境科学学报, 2016, 36(2): 359-372. DOI:10.13671/j.hjkxxb.2015.0117] |
| [3] |
Hosen JD, Aho KS, Fair JH et al. Source switching maintains dissolved organic matter chemostasis across discharge levels in a large temperate river network. Ecosystems, 2020, 1-21. DOI:10.1007/s10021-020-00514-7 |
| [4] |
Wang WW, Zheng BH, Jiang X et al. Characteristics and source of dissolved organic matter in lake Hulun, A large shallow eutrophic steppe lake in Northern China. Water, 2020, 12(4): 953. DOI:10.3390/w12040953 |
| [5] |
Ducklow HW, Hansell DA, Morgan JA. Dissolved organic carbon and nitrogen in the Western Black Sea. Marine Chemistry, 2007, 105(1/2): 140-150. DOI:10.1016/j.marchem.2007.01.015 |
| [6] |
Shafiquzzaman M, Haider H, Bhuiyan MA et al. Spatiotemporal variations of DOM components in the Kushiro River impacted by a wetland. Environmental Science and Pollution Research, 2020, 27(15): 18287-18302. DOI:10.1007/s11356-020-08192-7 |
| [7] |
Yu HB, Song YH, Gao HJ et al. Applying fluorescence spectroscopy and multivariable analysis to characterize structural composition of dissolved organic matter and its correlation with water quality in an urban river. Environmental Earth Sciences, 2015, 73(9): 5163-5171. DOI:10.1007/s12665-015-4269-y |
| [8] |
Yan YW, Zhai HY, Wang XJ. Formation characteristics of disinfection by-products from algal organic matter in ozonation/chlorine disinfection. China Water & Wastewater, 2020, 36(5): 7-13. [闫雨薇, 翟洪艳, 王雪娇. 臭氧/氯消毒中藻类有机物生成消毒副产物的特征. 中国给水排水, 2020, 36(5): 7-13. DOI:10.19853/j.zgjsps.1000-4602.2020.05.002] |
| [9] |
Wu DM, Li QF, Wu CY. Adsorption of dissolved organic matter onferrallitic soils. Environmental Chemistry, 2016, 35(4): 639-650. [吴东明, 李勤奋, 武春媛. 铁铝土对溶解性有机质的吸附特性. 环境化学, 2016, 35(4): 639-650.] |
| [10] |
Hu B, Wang PF, Bao TL et al. The photochemical release of dissolved organic matter from resuspended sediments: Insights from fluorescence spectroscopy. Chemosphere, 2020, 257: 127161. DOI:10.1016/j.chemosphere.2020.127161 |
| [11] |
Xue S, Wang C, Ma XP et al. Photodegradation of dissolved organic matter fractions in ice under natural solar radiation. Acta Scientiae Circumstantiae, 2015, 35(10): 3098-3106. [薛爽, 王超, 马溪平等. 天然太阳辐射作用下冰体中溶解性有机物组分的光降解. 环境科学学报, 2015, 35(10): 3098-3106. DOI:10.13671/j.hjkxxb.2015.0040] |
| [12] |
Gourlay C, Tusseau-Vuillemin MH, Mouchel JM et al. The ability of dissolved organic matter (DOM) to influence benzo[a]Pyrene bioavailability increases with DOM biodegradation. Ecotoxicology and Environmental Safety, 2005, 61(1): 74-82. DOI:10.1016/j.ecoenv.2004.12.005 |
| [13] |
Xu HC, Xu MW, Li YN et al. Characterization, origin and aggregation behavior of colloids in eutrophic shallow lake. Water Research, 2018, 142: 176-186. DOI:10.1016/j.watres.2018.05.059 |
| [14] |
Ju-Nam Y, Lead JR. Manufactured nanoparticles: An overview of their chemistry, interactions and potential environmental implications. Science of the Total Environment, 2008, 400(1/2/3): 396-414. DOI:10.1016/j.scitotenv.2008.06.042 |
| [15] |
Wei LL, Ding J, Xue M et al. Adsorption mechanism of ZnO and CuO nanoparticles on two typical sludge EPS: Effect of nanoparticle diameter and fractional EPS polarity on binding. Chemosphere, 2019, 214: 210-219. DOI:10.1016/j.chemosphere.2018.09.093 |
| [16] |
Lee PF, Sun DD, Leckie JO. Adsorption and photodegradation of humic acids by nano-structured TiO2 for water treatment. Journal of Advanced Oxidation Technologies, 2007, 10(1): 72-78. DOI:10.1515/jaots-2007-0112 |
| [17] |
Chen ZJ, Huang GC, Meng FG. Photochemical degradation of the size-fractionated dissolved organic matter. Chemistry, 2018, 81(3): 236-240. [陈子健, 黄国城, 孟凡刚. 不同分子尺寸溶解性有机物的光解行为研究. 化学通报: 印刷版, 2018, 81(3): 236-240.] |
| [18] |
Yang XF, Zheng X, Wu LJ et al. Interactions between algal (AOM) and natural organic matter (NOM): Impacts on their photodegradation in surface waters. Environmental Pollution, 2018, 242: 1185-1197. DOI:10.1016/j.envpol.2018.07.099 |
| [19] |
Cawley KM, McKnight DM, Miller P et al. Characterization of fulvic acid fractions of dissolved organic matter during ice-out in a hyper-eutrophic, coastal pond in Antarctica. Environmental Research Letters, 2013, 8(4): 045015. DOI:10.1088/1748-9326/8/4/045015 |
| [20] |
Xu HC, Yang CM, Jiang HL. Aggregation kinetics of inorganic colloids in eutrophic shallow lakes: Influence of cyanobacterial extracellular polymeric substances and electrolyte cations. Water Research, 2016, 106: 344-351. DOI:10.1016/j.watres.2016.10.023 |
| [21] |
Xu HC, Guo LD. Molecular size-dependent abundance and composition of dissolved organic matter in river, lake and sea waters. Water Research, 2017, 117: 115-126. DOI:10.1016/j.watres.2017.04.006 |
| [22] |
Xu HC, Zou L, Guan DX et al. Molecular weight-dependent spectral and metal binding properties of sediment dissolved organic matter from different origins. Science of the Total Environment, 2019, 665: 828-835. DOI:10.1016/j.scitotenv.2019.02.186 |
| [23] |
Huang XH, Leal M, Li QL. Degradation of natural organic matter by TiO2 photocatalytic oxidation and its effect on fouling of low-pressure membranes. Water Research, 2008, 42(4/5): 1142-1150. DOI:10.1016/j.watres.2007.08.030 |
| [24] |
Ma XL, Liu GM, Wu XD et al. Bioavailability of dissolved organic carbon in rivers for typical vegetation types in the permafrost regions on the Qinghai-Tibet plateau. Environmental Science, 2018, 39(5): 2086-2094. [马小亮, 刘桂民, 吴晓东等. 青藏高原多年冻土区典型植被下河流溶解性有机碳的生物可利用性. 环境科学, 2018, 39(5): 2086-2094. DOI:10.13227/j.hjkx.201709280] |
| [25] |
Guo WD, Cheng YY. Photodegradation of chromophoric dissolved organic matter from Jiulong River Estuary under natural solar radiation. Environmental Science, 2008, 29(6): 1463-1468. [郭卫东, 程远月. 天然日光辐照下河口区CDOM的光化学降解. 环境科学, 2008, 29(6): 1463-1468. DOI:10.13227/j.hjkx.2008.06.007] |
| [26] |
Shahid M, Saliby IE, McDonagh A et al. Photodesorption of specific organic compounds from titanium dioxide particles in aqueous media. Desalination and Water Treatment, 2014, 52(4/5/6): 867-872. DOI:10.1080/19443994.2013.826407 |
| [27] |
Chu HQ, Yu H, Tan XB et al. Extraction procedure optimization and the characteristics of dissolved extracellular organic matter (dEOM) and bound extracellular organic matter (bEOM) from Chlorella pyrenoidosa. Colloids and Surfaces B: Biointerfaces, 2015, 125: 238-246. DOI:10.1016/j.colsurfb.2014.08.007 |
| [28] |
Wang D, Zhang F, Zhang ZY et al. Characteristics of three-dimensional fluorescence spectra and its correlati- on with water quality of surface water during dry and wet seasons in Lake Ebinur Watershed, Xinjiang. J Lake Sci, 2020, 32(2): 483-495. [王迪, 张飞, 张兆永等. 新疆艾比湖流域枯、丰水期三维荧光光谱特性及其与水质的关系. 湖泊科学, 2020, 32(2): 483-495. DOI:10.18307/2020.0217] |
| [29] |
Xu HC, Cai HY, Yu GH et al. Insights into extracellular polymeric substances of cyanobacterium Microcystis aeruginosa using fractionation procedure and parallel factor analysis. Water Research, 2013, 47(6): 2005-2014. DOI:10.1016/j.watres.2013.01.019 |
| [30] |
Shammi M, Pan XL, Mostofa KMG et al. Investigating extracellular polymeric substances from microbial mat upon exposure to sunlight. Polymer Degradation and Stability, 2017, 146: 192-200. DOI:10.1016/j.polymdegradstab.2017.10.011 |
| [31] |
Nam SN, Amy G. Differentiation of wastewater effluent organic matter (EfOM) from natural organic matter (NOM) using multiple analytical techniques. Water Science and Technology, 2008, 57(7): 1009-1015. DOI:10.2166/wst.2008.165 |
| [32] |
Brezinski K, Gorczyca B. An overview of the uses of high performance size exclusion chromatography (HPSEC) in the characterization of natural organic matter (NOM) in potable water, and ion-exchange applications. Chemosphere, 2019, 217: 122-139. DOI:10.1016/j.chemosphere.2018.10.028 |
| [33] |
Lee BM, Hur J. Adsorption behavior of extracellular polymeric substances on graphene materials explored by fluorescence spectroscopy and two-dimensional Fourier transform infrared correlation spectroscopy. Environmental Science & Technology, 2016, 50(14): 7364-7372. DOI:10.1021/acs.est.6b01286 |
| [34] |
Li S, Sun WL. A comparative study on aggregation/sedimentation of TiO2 nanoparticles in mono- and binary systems of fulvic acids and Fe(Ⅲ). Journal of Hazardous Materials, 2011, 197: 70-79. DOI:10.1016/j.jhazmat.2011.09.059 |
| [35] |
Yang K, Lin DH, Xing BS. Interactions ofhumic acid with nanosized inorganic oxides. Langmuir, 2009, 25(6): 3571-3576. DOI:10.1021/la803701b |
| [36] |
Zhang YB. Study on the experiment and mechanism of TiO2 photocatalytic degradation of methyl orange[Dissertation]. Guangdong: Guangdong University of Technology, 2002. [张音波. TiO2光催化降解甲基橙的试验及机理研究[学位论文]. 广东: 广东工业大学, 2002. ]
|
| [37] |
Xu HC, Ji L, Kong M et al. Molecular weight-dependent adsorption fractionation of natural organic matter on ferrihydrite colloids in aquatic environment. Chemical Engineering Journal, 2019, 363: 356-364. DOI:10.1016/j.cej.2019.01.154 |
| [38] |
Phong DD, Hur J. Insight into photocatalytic degradation of dissolved organic matter in UVA/TiO2 systems revealed by fluorescence EEM-PARAFAC. Water Research, 2015, 87: 119-126. DOI:10.1016/j.watres.2015.09.019 |
| [39] |
Zheng LC, Song ZF, Meng PP et al. Seasonal characterization and identification of dissolved organic matter (DOM) in the Pearl River, China. Environmental Science and Pollution Research, 2016, 23(8): 7462-7469. DOI:10.1007/s11356-015-5999-9 |
| [40] |
Sanly M, Lim M, Chiang K et al. A study on the removal of humic acid using advanced oxidation processes. Separation Science and Technology, 2007, 42(7): 1391-1404. DOI:10.1080/01496390701289799 |
| [41] |
Guo W, Dai JL, Wang RQ. Progress in the effect of dissolved organic matter on adsorption of heavy metals by soil. Chinese Journal of Soil Science, 2012, 43(3): 761-768. [郭微, 戴九兰, 王仁卿. 溶解性有机质影响土壤吸附重金属的研究进展. 土壤通报, 2012, 43(3): 761-768.] |
 2021, Vol. 33
2021, Vol. 33 


