(2: 南昌大学鄱阳湖环境与资源利用教育部重点实验室, 资源环境与化工学院, 南昌 330031)
(2: Key Laboratory of Poyang Lake Environment and Resource Utilization, Ministry of Education, School of Resource Environmental and Chemical Engineering, Nanchang University, Nanchang 330031, P. R. China)
近几十年来,随着“温室效应”引起的全球气候变化加剧,全球碳循环处于地球各圈层间相互连接与转化的枢纽和核心地位,是全球物质能量循环与气候变化的关键,对维持生物圈功能和结构具有重要的作用[1]. 湖泊是内陆水体的自然单元之一,存储着丰富的区域性和全球性的环境变化信息,其面积虽远小于海洋,但其与陆地生态系统的物质、能量、信息交换更加强烈,对区域性和全球性气候变化的响应也更加敏感[2],湖泊每年的碳埋藏量占海洋碳埋藏量的25 % ~85 % [3-4],是陆地地表水碳元素的汇集地之一,同时也是重要的CO2释放源,因此,湖泊碳循环是全球碳循环的重要组成部分,也是碳循环研究的热点领域之一.
湖泊水体中的溶解无机碳不仅是湖泊碳通量的主要形式,而且在湖泊流域碳循环及水气碳通量交换中占有枢纽地位. 无机碳的浓度与湖泊富营养化水平存在直接或间接的联系,对水生态系统的养分可用性和生产力产生一定的影响,因此无机碳通量及其分布特征是水体碳循环研究的一个重要组成部分. 湖泊中碳酸钙的沉积对无机碳循环具有很大的作用;全世界范围内,碳酸盐型湖泊的总面积仅占非碳酸盐型湖泊总面积的1/9左右,但其对溶解无机碳(DIC) 的平均滞留率为非碳酸盐型湖泊的20倍[5]. 水体中DIC浓度及碳同位素分馏过程中δ13CDIC变化能够反映碳的地球化学行为和生物地球化学循环特征[6-9]. 众多学者对湖泊、河流溶解无机碳的来源[10-12]、水气交换通量估算[13]、CO2在表层水的行为[14]、碳与营养盐及水环境参数的关系[15]、沉积物与DIC碳同位素关系[16]等方面进行了大量的研究. 湖泊DIC来源主要包括河流输入、降水、碳酸盐分解以及水气直接交换等,Marsh等[17]研究南极洲温特塞(Untersee)湖中的主要溶质和碳的来源,表明湖水中DIC主要来源于河流输入和水气交换;Richey等[18]对4个湖泊系统碳进行研究,结果表明湖泊碳除从地表径流、地下水获得以外,还可从大气中获取;Hope等[19]在研究美国威斯康星州27个湖泊表层水CO2的分压和溶解有机碳关系时发现湖泊中碳主要来源于流域的河流输入.
随着流域社会经济的发展,人类活动加剧,温室气体的排放及河流的输入,湖泊碳通量以及湖泊富营养化水平升高,流域内湖泊碳汇的作用越来越明显,有研究表明,内陆水体中的碳源/碳汇强度要高于海洋的碳源/碳汇强度[20],这是由于中国内陆水体大多为浅水湖泊,其碳循环具有较强的碳循环驱动因素,如湖泊生产力较高,水体循环周期较快,内陆水体中的碳酸盐浓度较高[21]. 鄱阳湖是中国最大的淡水湖泊,较强碳汇强度和较高生产力的湖泊水体对实现碳减排和缓解全球气候变暖具有重要的意义. 前人对该湖泊碳循环的研究主要集中在沉积物[22]和湿地土壤[23],而对湖泊水体无机碳及其同位素的分布特征、来源及影响因素未作深入探讨,近年来鄱阳湖受流域人类活动的影响逐渐加剧,出现水位下降、水体富营养化加剧和湿地面积减少等现象. 因此,本文通过研究鄱阳湖水体DIC、δ13CDIC的时空分布特征及其与相关环境因子的关系,估算鄱阳湖无机碳通量,并基于碳同位素法分析不同碳源对鄱阳湖的贡献率,为探寻湖泊CO2的源汇、湖泊碳储备对气候变化的响应以及间接反映人类活动对全球气候变化的影响程度提供科学依据.
1 研究区域鄱阳湖(28°11′~29°51′N, 115°49′~116°46′E)位于江西省北部,承接赣江、抚河、信江、饶河、修水“五河”来水,调蓄后经湖口注入长江,是中国最大的淡水湖. 鄱阳湖是一个典型的过水型、吞吐型、季节型的湖泊,具有“高水是湖、低水似河”、“洪水一片、枯水一线”的水文特征. 鄱阳湖湖水补给的主要来源是河水和降水,其次是地下水,2016年5条水系的径流量占鄱阳湖总径流量的90.4 %.
鄱阳湖流域为典型的亚热带湿润季风气候,降水丰富,多年(1956-2016年)平均降雨量1645.8 mm. 降雨主要集中在4—6月,最低在1、2、12月. 鄱阳湖流域湖水和河水水化学主要为碳酸盐型,主要受岩石风化和降水径流作用的影响,对流域碳通量的输入和输出影响重大[24].
2 材料与方法 2.1 样品采集与分析于2019年2月(枯水期)和8月(丰水期)、2020年2月和8月在“五河”入湖口及湖区布设18个水样监测点(图 1),每个监测点每次采集1个水样,4次共采集72个水样. 现场使用HACH便携式分析仪(HQ40d,美国)测定水样的水温、pH、电导率等,使用0.05 mol/L稀盐酸以甲基橙为指示剂,现场测定碱度. 现场用针头式过滤器过滤100 mL滤液于聚乙烯瓶中,加入HgCl2毒化抑制微生物活动,不留气泡,用封口胶密封盖紧,冷藏,带回实验室测定δ13CDIC.
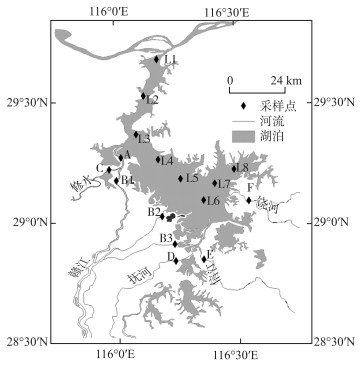
|
图 1 鄱阳湖水体采样点位分布(L1:湖口(出湖口);L2:星子;L3:老爷庙;L4:都昌;L5:主湖区1;L6:主湖区2;L7:周溪嘴;L8:西源;A:赣、修河混合后;B1:赣江北支入湖口;B2:赣江中支入湖口;B3:赣江南支入湖口;C:修河入湖口;D:抚河入湖口;E:信江入湖口;F:饶河入湖口) Fig.1 Distribution of sampling sites in Lake Poyang |
总氮(TN)浓度使用碱性过硫酸钾消解紫外分光光度法(HJ 636—2012)测定,总磷(TP)浓度使用钼酸铵分光光度法(GB 11893—1989)测定. δ13CDIC的测定依据Atekawana等[25]的方法,对样品进行预处理,使用自然资源部第三海洋研究所的气体稳定同位素质谱仪MAT253测定. 测定结果用千分比单位(‰),分析误差 < 0.1 ‰. δ13CDIC值以VPDB国际标准作为参考标准,按以下公式计算:
| $ {\mathtt{δ}}^{13} \mathrm{C}=\left[\frac{R\left({ }^{13} \mathrm{C} /{ }^{12} \mathrm{C}_{\text {sample }}\right)}{R\left({ }^{13} \mathrm{C} /{ }^{12} \mathrm{C}_{\mathrm{VPDB}}\right)}-1\right] \times 1000 $ | (1) |
式中,R(13C/12CVPDB)为国际标准物VPDB的碳同位素丰度比值,其值为0.0112372.
2.2 计算方法 2.2.1 溶解无机碳组成计算水体溶解无机碳由H2CO3、HCO3-、CO32-组成,根据水体中碳酸盐平衡体系中的pH值、碱度以及与水温相关的碳酸盐平衡体系的反应常数K1、K2和KCO2,计算水体DIC各组分的摩尔浓度和水中CO2分压pCO2[26].
2.2.2 河流水系输入溶解无机碳碳通量估算及贡献率水体输入无机碳通量及贡献率计算公式[27]如下:
| $ F_{i j}=12 \times 10^{-9} C_{i j} \cdot Q $ | (2) |
| $ X_{i}=F_{i j} / \sum\limits_{j=1} F_{i j} $ | (3) |
式中,Fij为DIC月通量(t);Cij为水体第i月份j点的DIC平均浓度(μmol/L);Q为月径流量(m3);12为摩尔质量转换系数(g/mol);Xi为DIC贡献率;10-9为单位转化系数(t).
2.2.3 非河流水系途径输入碳通量贡献率估算文中非河流水系途径主要为水-气交换和湖区底泥矿化分解,估算公式如下:
| $ {\mathtt{δ}}^{13} \mathrm{C}(\mathrm{t})={\mathtt{δ}}^{13} \mathrm{C}(\mathrm{h}) \cdot x+ {\mathtt{δ}}^{13} \mathrm{C}(\mathrm{j}) \cdot y+ {\mathtt{δ}}^{13} \mathrm{C}(\mathrm{f}) \cdot(1-x-y) $ | (4) |
式中, δ13C(t)为湖区平均碳同位素含量;δ13C(h)为河流输入碳同位素值;δ13C(j)为CO2水-气交换输入碳同位素值;δ13C(f)为底泥矿化分解碳同位素值;x为河流输入的贡献率;y为CO2水-气交换的贡献率;1-x-y为底泥矿化分解的贡献率.
2.3 数据处理与分析本实验数据采用Microsoft Excel 2010软件进行统计分析,采用Microsoft Excel 2010和Origin 2019进行绘图. 为更好地分析鄱阳湖水体水化学、DIC和δ13CDIC的分布特征,以两个年份的18个监测点丰、枯水期的实测数据的均值作为丰、枯水期的含量.
3 结果与分析 3.1 鄱阳湖水体化学特征鄱阳湖水体丰、枯水期水温差异较大,丰水期平均水温为31.2℃,枯水期平均水温为8.9℃;pH变化幅度较小,为6.2~9.3,平均值为7.4;pCO2季节变化幅度均较大,丰水期为0.455×103~65.46×103 μatm,平均值为9.034×103 μatm,枯水期为0.191×103~22.02×103 μatm,平均值为4.348×103 μatm;空间上pCO2在湖区变化不大,在入湖口处pCO2均较大,尤其是赣江北支、南支和抚河入湖口. 丰、枯水期TN平均浓度分别为1.794、3.656 mg/L,TP平均浓度分别为0.094、0.148 mg/L;枯水期TN、TP浓度均大于丰水期.
3.2 鄱阳湖水体DIC和δ13CDIC组成时空差异特征鄱阳湖及其5条河流入湖口丰、枯水期水体的DIC组成均以HCO3-为主,占67 % ~98 %,平均为85 %;其次为H2CO3,占1 % ~57 %,平均为14 %;CO32-含量极少,表明鄱阳湖及其5条河流入湖口水体均属于以碳酸盐岩为主的水体.
枯水期(2月)DIC浓度范围为984~4436 μmol/L,平均值为1445 μmol/L;2019年和2020年DIC浓度分别在饶河和信江入湖口达到最大(图 2);除这2个点外,湖区和入湖口的DIC浓度差异较小. 丰水期(8月)DIC浓度范围为306~5601 μmol/L,平均值为1659 μmol/L,大于枯水期,且DIC浓度空间变化较大;2019年和2020年DIC浓度分别在赣江和抚河入湖口达到最大. 另外,对比丰枯水期DIC浓度,DIC浓度较高值多出现在入湖口,且2019年丰水期大于枯水期,而2020年不明显.
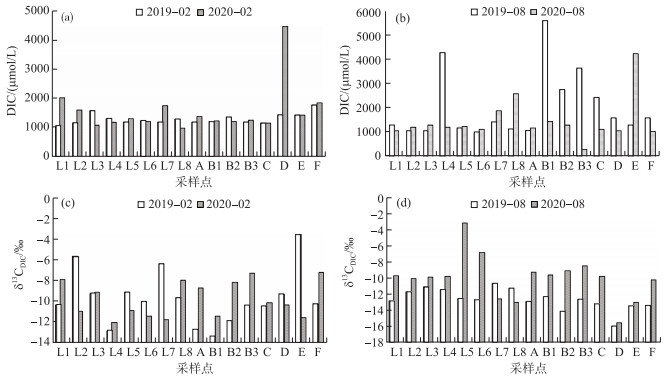
|
图 2 鄱阳湖水体DIC浓度和δ13CDIC分布特征 Fig.2 Distributions of DIC concentration and δ13CDIC in Lake Poyang |
鄱阳湖区及河流入湖口δ13CDIC变化幅度较大,枯水期为-13.29 ‰ ~-3.51 ‰,平均值为-9.82 ‰,2019年和2020年最高值出现在信江、饶河入湖口,分别为-3.51 ‰、-7.15 ‰;丰水期为-15.89 ‰ ~-3.14 ‰,平均值为-11.34 ‰,2019年和2020年最高值出现在周溪嘴(L7)、主湖区(L5),分别为-10.62 ‰、-3.14 ‰;整体上全年平均为-10.58 ‰. 2019年和2020年丰、枯水期δ13CDIC变化趋势较一致,总体上枯水期δ13CDIC大于丰水期;空间上表现为湖区δ13CDIC值大于入湖口δ13CDIC值.
3.3 DIC和δ13CDIC与水体理化参数的相关关系分析DIC与水温(T)、pH、pCO2、营养盐及δ13CDIC之间的相关关系(图 3)发现:(1)丰水期水温较高,DIC浓度也较高,大于枯水期;(2)除去一个DIC异常高值点,丰、枯水期pH与DIC相关性系数分别为0.262、0.538,枯水期两者存在相关性但不显著;(3)水体中的N、P营养盐和DIC不存在明显的相关性,但营养盐输入对DIC具有一定影响;(4)pCO2变化趋势与DIC变化趋势相似,丰、枯水期相关系数分别为0.631、0.882,存在显著相关性;(5)δ13CDIC与DIC具有相似的变化趋势,它们之间具有一定的相关性,丰水期相关性大于枯水期,鄱阳湖在流经碳酸盐岩地区的水体中δ13CDIC与DIC浓度较高,而流经硅酸盐岩地区的偏低(图 3f).
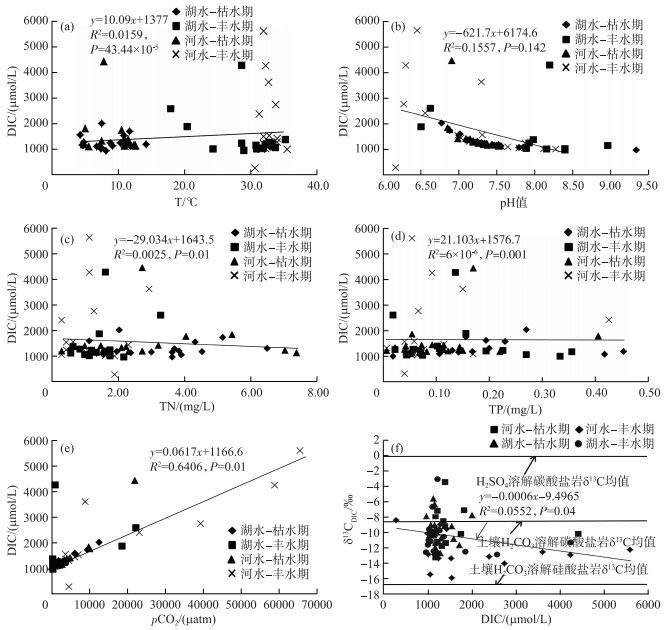
|
图 3 鄱阳湖水体DIC浓度、水体理化指标、δ13CDIC的相关关系 Fig.3 The relationships between DIC concentration, water physic-chemical parameters and δ13CDIC of Lake Poyang |
本研究首先根据湖区、入湖口、出湖口DIC浓度及月平均径流量计算各入湖河流的碳通量,继而分析不同河流碳输入对鄱阳湖DIC通量的贡献率,再根据(式(3))和同位素数据计算两个端元:CO2水-气交换、底泥矿化分解的碳贡献情况,其中丰、枯水期CO2水-气交换、底泥矿化分解碳同位素组成均取平均值. 计算结果见表 1.
| 表 1 不同水体碳通量及其对鄱阳湖水体碳通量的贡献 Tab. 1 Carbon fluxes from different water sources and their contributions to Lake Poyang |
鄱阳湖水体碳通量季节特征明显,湖区月碳通量范围为2.82~268.4 t,平均值为135.8 t;丰水期碳通量远大于枯水期,将近60.6倍;丰、枯水期“五河”水系输入碳通量中赣江输入均最大,居“五河”之首. 分析2019和2020年丰、枯水期鄱阳湖碳源贡献情况发现,CO2水-气交换对碳通量的贡献最大,占主要地位,贡献率范围为65.09 % ~78.80 %,平均值为73.07 %;河流水系次之,为6.43 % ~28.18 %,平均值为15.53 %,其中赣江水系贡献率最大,平均值为10.22 %,贡献率大小顺序为:赣江>修河>信江>饶河>抚河;底泥矿化分解的贡献率最次,为6.72 % ~15.70 %,平均值为11.41 %. 另外也发现枯水期底泥矿化分解的贡献率大于河流水系输入的贡献率,丰水期河流水系的贡献率大于底泥矿化分解的贡献率.
4 讨论 4.1 DIC浓度和δ13CDIC组成时空分布特征一般情况下,水体中DIC浓度和δ13CDIC值的时空变化受多种因素的影响,水体环境要素对其影响明显. 在时间上,鄱阳湖及入湖口DIC浓度表现为丰水期高于枯水期,丰水期湖区DIC通量是枯水期的60.6倍,入湖口DIC通量也大于枯水期(表 1),这与He等[28]、Atkins等[15]的研究结果一致,丰水期鄱阳湖流域雨量丰富,随着降水在缓慢下渗过程中溶解了土壤中更多的CO2,同时在不饱和的条件下,丰水期较高的温度和湿度环境也促进了土壤水对碳酸盐岩的溶解作用,导致DIC值增加,呈现雨季的土壤CO2效应[29];δ13CDIC值丰水期较枯水期偏负,三峡水库[30]、维斯杜拉(Vistula)河[31]、密西西比河[32]和云南澜沧江[11]中均具有此类似的变化特征,主要原因归结为丰水期生物量活性和土壤有机质分解作用强于枯水期,在丰水期微生物活性加强,对土壤有机质的分解速率加快,而丰富的雨水也有利于土壤CO2被携带至水体中,从而使得丰水期δ13CDIC更偏负,枯水期由于水温的降低,水体对大气CO2的溶解能力增强,同时枯水期水体DIC与大气CO2之间的同位素之间交换增强,使枯水期水体中δ13CDIC值偏大[33].
空间上,DIC值总体上表现为入湖口高于湖区(图 2),最高值出现在赣江入湖口,河流入湖口的沉积物受水体的冲击作用和上游土壤流失导致入湖口DIC浓度较高,大于湖区,赣江入湖口DIC浓度最高,主要是因为赣江是鄱阳湖最大的支流,其径流量居5条入湖河流之首,此外赣江流域上游的赣南地区水土流失较严重,在雨水不断冲刷下,土壤有机质的分解及碳酸盐岩的分解作用,使得水体中DIC浓度最高;湖区水流速缓慢,DIC混合均匀,故空间差异较小;δ13CDIC值表现为湖区大于入湖口,湖区水面面积大,水体流速缓慢,水体滞留时间普遍比入湖口长,水体与大气CO2交换程度较河流增加,同时湖区浮游植物光合作用增强,δ13CDIC值大于“五河”入湖口.
4.2 鄱阳湖DIC和δ13CDIC变化的驱动因素分析刘启明等[34]认为当水温升高时,藻类光合作用消耗无机碳转化为有机碳,水温升高时,也会促进有机碳的再矿化过程转化为无机碳[27],有机碳的再矿化过程在鄱阳湖及其入湖口水体中作用大于浮游植物,导致丰水期DIC浓度大于枯水期. 浮游植物的呼吸作用利用DIC,会使水体pH降低,DIC与pH具有一定的相关性[35]. 水-气界面pCO2交换受风速、温度等物理参数的影响[13],因此,生物好氧呼吸作用是水体中pCO2主要来源,而pCO2向大气的扩散作用以及浮游植物光合作用能够降低pCO2[36]. 湖泊水体中浮游植物通过光合作用利用水体中DIC转化为DOC,水体CO2分压降低,大气中的CO2进入水体;而水生生物的呼吸作用刚好相反,它释放CO2,使水中CO2的分压增加,进而使CO2从水体进入空气,pCO2和DIC存在较高的相关性(图 3e). 考虑到N、P营养盐和DIC不存在明显的相关性,水中CO2与大气的交换作用比浮游植物光合作用更强,是水体pCO2主要的控制因素. 此外,水体中的氮、磷营养盐是水体环境中的重要化学参数,是控制浮游植物生长的重要因子,大多数湖泊属于磷限制型,因此枯水期较高的磷酸盐输入足以支持浮游植物大量生长,浮游植物光合作用将无机碳转化为有机碳,从而造成枯水期DIC浓度比丰水期小. 从理论上来讲当浮游植物光合作用利用水体中DIC时会造成δ13CDIC增大,DIC应与δ13CDIC呈一定的负相关性,但Broecker[37]认为,由于水中的δ13CDIC除了受控于光合作用、呼吸过程中的动力学分馏外,同时还受到CO2水气间交换过程中的热力学分馏的影响,有机质的再矿化过程也对δ13CDIC具有一定影响,因此鄱阳湖水体中δ13CDIC和DIC的相关性不高是合理的.
4.3 溶解无机碳的来源湖泊水体碳源较多,一般认为湖泊水体DIC主要来源于地表径流、CO2的水-气交换、土壤有机质的矿化分解、沉积物碳酸盐分解[38-39]. 现代大气CO2的δ13C平均为-7 ‰ [38];H2CO3溶解碳酸盐岩可产生两份HCO3-,一份来自碳酸盐岩,一分来自土壤,形成DIC的δ13C均值为-8.5 ‰;而H2CO3溶解硅酸盐岩产生的HCO3-全部来自土壤,形成DIC的δ13C均值为-17 ‰;H2SO4溶解碳酸盐的δ13C均值为0[39-40]. 从图 3f可以看出,鄱阳湖水体δ13CDIC主要介于土壤H2CO3溶解碳酸盐岩和H2CO3溶解硅酸盐岩之间,主要分布于土壤H2CO3溶解碳酸盐岩两侧,说明H2CO3溶解碳酸盐岩是鄱阳湖流域水体中δ13CDIC与DIC的主要来源,而H2SO4溶解碳酸盐岩和H2CO3溶解硅酸盐岩对水体中δ13CDIC的组成也有一定的影响.
鄱阳湖溶解无机碳通量季节性差异较大,CO2水-气交换对碳通量的贡献率最大,是鄱阳湖无机碳的主要来源;其次为河流水系输入. 鄱阳湖流域季节性降雨径流量的变化可以影响CO2水-气交换和河流水系输入,是碳通量的主控因素. 丰水期时,由于流域降雨量的急剧增大,河流和湖泊水面面积的增大能够为CO2水-气交换提供充分的条件,此时底泥矿化分解的作用较弱,河流输入碳通量高于风化作用;枯水期,虽然河流和湖泊水面面积的减少会降低CO2水-气交换碳通量输入的作用,由于上文讨论中表明CO2水-气交换对丰、枯水期鄱阳湖的DIC、δ13CDIC、pCO2仍然具有较大影响,因此枯水期CO2水-气交换贡献作用最大,但小于丰水期;枯水期鄱阳湖底泥矿化分解作用是水体中DIC的主要来源,其碳通量贡献大于丰水期. 此外从CO2水-气交换对碳通量的贡献率最大可以推测,如果人类活动造成温室气体的排放加剧,湖泊水体中碳通量也会大大增加,因此能够对气候变化起到响应作用,并且诸如鄱阳湖这样的大湖体碳储备对降低气候变化是具有重要作用.
湖泊水体碳源较多,本研究重点分析了3种主要的碳源,忽略了贡献率相对较小的其他碳源:大气降水、浮游植物的光合和呼吸作用等影响,而且只应用简单的同位素计算公式估算不同碳源的贡献情况,碳源的碳同位素含量均取自于全球平均值,本身就存在一定的误差,需要进一步地完善此研究;接下来的研究工作中将有针对性的研究鄱阳湖各类碳源的碳同位素组成区域性特征,尤其是较难直接测定的碳源,如大气降水、浮游植物的光合和呼吸作用等.
5 结论1) 鄱阳湖区和入湖口丰水期DIC浓度大于枯水期,是丰、枯水期降雨径流量的巨大变化导致沉积物有机质释放和土壤流失造成的,有机质的再矿化和CO2水-气交换作用比浮游植物对DIC具有更大的影响. 枯水期的δ13CDIC较丰水期大,水体中DIC主要受流域H2CO3碳酸盐岩风化影响.
2) 鄱阳湖溶解无机碳通量季节差异较大,丰、枯水期的比值将近60.6倍. 鄱阳湖水体中无机碳主要来源于CO2水-气交换,其次为河流水系输入,底泥矿化分解作用也是鄱阳湖水体无机碳的来源之一. 鄱阳湖流域季节性降雨径流量的变化可以影响CO2水-气交换和河流水系输入,是碳通量的主控因素,有待增加贡献率相对较小的其他碳源的研究.
鄱阳湖DIC及其碳同位素时空特征的研究和分析各碳源对鄱阳湖的贡献情况,为探寻湖泊CO2的源汇、湖泊碳储备对气候变化的贡献及其受人类活动的影响程度提供重要参考.
| [1] |
Duan WY, Huang C. Research progress on the carbon cycle of rivers and lakes. China Environmental Science, 2021. [段巍岩, 黄昌. 河流湖泊碳循环研究进展. 中国环境科学, 2021.] |
| [2] |
Wang SM, Dou HS. A directory of lakes in China. Beijing: Science Press, 1998. [王苏民, 窦鸿身. 中国湖泊志. 北京: 科学出版社, 1998.]
|
| [3] |
Cole JJ, Prairie YT, Caraco NF et al. Plumbing the global carbon cycle: Integrating inland waters into the terrestrial carbon budget. Ecosystems, 2007, 10(1): 172-185. DOI:10.1007/s10021-006-9013-8 |
| [4] |
Zigah PK, Minor EC, Werne JP. Radiocarbon and stable-isotope geochemistry of organic and inorganic carbon in Lake Superior. Global Biogeochemical Cycles, 2012, 26(1): 1346-1346. DOI:10.1029/2011gb004132 |
| [5] |
Yan GA, Liu YD. Aquatic ecosystems: Carbon cycle and as atmospheric CO2 sink. Acta Ecologica Sinica, 2001, 21(5): 827-833. [严国安, 刘永定. 水生生态系统的碳循环及对大气CO2的汇. 生态学报, 2001, 21(5): 827-833. DOI:10.3321/j.issn:1000-0933.2001.05.022] |
| [6] |
Liu CQ. Biogeochemical processes and surface material cycling: Erosion and biogenic elements cycling in Karst Watershed of Southwest China. Beijing: Science Press, 2007. [刘丛强. 生物地球化学过程与地表物质循环——西南喀斯特流域侵蚀与生源要素循环. 北京: 科学出版社, 2007.]
|
| [7] |
Bai X, Chetelat B, Song YL. Sources of dissolved inorganic carbon in rivers from the Changbaishan area, an active volcanic zone in North Eastern China. Acta Geochimica, 2017, 36(3): 410-415. DOI:10.1007/s11631-017-0178-y |
| [8] |
Wang X, Luo C, Ge T et al. Controls on the sources and cycling of dissolved inorganic carbon in the Changjiang and Huanghe River estuaries, China: 14C and 13C studies. Limnology and Oceanography, 2016, 61(4): 1358-1374. DOI:10.1002/lno.10301 |
| [9] |
Ishikawa N, Tayasu I, Yamane M et al. Sources of dissolved inorganic carbon in two small streams with different bedrock geology: Insights from carbon isotopes. Radiocarbon, 2016, 57(3): 439-448. |
| [10] |
Kai JL, Wang JB, Huang L et al. Seasonal variations of dissolved organic carbon and total nitrogen concentrations in Nam Co and inflowing rivers, Tibet Plateau. J Lake Sci, 2019, 31(4): 1099-1108. [开金磊, 王君波, 黄磊等. 西藏纳木错及其入湖河流溶解有机碳和总氮浓度的季节变化. 湖泊科学, 2019, 31(4): 1099-1108. DOI:10.18307/2019.0410] |
| [11] |
Yuan B, Wu W, Guo MJ et al. Spatio-temporal variations of dissolved inorganic carbon and its isotopes in river-reservoir continuum: A case study on Yunnan Section of the Lancang River. J Lake Sci, 2020, 32(1): 173-186. [袁博, 吴巍, 郭梦京等. 河库连续体中溶解性无机碳及其同位素的时空分异特征——以澜沧江云南段为例. 湖泊科学, 2020, 32(1): 173-186. DOI:10.18307/2020.0117] |
| [12] |
Li YX, Huang X, Zou YJ et al. Isotopic composition of dissolved inorganic carbon and its source in the main stream of the Fenhe River during summer. China Environmental Science, 2020, 40(9): 3871-3878. [李云霄, 黄潇, 邹英杰等. 夏季汾河干流溶解无机碳同位素组成及其来源. 中国环境科学, 2020, 40(9): 3871-3878. DOI:10.3969/j.issn.1000-6923.2020.09.019] |
| [13] |
Liu HZ, Feng JW, Sun JH et al. Eddy covariance measurements of water vapor and CO2 fluxes above the Erhai Lake. Science China: Earth Sciences, 2014, 44(11): 2527-2539. [刘辉志, 冯健武, 孙绩华等. 洱海湖气界面水汽和二氧化碳通量交换特征. 中国科学: 地球科学, 2014, 44(11): 2527-2539.] |
| [14] |
Marx A, Dusek J, Jankovec J et al. A review of CO2 and associated carbon dynamics in headwater streams: A global perspective. Reviews of Geophysics, 2017, 55(2): 560-585. DOI:10.1002/2016RG000547 |
| [15] |
Atkins ML, Santos IR, Maher DT. Seasonal exports and drivers of dissolved inorganic and organic carbon, carbon dioxide, methane and δ13C signatures in a subtropical river network. Science of the Total Environment, 2017, 575: 545-563. DOI:10.1016/j.scitotenv.2016.09.020 |
| [16] |
Xu SD, Zhang ZN, Jia GD et al. Controlling factors and environmental significance of BIT and δ13C of sedimentary GDGTs from the Pearl River Estuary, China over recent decades. Estuarine, Coastal and Shelf Science, 2020, 233: 106534. DOI:10.1016/j.ecss.2019.106534 |
| [17] |
Marsh NB, Lacelle D, Faucher B et al. Sources of solutes and carbon cycling in perennially ice-covered Lake Untersee, Antarctica. Scientific Reports, 2020, 10: 12290. DOI:10.1038/s41598-020-69116-6 |
| [18] |
Richey JE, Wissmar RC, Devol AH et al. Carbon flow in four lake ecosystems: A structural approach. Science, 1978, 202(4373): 1183-1186. DOI:10.1126/science.202.4373.1183 |
| [19] |
Hope D, Kratz TK, Riera JL. Relationship between and dissolved organic carbon in northern Wisconsin lakes. Journal of Environmental Quality, 1996, 25(6): 1442-1445. DOI:10.2134/jeq1996.00472425002500060039x |
| [20] |
Yang L. Review on the research progress of carbon cycle in lake water. China Resources Comprehensive Utilization, 2020, 38(7): 122-124. [杨琳. 湖泊水体碳循环研究进展综述. 中国资源综合利用, 2020, 38(7): 122-124.] |
| [21] |
Keeling RF, Piper SC, Heimann M. Global and hemispheric CO2 sinks deduced from changes in atmospheric O2 concentration. Nature, 1996, 381(6579): 218-221. DOI:10.1038/381218a0 |
| [22] |
Shao L, Wu DS, Zhang D et al. Using isotopes to identify the sources of organic carbon and nitrogen in surface sediment in shallow lakes alongside Lake Poyang. Wetlands, 2019, 39(1): 25-33. DOI:10.1007/s13157-017-0988-z |
| [23] |
Shen RC, Lan ZC, Fang CM et al. The dikes of the sub-lakes change soil carbon cycle in the littoral wetland in Lake Poyang. J Lake Sci, 2018, 30(5): 1260-1270. [沈瑞昌, 兰志春, 方长明等. "堑秋湖"围堤改变鄱阳湖洲滩湿地土壤碳循环过程. 湖泊科学, 2018, 30(5): 1260-1270. DOI:10.18307/2018.0509] |
| [24] |
Hu CH, Zhou WB. Spatiotemporal variations of hydrochemistry parameters in the Lake Poyang catchment. Resources and Environment in the Yangtze Basin, 2014, 23(3): 427-433. [胡春华, 周文斌. 鄱阳湖流域水化学环境参数的变化特征. 长江流域资源与环境, 2014, 23(3): 427-433. DOI:10.11870/cjlyzyyhj201403018] |
| [25] |
Atekwana EA, Krishnamurthy RV. Seasonal variations of dissolved inorganic carbon and δ13C of surface waters: Application of a modified gas evolution technique. Journal of Hydrology, 1998, 205(3/4): 265-278. DOI:10.1016/S0022-1694(98)00080-8 |
| [26] |
Li GR, Liu CQ, Chen C et al. Dissolve inorganic carbon and its carbon isotope composition in cascade reservoir of the Maotiao river during summer and autumn. Environmental Science, 2009, 30(10): 2891-2897. [李干蓉, 刘丛强, 陈椽等. 猫跳河流域梯级水库夏-秋季节溶解无机碳(DIC)含量及其同位素组成的分布特征. 环境科学, 2009, 30(10): 2891-2897. DOI:10.13227/j.hjkx.2009.10.011] |
| [27] |
Chen YF, Zhang J, Wan GJ. A simple carbon cycle model of Lake Caohai, Guizhou Province. J Lake Sci, 2001, 13(1): 15-20. [陈毅凤, 张军, 万国江. 贵州草海湖泊系统碳循环简单模式. 湖泊科学, 2001, 13(1): 15-20. DOI:10.18307/2001.0103] |
| [28] |
He SJ, Xu YJ. Assessing dissolved carbon transport and transformation along an estuarine river with stable isotope analyses. Estuarine, Coastal and Shelf Science, 2017, 197: 93-106. DOI:10.1016/j.ecss.2017.08.024 |
| [29] |
Liu ZH, Groves C, Yuan DX et al. Study on the hydrochemical variations caused by the water-rock-gas interaction—an example from the Guilin Karst experimental site. Hydrogeology and Engineering Geology, 2003, 30(4): 13-18. [刘再华, Groves C, 袁道先等. 水-岩-气相互作用引起的水化学动态变化研究——以桂林岩溶试验场为例. 水文地质工程地质, 2003, 30(4): 13-18. DOI:10.3969/j.issn.1000-3665.2003.04.003] |
| [30] |
Yu YX, Wang FS, Wang BL et al. Response of dissolved inorganic carbon and its isotopic spatial and temporal characteristics to the earlier reservoir process: A case study on a new reservoir(Hongjiadu). Acta Mineralogica Sinica, 2009, 29(2): 268-274. [喻元秀, 汪福顺, 王宝利等. 溶解无机碳及其同位素组成特征对初期水库过程的响应——以新建水库(洪家渡)为例. 矿物学报, 2009, 29(2): 268-274. DOI:10.3321/j.issn:1000-4734.2009.02.021] |
| [31] |
Wachniew P. Isotopic composition of dissolved inorganic carbon in a large polluted river: The Vistula, Poland. Chemical Geology, 2006, 233(3/4): 293-308. DOI:10.1016/j.chemgeo.2006.03.012 |
| [32] |
Cai YH, Guo LD, Wang XR et al. Abundance, stable isotopic composition, and export fluxes of DOC, POC, and DIC from the Lower Mississippi River during 2006-2008. Journal of Geophysical Research: Biogeosciences, 2015, 120(11): 2273-2288. DOI:10.1002/2015JG003139 |
| [33] |
Li XD, Liu XL, Yang Z et al. Spatial and seasonal variation of dissolved inorganic carbon isotope compositions in the cascade reservoirs of the Jialing River. Journal of Shanghai University: Natural Science Edition, 2015, 21(3): 286-293. [李晓东, 刘小龙, 杨周等. 嘉陵江梯级水库群溶解无机碳同位素的时空变化特征. 上海大学学报: 自然科学版, 2015, 21(3): 286-293. DOI:10.3969/j.issn.1007-2861.2015.03.009] |
| [34] |
Liu QM, Wu Q, Cao YL et al. Stable isotope geochemical characteristics of dissolved inorganic carbon in the Jiulong River Estuary, Fujian Province, China. Chinese Journal of Geochemistry, 2014, 33(2): 178-182. DOI:10.1007/s11631-014-0675-1 |
| [35] |
Dean WE. The carbon cycle and biogeochemical dynamics in lake sediments. Journal of Paleolimnology, 1999, 21(4): 375-393. DOI:10.1023/A:1008066118210 |
| [36] |
Frankignoulle M, Bourge I, Wollast R. Atmospheric CO2 fluxes in a highly polluted estuary (the Scheldt). Limnology and Oceanography, 1996, 41(2): 365-369. DOI:10.4319/lo.1996.41.2.0365 |
| [37] |
Broecker WS, Maier-Reimer E. The influence of air and sea exchange on the carbon isotope distribution in the sea. Global Biogeochemical Cycles, 1992, 6(3): 315-320. DOI:10.1029/92GB01672 |
| [38] |
Zhang LC, Dong WJ, Wang LP. The geochemical characteristics of the water in the Changjiang River system. Acta Geographica Sinica, 1992, 47(3): 220-232. [张立成, 董文江, 王李平. 长江水系河水的地球化学特征. 地理学报, 1992, 47(3): 220-232. DOI:10.3321/j.issn:0375-5444.1992.03.003] |
| [39] |
Telmer K, Veizer J. Carbon fluxes, pCO2 and substrate weathering in a large northern river basin, Canada: Carbon isotope perspectives. Chemical Geology, 1999, 159(1/2/3/4): 61-86. DOI:10.1016/S0009-2541(99)00034-0 |
| [40] |
Amiotte-Suchet P, Aubert D, Probst JL et al. δ13C pattern of dissolved inorganic carbon in a small granitic catchment: The Strengbach case study (Vosges mountains, France). Chemical Geology, 1999, 159(1/2/3/4): 129-145. DOI:10.1016/S0009-2541(99)00037-6 |
 2022, Vol. 34
2022, Vol. 34 

