(2: 清华大学环境学院, 北京 100084)
(2: School of Environment, Tsinghua University, Beijing 100084, P.R.China)
氮磷营养盐被认为是影响蓝藻水华暴发的关键影响因素[1-4],国内外开展氮磷营养盐与蓝藻水华相关性的研究也较多. 大量研究[5-7]表明,藻类在一定营养盐浓度下的生长特征可用“S”型的Logistic函数进行描述,藻类生长与营养盐浓度存在藻类几何级数增长的营养盐浓度变化的下限阈值和藻类生长不受氮磷浓度增加影响的上限阈值. 当营养盐浓度超过下限阈值时,藻类生长呈指数增长趋势;随着氮磷浓度的消耗,当藻类种群数量达到半饱和状态(K/2)时,藻类的增长速率最大,之后藻类增长速率下降;当藻类种群数量达到环境条件允许的最大值(K)时,藻类停止生长,增长率为零,即达到藻类生长的稳定期;此时藻量最大值对应的营养盐浓度即为藻类生长不受氮磷浓度增加影响的上限阈值. 当营养盐浓度达到上限阈值时,藻类生长不受氮磷浓度增加的影响或影响程度较小.
针对蓝藻水华暴发的氮磷阈值,Gibson等[8]指出湖泊和水库中总氮(TN)、总磷(TP)浓度分别超过0.15和0.01 mg/L即有可能发生蓝藻水华,此阈值为蓝藻生长的下限阈值. 针对蓝藻水华发生的氮磷上限阈值,也开展过不少研究. 吴雅丽等[9]基于实验室原位培养实验对太湖春季藻类生长的磷阈值研究得出,藻类生长的无机磷阈值为0.02 mg/L,相当于TP阈值为0.059 mg/L. Xu等[10]基于实验室原位培养实验对太湖夏季蓝藻水华暴发期间氮磷阈值研究得出,TN浓度超过1.5~2.0 mg/L、TP浓度超过0.15~0.20 mg/L时,藻类生长不受营养盐限制. Xu等[11]基于原位微生物营养稀释生物测定法和中试营养添加实验研究指出,控制太湖叶绿素a(Chl.a)浓度在16 μg/L以下,需要控制TN在1.3 mg/L以下、TP在0.08 mg/L以下. Xu等[12]以太湖梅梁湾为例,通过野外监测数据研究指出TN=1.0 mg/L和TP=0.08 mg/L可作为控制有害藻华发生频率和强度的阈值. OECD通过询问专家意见得出富营养化状态下对应的Chl.a浓度为14 μg/L,相对应的TN和TP阈值分别为1.9和0.084 mg/L[13].
近几十年来,我国不同营养状态的大型重点湖泊如太湖、巢湖、滇池等的蓝藻水华频发[14-17],而这些湖泊的TN、TP浓度均处于较高水平,有些湖泊已经超过文献给出的蓝藻水华暴发的氮磷影响阈值,其中太湖近十年来(2007—2020年)的年均TN和TP浓度分别在1.26~2.43和0.060~0.103 mg/L之间波动. 对于不同富营养化程度的湖泊或同一湖泊的不同富营养化阶段来说,TN、TP浓度与蓝藻水华暴发的响应关系由于受环境因素的影响而存在较大差别[1, 4, 18-19]. 就太湖而言,由于太湖目前属于水生植物快速退化的草—藻型生态系统[20-21],污染物集中输入、风速风向和风浪扰动等导致水体氮磷浓度快速波动变化,致使太湖蓝藻水华与氮磷间的响应关系有所不同,进而导致蓝藻水华暴发的氮磷阈值至今难以确定. 而现有研究成果虽然对湖泊蓝藻水华暴发的氮磷阈值有所研究,但多集中在实验室研究阶段或经验值的判断,虽然也有基于野外实测数据的研究,但也限制于某一特定区域,而基于野外长序列实测数据并且覆盖整个湖泊的氮磷阈值研究则是空白.
郑丙辉等[22]指出,在制定水体营养物及其响应指标基准时,若收集和采集到生态区域中几乎所有水体的水质数据或同一水体多点位长期监测数据时,可采用频率分布法. 频率分布法分析的数据无需服从正态分布,能够直观反映数据分布的总体趋势,因此本研究参考制定营养物基准的频率分布法,利用太湖野外监测的长序列历史水质数据,确定太湖蓝藻水华暴发的TP和TN浓度控制阈值. 目前对水华暴发时水体中Chl.a浓度尚未有统一标准,Oliver等[23]将美国饮用水中Chl.a浓度高于10 μg/L定义为水华;孔繁翔等[24]指出水华形成时水体中Chl.a浓度一般在10 μg/L以上;中国科学院太湖湖泊生态系统研究站(TLLER)秦伯强团队将Chl.a浓度超过20 μg/L定义为太湖蓝藻水华发生[25];Xu等[11]也指出Chl.a浓度超过20 μg/L是蓝藻水华发生期间常见的现象. 由于太湖水体中藻类生长的磷限制一直存在,因此修正的卡森指数法(TSIM)适用于太湖富营养化评价,TSIM对水质参数Chl.a进行了分级,其中富营养状态50~100对应的Chl.a浓度范围为10~1000 μg/L. 综合上述争议,本研究以修正的卡森指数法[26]对应的富营养化Chl.a分级标准统计TP和TN浓度特征值分布,确定太湖蓝藻水华暴发的TP和TN浓度控制阈值,该阈值将会为太湖蓝藻水华防治和水环境管理提供数据支撑及依据.
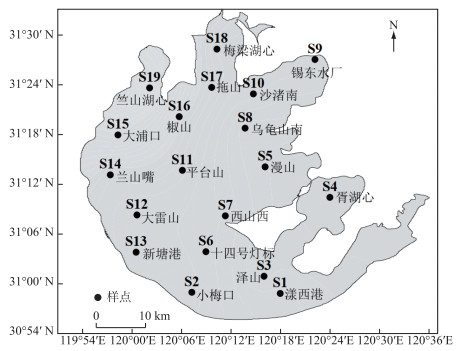
1 研究区域与方法 1.1 研究区域及点位太湖(30°56′~31°34′N, 119°54′~120°36′E)位于长江中下游地区、中国江苏省南部,是中国第三大淡水湖,水面面积2338 km2[27],水力停留时间约为284 d[10]. 水质监测点位为19个湖体监测国控点位S1~S19(图 1),监测时段为2007—2018年,监测频次为每月1次,分析指标包括叶绿素a浓度(Chl.a, μg/L)、总氮浓度(TN, mg/L)和总磷浓度(TP, mg/L).
|
图 1 研究区域及点位设置 Fig.1 Study area and sites setting |
水质数据来源于中国环境监测总站每月1次的常规水质人工采样监测结果. 依据《地表水和污水监测技术规范》(HJ/T 91—2002)中的采样方法将样品带回实验室,分析Chl.a、TN和TP浓度. 2017年之前的Chl.a浓度测定采用国家环境保护总局水和废水监测分析方法编委会的丙酮萃取法[28],2017年后的Chl.a采用环境保护部的“水质叶绿素a的测定分光光度法”[29]进行分析;TN浓度采用碱性过硫酸钾消解紫外分光光度法(GB 11894—1989)测定,TP浓度采用钼酸铵分光光度法(GB 11893—1989)测定. 太湖出入湖水量及TP、TN入湖负荷数据来自2007—2018年《太湖健康状况报告》.
1.3 数据处理及统计参考修正的卡森指数法确定不同营养状态下对应的Chl.a分级标准,依据频率分布法确定各营养状态下对应的TN和TP浓度特征值分布. 数据整理和绘图使用Microsoft Excel和Origin 2021进行;等值线图的绘制采用Surfer 12.0进行,将输入的XYZ数据文件进行网格化,再利用边界对湖泊范围进行白化,最后利用克里金插值法绘制空间分布等值线图;数据统计分析使用IBM SPSS Statistics 19.0软件包进行.
由于目前对湖泊蓝藻水华暴发时对应的Chl.a浓度尚未有统一的标准,因此结合太湖现有研究[11, 25],以轻富营养化Chl.a分级(10, 26]表征太湖蓝藻水华暴发,分析该分级标准下的TP和TN浓度控制阈值. 在对各组数据进行频率统计分析时,参考郑丙辉等[30]对湖泊营养盐控制标准的制订方法,分别统计计算3个频率取值,分别为25%分位(下1/4百分点)、50%分位(1/2百分点)、75%分位(上1/4百分点). 由于4—10月是蓝藻水华高发期,理论上Chl.a与TP、TN间的相关关系应更加显著,因此TP、TN控制阈值的确定应结合水华高发期的结果.
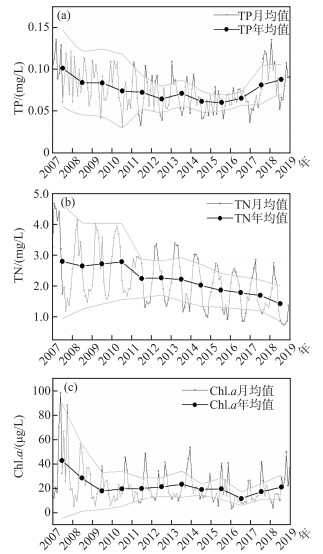
2 结果 2.1 总磷、总氮和叶绿素a的时空分布2007—2015年,太湖TP及Chl.a浓度呈下降趋势,但自2016年起出现反弹(图 2a, c). 2007—2015年TP年均值从0.10 mg/L下降至0.060 mg/L,2016年回升至0.067 mg/L,2018年达到0.087 mg/L. 2007—2018年Chl.a年均值在11.6~42.3 μg/L之间变化,从2007年的42.3 μg/L下降至2016年的11.6 μg/L,但2017年和2018年分别上升至17.3和21.0 μg/L. 2007—2018年太湖TN浓度呈持续下降趋势(P < 0.01),年均值从2007年的2.77 mg/L下降到2018年的1.42 mg/L(图 2b). 近十年内TP、TN及Chl.a浓度年均值波动分别在0.05 mg/L、1.5 mg/L和20 μg/L范围内,年内月最大值偏离年均值较大,说明太湖水体TP、TN及Chl.a浓度在时间分布上存在很大差异.
|
图 2 2007—2018年太湖TP(a)、TN(b)及Chl.a(c)月均值及年均值变化 Fig.2 Monthly and annual mean values of TP (a), TN (b) and Chl.a (c) in Lake Taihu from 2007 to 2018 |
为保证时间和空间分布的连续性和代表性,选取19个国控点位时间和空间均有覆盖的2011—2018年数据,以TP、TN和Chl.a浓度的多年均值绘制空间分布等值线图,结果发现西北湖区TP、TN和Chl.a浓度明显较高(图 3). 全湖各点位TP浓度在0.04~0.15 mg/L之间波动,其中以西北湖区的竺山湖心、大浦口及椒山水域最高,多年均值分别为0.15、0.12和0.09 mg/L. 全湖各点位TN浓度在1.0~4.3 mg/L之间波动,其中以西北湖区的竺山湖心、大浦口、椒山及拖山水域最高,多年均值分别为4.3、2.9、2.6和2.1 mg/L. 全湖各点位Chl.a浓度在8.5~30.7 μg/L之间波动,其中以西北湖区的大浦口、竺山湖心、椒山及拖山水域Chl.a浓度最高,多年均值分别为30.7、29.7、28.9和28.1 μg/L.

|
图 3 2011—2018年太湖TP(a)、TN(b)及Chl.a(c)多年均值等值线图 Fig.3 The contour map of TP (a), TN (b) and Chl.a (c) of multi-year mean values in Lake Taihu from 2011 to 2018 |
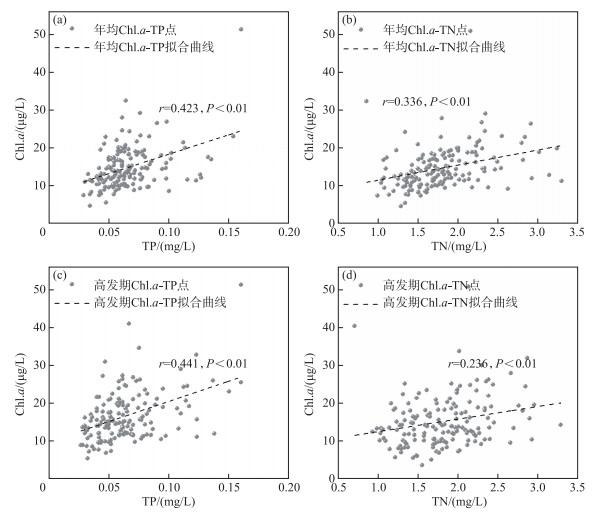
将太湖19个点位2011—2018年Chl.a、TP和TN的国控监测断面月数据进行平均,分别计算各点位全年均值及水华高发期(4—10月)均值. 从各点位全年均值来看,TP与Chl.a以及TN与Chl.a之间均呈显著正相关(r=0.423, P < 0.01;r=0.336, P < 0.01)(图 4a, b). 从水华高发期均值来看,TP与Chl.a之间以及TN与Chl.a之间也呈显著正相关(r=0.441, P < 0.01;r=0.236, P < 0.01)(图 4 c, d). 综合太湖氮磷及叶绿素a的时空分布特征,太湖氮磷浓度分布决定蓝藻水华空间格局,尽管藻类生长过程对氮磷响应过程十分复杂,但总体上太湖氮磷营养盐的空间分布决定着太湖蓝藻水华的空间分布和强度.
|
图 4 各点位TP、TN全年均值与Chl.a浓度的相关性(a, b)以及水华高发期TP、TN与Chl.a浓度的相关性(c, d) Fig.4 Correlations between annual mean values of TP, TN and Chl.a (a, b), and correlations between TP, TN and Chl.a of bloom high incidence season at each site (c, d) |
对2011—2018年太湖19个国控点位的Chl.a、TP和TN全年均值及水华高发期均值进行正态分布检验,若不符合正态分布,则将数据对数转换为ln(Chl.a)、ln(TP)和ln(TN)后再进行正态分布检验. 经检验,各组数据的偏度均较大,介于-0.244~1.572之间,因此各组数据属于偏态分布而非正态分布. 由于样本数量较少,介于3~2000之间,因此选择Shapiro-Wilk (S-W)检验方法[31]对数据进行正态检验,检验结果也显示P值均小于显著度水平0.05,因此拒绝零假设,各组数据不服从正态分布(表 1). 因此采用郑丙辉等[28]湖泊营养盐控制标准制订方法中的频率分布法确定太湖蓝藻水华暴发的TP和TN控制阈值.
| 表 1 TP、TN及Chl.a数据的正态分布检验结果 Tab. 1 Normal distribution test results of TP, TN and Chl.a |
基于修正的卡森指数法确定的Chl.a分级标准,参考湖泊营养盐控制标准制订方法的频率分布法[30],分别统计各点位Chl.a全年均值和水华高发期(4—10月)均值各富营养化分级标准对应的各百分位TP和TN浓度特征值(表 2~3). 由表可知,随着富营养化程度的加剧,Chl.a浓度随着TP和TN浓度的增加呈增长趋势;从25%分位至75%分位,TP和TN全年均值及水华高发期均值均呈显著增加趋势,表明在同一富营养化水平或Chl.a浓度范围内,存在不同污染程度的水域.
| 表 2 太湖各富营养等级下的TP、TN年均浓度统计特征值——全年均值 Tab. 2 Statistical values of TP and TN in each eutrophication grade of Lake Taihu—Annual average value |
| 表 3 太湖各富营养等级下的TP、TN统计特征值——水华高发期均值 Tab. 3 Statistical values of TP and TN in each eutrophication grade of Lake Taihu—Average value of bloom high incidence season |
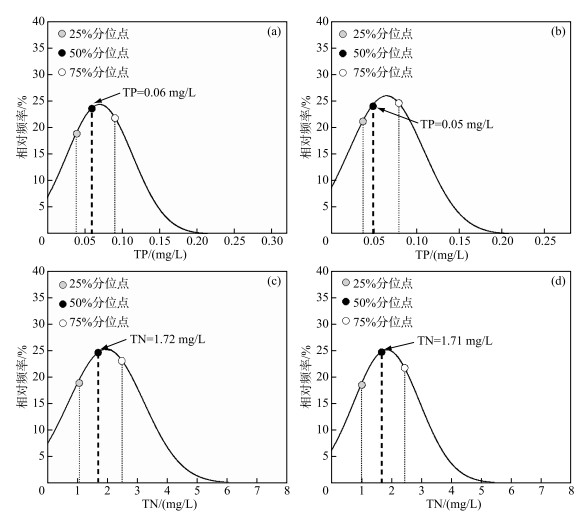
郑丙辉等[30]指出,25%分位值反映了同级营养水平下水质较好的状态,50%分位值反映了同级营养水平下水质的平均水平,75%分位值反映了同级营养水平下水质相对较差的状况,根据反退化政策,建议除贫营养水平外,其余均采用50%分位值,因此使用50%分位值作为太湖蓝藻水华相应富营养化Chl.a分级标准下的控制阈值. 若以轻富营养化等级下的Chl.a浓度(10, 26]为标准进行统计,从全年均值看,TP和TN浓度的50%分位值分别为0.06和1.72 mg/L(表 2,图 5a, c);从水华高发期均值看,TP和TN浓度的50%分位值分别为0.05和1.71 mg/L(表 3,图 5b, d).
|
图 5 太湖全湖区轻富营养等级下TP、TN浓度全年均值及高发期均值频率分布 (a, c: 2011—2018年全年均值,b, d: 2011—2018年高发期均值) Fig.5 The frequency distribution of TP and TN concentrations of annual mean value and mean value from April to October of Lake Taihu in light eutrophication grade (a, c: annual average value from 2011 to 2018, b, d: average value of bloom high incidence season from 2011 to 2018) |
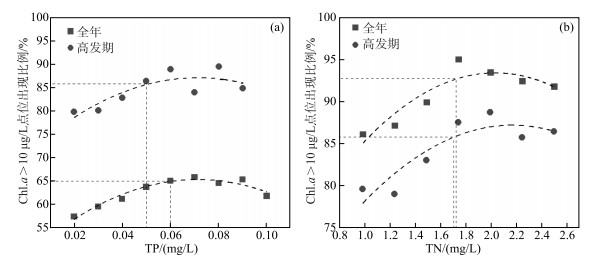
以TP 0.01 mg/L、TN 0.1 mg/L为梯度,分别统计超过不同浓度TP和TN时,Chl.a浓度高于10 μg/L的点位出现比例(图 6). 从全年均值看,当TP浓度高于0.06 mg/L、TN浓度高于1.72 mg/L时,Chl.a高于10 μg/L点位出现比例分别在65%以上和92%以上(图 6a);从水华高发期均值看,当TP浓度高于0.05 mg/L、TN浓度高于1.71 mg/L时,Chl.a浓度高于10 μg/L的点位出现比例都在85%以上(图 6a, b). 并且不论从全年均值还是高发期均值看,50%分位值对应的频率均接近拟合曲线最高点,表明50%分位值确定的TP和TN阈值对应的水华出现频率最大,最能反映水华发生状况. 综上,以轻富营养化等级下的Chl.a浓度(10, 26]为标准进行统计,太湖蓝藻水华暴发的TP和TN控制阈值分别为0.05~0.06和1.71~1.72 mg/L.
|
图 6 太湖TP(a)、TN(b)与Chl.a浓度>10 μg/L点位出现比例之间的拟合关系 Fig.6 Fitting relationship between TP (a), TN (b) and the percentage of site occurrence of Chl.a>10 μg/L |
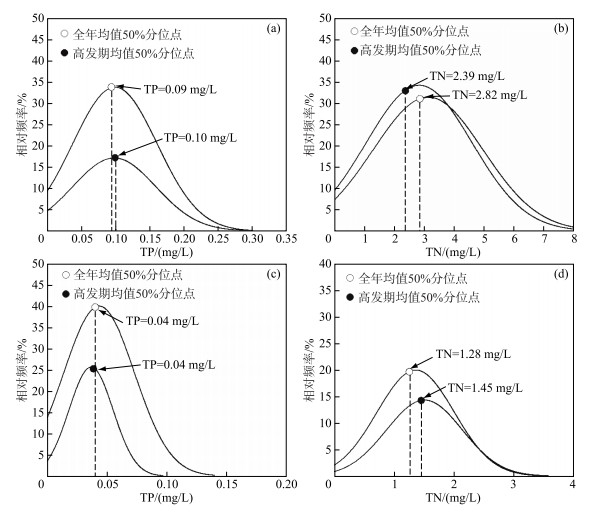
太湖目前处于典型的草—藻共存型生态系统,存在典型的西北藻型湖区和东南沿岸草型湖区[25, 32],利用本研究中确定太湖蓝藻水华暴发氮磷阈值的频率分布法对太湖藻型区(S18、S19)和草型区(S1、S4)进行验证发现,在轻富营养化叶绿素a分级标准下,藻型区50%分位对应的年均TP、TN浓度分别为0.09~0.10和2.82~2.39 mg/L(图 7a, b),远高于全湖区TP、TN控制阈值0.05~0.06和1.71~1.72 mg/L,该结果表明太湖北部藻型区的氮磷浓度高位水平为蓝藻水华的发生提供了充足的营养盐条件,再加上春夏季水温高、光照强,藻型区水华暴发难以避免. 然而,藻型区水华高发期50%分位对应的TP、TN浓度与TP、TN浓度全年均值相差不大,说明在高氮磷背景下,即便在蓝藻水华发生风险低的季节,水华发生风险仍然较大. 草型区50%分位对应的全年年均TP、TN浓度分别为0.04和1.28 mg/L、水华高发期平均TP、TN浓度分别为0.04和1.45 mg/L(图 7 c, d),低于全湖区全年年均TP、TN控制阈值以及水华高发期平均TP、TN浓度控制阈值,表明相对于太湖藻型区,草型区氮磷背景较低,蓝藻水华发生风险也较低,这可能与草型区较高的抵抗外部营养盐胁迫的反弹能力有关.
|
图 7 太湖藻型区(a, b)及草型区(c, d)轻度富营养等级下TP、TN浓度频率分布 Fig.7 The frequency distribution of TP and TN concentrations of Lake Taihu's phytoplankton-dominated area (a, b) and macrophyte-dominated area (c, d) in light eutrophication grade |
太湖处于长江下游泛滥平原区,具有较高的营养盐滞留率,湖泊发展历史时期即已具有较高的营养背景,很容易发生富营养化[33-34],一旦水体TP和TN浓度达到水华暴发的阈值,水华发生风险极高. 湖泊草型生态系统具有较高的抵抗外部胁迫的反弹能力,然而过去百年以来长江中下游地区草型湖泊生态系统功能持续损失,高氮磷条件下草型湖泊向藻型湖泊的演替随之而来[34-35]. Chl.a作为一种常用的藻类生物量表征指标,已被作为一种鉴定水体富营养化及水华发生风险的重要参考[12]. 由于目前对水华暴发时水体中Chl.a浓度尚未有统一标准,因此在前人研究结果10~20 μg/L[11, 13]基础上,以修正的卡森指数法确定的轻富营养化等级对应的Chl.a浓度范围(10, 26]作为表征水华暴发的条件,确定了TP和TN浓度控制阈值分别为0.05~0.06和1.71~1.72 mg/L.
太湖位于中东部平原湖区,地势低平,营养盐本底值高,随着湖泊流域人类活动强度的增大,入湖污染负荷不断升高,水体氮磷浓度不断增加[36-37],蓝藻水华不断加剧,2007年暴发了严重的蓝藻水华事件,造成无锡市生活用水和饮用水严重短缺[38]. 2007年后,中共中央及地方政府采取一系列措施减少外源污染物的输入,2007年以来太湖水体TP和TN浓度显著下降,但蓝藻水华发生态势依然严峻,文献表明这一现象可以用氮磷浓度与浮游植物生长间的响应关系减弱进行解释[12]. Xu等[12]以太湖典型的藻型区梅梁湾为例进行研究指出,2007年之前TP、TN与Chl.a呈显著正相关,但2007—2012年TN与Chl.a间无明显相关性. 而本研究中使用2011—2018年全湖19个点位的全年均值及高发期均值分析得出,太湖TP、TN与Chl.a仍呈显著性正相关,这说明,TP、TN与Chl.a之间的响应关系存在明显的空间差异,藻型区和草型区可能会存在不同的响应关系. 但由图 6可知,Chl.a>10 μg/L点位出现比例最大时会对应最适的氮磷浓度范围,当超过该范围时,Chl.a>10 μg/L点位出现比例将有所减弱,该范围与频率分布法50%分位确定的阈值保持一致(图 5). 因此,藻类对TP和TN的利用存在上限阈值,当超过该阈值时,藻类生长不再随着TP、TN浓度升高而发生较大的变化. Chl.a与TP、TN响应关系的减弱实际上就是因为氮磷浓度高于阈值,能充分满足水华蓝藻生长,对水华限制作用减弱,这一现象尤其在TN与Chl.a的响应关系上最为突出. 由图 4可知,每0.01 mg TP能产生约1.02 μg Chl.a,每0.1 mg TN能产生约0.4 μg Chl.a,表明TP每增加0.01 mg对Chl.a的贡献量大于TN每增加0.1 mg对Chl.a的贡献量,说明TP对藻类生长的限制作用更加明显,也进一步解释了近些年TN与Chl.a响应关系明显减弱的现象.
本研究确定的TP和TN阈值与先前研究结果存在一定差别,吴雅丽等[9]和Xu等[10]分别得到太湖春季藻类生长的TP阈值为0.059 mg/L,夏季藻类生长的TN阈值为1.5~2.0 mg/L、TP阈值为0.15~0.20 mg/L,但都是基于实验室研究的结果;近几年Xu等[11-12]进一步通过中试和野外实测分析方法研究了控制太湖有害藻华所需的临界营养阈值,其中夏季TP、TN控制阈值分别为0.08和1.3 mg/L,藻型区TP、TN控制阈值分别0.08和1.0 mg/L. 而本研究中,以(10, 26]作为水华发生的Chl.a基准条件,确定TP和TN阈值分别为0.05~0.06和1.71~1.72 mg/L,藻型区TP和TN控制阈值分别为0.09~0.10和2.82~2.39 mg/L. 由于本研究采用长序列实测数据对全湖进行了分析,不同于前人的实验室理论研究及野外特定区域的研究,研究结果代表对太湖整体的判断,加上选取的数据时段也不尽相同,使得分析结果与前人研究存在较大差别. Xu等[12]的研究虽然针对藻型区梅梁湾进行了分析,但确定的阈值仅适用于2012年之前的水华控制,对于2012年后水华控制则缺乏代表性.
另外蓝藻水华的形成不仅与氮磷营养盐浓度直接相关,温度、风速风向、水动力等很多其他影响因素也会通过影响蓝藻对营养盐的利用率进而影响水华的形成[1, 4, 18-19]. 温度(水温和气温)是影响蓝藻生长的重要条件[39-42]. 营养盐和温度对于蓝藻生长是一个双驱动过程,在营养水平相似年份,蓝藻对温度、特别是前一年冬季气温和水温很敏感,暖冬易导致第二年蓝藻水华的大规模暴发[43];而在气温或水温相似条件下,营养盐高的年份则会造成蓝藻水华暴发规模增大、持续时间增长[44]. 因此,温度有助于蓝藻对氮磷营养盐的提前利用,进而影响叶绿素a与氮磷浓度的季节性响应关系. 风速风向影响蓝藻水华的表面聚集和分散[45-46]. 水柱中营养盐充足,将促使水柱中蓝藻生物量迅速增多,此时若风速降低到接近静水状态时,水体受到扰动小,水柱中的蓝藻易凭借浮力调节机制上浮并聚集到水体表面且向下风向漂移堆积形成水华[47];当风速较大时,又会通过影响营养盐的时空场分布影响蓝藻对营养盐的吸收利用. 因此,风速风向将会影响叶绿素a与氮磷浓度的垂向及空间响应.
降水会造成污染负荷的集中输入,为蓝藻水华形成提供有利条件[48-49],降水会影响蓝藻对营养盐的利用率[50],从而导致单位氮磷浓度下的叶绿素a产量有所不同,进而影响叶绿素a与氮磷的对应关系. 水文水动力条件如换水周期的变化将导致整个湖泊内污染物的累积量及空间格局发生变化[51],进而影响蓝藻生长及水华暴发的营养盐供给. 此外,营养盐结构、光照、水量、藻类生理生态特征等其他因素也会影响蓝藻对营养盐的利用进而影响蓝藻水华的形成[52-55]. 此外,受限于《地表水和污水监测技术规范》(HJ/T 91—2002)中规定的采样方法,对于太湖这种水深小于5 m的浅水湖泊,Chl.a及TP和TN浓度均采集于表层0.5 m,对于水柱中的蓝藻量及其与氮磷浓度的垂向响应关系不能准确进行分析;然而太湖蓝藻水华以微囊藻为优势种,微囊藻在水中的分布呈现明显的分层特征,表层显著高于下层,尤其在蓝藻水华暴发时尤为显著,因此,分析表层0.5 m以上水层中的Chl.a及TP、TN浓度的响应关系具有一定的代表性.
综上分析,太湖蓝藻水华暴发的TP和TN浓度控制阈值在受多种因素的影响下存在一定统计学范围内的不确定性,而气温、水文气象等因子又是以年为周期的随机变化,因此本研究中太湖蓝藻水华控制的营养盐阈值也只是统计学意义上的一个范围值,但对于预防和治理太湖蓝藻水华及富营养化具有一定的现实指导意义,能为蓝藻水华控制和管理过程中氮磷的协调控制提供依据.
3.2 氮磷阈值的适用性及水华治理重点区域2007年以来,太湖湖体TP浓度总体呈下降趋势,自2016年起出现反弹现象(图 2). 2007—2015年湖体年均TP从0.101 mg/L下降到0.060 mg/L;而2016年回升至0.067 mg/L,近几年维持在0.08 mg/L以上. 太湖湖体TN浓度呈持续下降趋势,年均值从2007年的2.77 mg/L下降至2018年的1.42 mg/L(图 2). 虽然近十几年来太湖湖体TP、TN浓度呈下降趋势,但对于蓝藻水华来说,TP、TN浓度仍然持续在高位运行,尤其是水华高发期的高发区域. 经分析发现,2011—2018年太湖TP、TN浓度年均值波动在0.13和4.01 mg/L范围内,TP、TN浓度在时间和空间上存在较大的差异,某些时段和某些区域TP、TN浓度远高于阈值;由图 3也可看出,藻型区TP、TN浓度远高于蓝藻水华暴发的氮磷控制阈值. 因此,基于太湖水体TP、TN时间和空间变化特征,本文确定的蓝藻水华暴发的氮磷控制阈值仅代表全湖的一个总体水平、一个平均水平,即使全湖平均达到蓝藻水华控制的氮磷阈值水平,但太湖藻型区氮磷背景值高、氮磷浓度远高于此限制,加上春夏季水温升高、光照增强,该水域蓝藻水华暴发风险较高;而太湖草型区氮磷浓度低于此限制,水华发生风险较低.
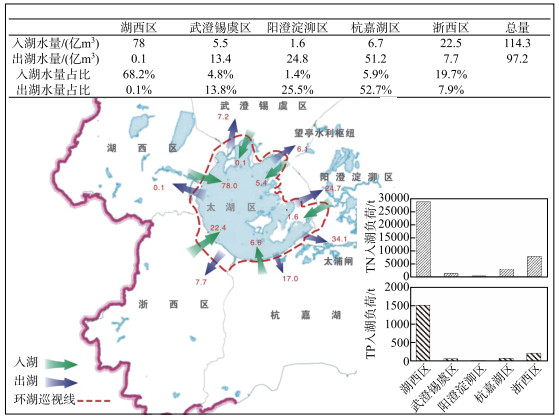
太湖流域自2007年以来虽然经过了大规模控源截污等十余年高强度治理,但伴随着社会经济快速发展带来的巨大压力[56],进入太湖的外源营养盐负荷仍然较高,根据太湖流域管理局测算,按照太湖水质目标,TN允许入湖负荷为0.9万t/a,TP允许入湖负荷为0.06万t/a,而2007—2018年入湖氮磷负荷年均值分别是3.2万t和0.16万t,分别是环境容量的3.6倍和2.7倍. 尤其湖西区是太湖氮磷污染负荷的主要来源,湖西区属于太湖流域上游,入湖水量及氮磷入湖负荷占整个太湖总入湖水量的比重较大. 以2018年为例,湖西区入湖水量占太湖总入湖水量的68.2%,入湖TN、TP负荷占太湖入湖TN、TP总负荷的比例分别为79.6%、69.3%(图 8). 大量外源污染物的输入使得湖体氮磷浓度高位运行,而梅梁湾、竺山湾和西部沿岸等区域由于水动力作用较弱,氮磷浓度不易扩散循环,为蓝藻水华暴发提供了有利条件,这可能是导致太湖水体富营养化和蓝藻水华暴发的根本原因. 因此,湖西区控源减排、污染负荷削减仍然是太湖富营养化及蓝藻水华防控的重点.
|
图 8 2018年太湖出入湖水量及入湖污染负荷(数据及底图来自2018年《太湖流域健康报告》) Fig.8 Inflow and outflow volume of Lake Taihu and pollution load into the lake in 2018 (Data and bottom map from Health Report of Taihu Basin in 2018) |
1) 从时间分布上看,2007年以来,太湖TP、TN和Chl.a浓度总体呈下降趋势,TN持续下降,TP及Chl.a自2016年起有所反弹. 从空间分布上看,TP、TN及Chl.a浓度空间差异较大,全湖各点位TN、TP及Chl.a浓度分别在1.0~4.3 mg/L、0.04~0.15 mg/L和8.5~30.7 μg/L之间波动,西北湖区的竺山湖心、大浦口、椒山及拖山水域TP、TN和Chl.a明显较高.
2) 不论从各点位全年均值来看,还是从水华高发期均值来看,太湖TP、TN与Chl.a浓度均呈显著正相关关系,表明TP、TN浓度的高水平状态仍然是Chl.a浓度保持高位的重要影响因素,氮磷营养盐的空间分布决定着太湖蓝藻水华的空间分布和强度.
3) 基于修正的卡森指数法及频率分布法,以轻富营养化等级下的Chl.a浓度(10, 26]为标准进行统计,在50%分位值下,确定了太湖蓝藻水华暴发的TP和TN控制阈值分别为0.05~0.06 mg/L和1.71~1.72 mg/L. 由于太湖TP、TN和Chl.a时间和空间差异显著,藻型区氮磷背景值高,远高于氮磷控制阈值,因此,即使氮磷全湖平均浓度控制在蓝藻水华暴发的氮磷阈值水平之下,但藻型区在气象水文等因素适宜条件下,水华发生风险仍然很高.
4) 近十几年来,虽然太湖氮磷浓度呈下降趋势,但对于蓝藻水华而言,进入太湖的外源营养盐负荷仍然较高,尤其是湖西区的TP和TN入湖污染负荷分别占到总入湖负荷的60%和70%以上,致使太湖藻型区氮磷浓度仍然处于高位运行状态. 因此,为防控太湖蓝藻水华暴发,湖西区控源减排仍然是太湖富营养化及蓝藻水华防控的重点.
| [1] |
Chen YW, Qin BQ, Teubner K et al. Long-term dynamics of phytoplankton assemblages: Microcystis-domination in Lake Taihu, a large shallow lake in China. Journal of Plankton Research, 2003, 25(4): 445-453. DOI:10.1093/plankt/25.4.445 |
| [2] |
Smith VH. Eutrophication of freshwater and coastal marine ecosystems: a global problem. Environmental Science and Pollution Research International, 2003, 10(2): 126-139. DOI:10.1065/espr2002.12.142 |
| [3] |
O'Neil JM, Davis TW, Burford MA et al. The rise of harmful cyanobacteria blooms: The potential roles of eutrophication and climate change. Harmful Algae, 2012, 14: 313-334. DOI:10.1016/j.hal.2011.10.027 |
| [4] |
Lee TA, Gretchen RB, Bollens SM. The influence of water quality variables on cyanobacterial blooms and phytoplankton community composition in a shallow temperate lake. Environmental Monitoring and Assessment, 2015, 187(6): 315. DOI:10.1007/s10661-015-4550-2 |
| [5] |
John C. Population growth in micro-organisms limited by food supply. Ecology, 1967, 48(5): 715-722. DOI:10.2307/1933728 |
| [6] |
Morrison KA, Thérien N, Marcos B. Comparison of six models for nutrient limitations on phytoplankton growth. CanadianJournal of Fisheries and Aquatic Sciences, 1987, 44(7): 1278-1288. DOI:10.1139/f87-151 |
| [7] |
Zhao GX, Gao XP, Zhang C et al. The effects of turbulence on phytoplankton and implications for energy transfer with an integrated water quality-ecosystem model in a shallow lake. Journal of Environmental Management, 2020, 256: 109954. DOI:10.1016/j.jenvman.2019.109954 |
| [8] |
Gibson G, Carlson R, Simpson J et al eds. Nutrient criteria technical guidance manual lakes and reservoirs. Washington, DC, EPA, 2000.
|
| [9] |
Wu YL, Xu H, Yang GJ et al. Developing the critical phosphorus threshold for spring algal growth in Lake Taihu, China. China Environmental Science, 2013, 33(9): 1622-1629. [吴雅丽, 许海, 杨桂军等. 太湖春季藻类生长的磷营养盐阈值研究. 中国环境科学, 2013, 33(9): 1622-1629.] |
| [10] |
Xu H, Paerl HW, Qin BQ et al. Nitrogen and phosphorus inputs control phytoplankton growth in eutrophic Lake Taihu, China. Limnology and Oceanography, 2010, 55(1): 420-432. DOI:10.4319/lo.2010.55.1.0420 |
| [11] |
Xu H, Paerl HW, Qin BQ et al. Determining critical nutrient thresholds needed to control harmful cyanobacterial blooms in eutrophic Lake Taihu, China. Environmental Science & Technology, 2015, 49(2): 1051-1059. DOI:10.1021/es503744q |
| [12] |
Xu H, Paerl HW, Zhu G et al. Long-term nutrient trends and harmful cyanobacterial bloom potential in hypertrophic Lake Taihu, China. Hydrobiologia, 2016, 787(1): 229-242. DOI:10.1007/s10750-016-2967-4 |
| [13] |
Vollenwelder RA, Janus LL. Summary Report: OECD Cooperative Programme on Eutrophication, 1981.
|
| [14] |
Yang LY, Yang XY, Ren LM et al. Mechanism and control strategy of cyanobacterial bloom in Lake Taihu. J Lake Sci, 2019, 31(1): 18-27. [杨柳燕, 杨欣妍, 任丽曼等. 太湖蓝藻水华暴发机制与控制对策. 湖泊科学, 2019, 31(1): 18-27. DOI:10.18307/2019.0102] |
| [15] |
Zhu GW, Qin BQ, Zhang YL et al. Variation and driving factors of nutrients and chlorophyll-a concentrations in northern region of Lake Taihu, China, 2005-2017. J Lake Sci, 2018, 30(2): 279-295. [朱广伟, 秦伯强, 张运林等. 2005—2017年北部太湖水体叶绿素a和营养盐变化及影响因素. 湖泊科学, 2018, 30(2): 279-295. DOI:10.18307/2018.0201] |
| [16] |
Zhang M, Shi XL, Yang Z et al. The variation of water quality from 2012 to 2018 in Lake Chaohu and the mitigating strategy on cyanobacterial blooms. J Lake Sci, 2020, 32(1): 11-20. [张民, 史小丽, 阳振等. 2012—2018年巢湖水质变化趋势分析和蓝藻防控建议. 湖泊科学, 2020, 32(1): 11-20. DOI:10.18307/2020.0102] |
| [17] |
Li JQ, Gao LY, Zhang QH et al. Design of monitoring and early warning platform for cyanobacteria bloom in Dianchi Lake. Environmental Monitoring in China, 2021, 37(2): 163-168. [李俊萩, 高凌宇, 张晴晖等. 滇池蓝藻水华监测预警平台设计. 中国环境监测, 2021, 37(2): 163-168.] |
| [18] |
Reynolds CS. What factors influence the species composition of phytoplankton in lakes of different trophic status?. Hydrobiologia, 1998, 369/370: 11-26. DOI:10.1023/a:1017062213207 |
| [19] |
Zhou QC, Zhang YL, Lin DM et al. The relationships of meteorological factors and nutrient levels with phytoplankton biomass in a shallow eutrophic lake dominated by cyanobacteria, Lake Dianchi from 1991 to 2013. Environmental Science and Pollution Research, 2016, 23(15): 15616-15626. DOI:10.1007/s11356-016-6748-4 |
| [20] |
Li WC. Multiplicity of stable states in shallow lakes and its application. J Lake Sci, 1997, 9(2): 97-104. [李文朝. 浅水湖泊生态系统的多稳态理论及其应用. 湖泊科学, 1997, 9(2): 97-104. DOI:10.18307/1997.0201] |
| [21] |
Qin BQ, Hu WP, Chen WM et al. Evolution process and mechanism of water environment in Lake Taihu. Beijing: Science Press, 2004. [秦伯强, 胡维平, 陈伟民等. 太湖水环境演化过程与机理. 北京: 科学出版社, 2004.]
|
| [22] |
Zheng BH, Xu QJ, Zhou BH et al. Building nutrient and its response indications reference state for criteria enaction: On the case of Lake Taihu, a typical shallow lake in Eastern China. J Lake Sci, 2009, 21(1): 21-26. [郑丙辉, 许秋瑾, 周保华等. 水体营养物及其响应指标基准制定过程中建立参照状态的方法——以典型浅水湖泊太湖为例. 湖泊科学, 2009, 21(1): 21-26. DOI:10.18307/2009.0103] |
| [23] |
Whitton BA, Potts M. Freshwater blooms. In: Oliver RL, Ganf GG eds. The ecology of cyanobacteria. Netherlands: Kluwer Academic, 2007: 149-194.
|
| [24] |
Kong FX, Gao G. Hypothesis on cyanobacteria bloom-forming mechanism in large shallow eutrophic lakes. Acta Ecologica Sinica, 2005, 25(3): 589-595. [孔繁翔, 高光. 大型浅水富营养化湖泊中蓝藻水华形成机理的思考. 生态学报, 2005, 25(3): 589-595. DOI:10.3321/j.issn:1000-0933.2005.03.028] |
| [25] |
Qin BQ, Li W, Zhu GW et al. Cyanobacterial bloom management through integrated monitoring and forecasting in large shallow eutrophic Lake Taihu (China). Journal of Hazardous Materials, 2015, 287: 356-363. DOI:10.1016/j.jhazmat.2015.01.047 |
| [26] |
Aizaki M, Otsuki A, Fukushima T et al. Application of Carlson's trophic state index to Japanese lakes and relationships between the index and other parameters. SIL Proceedings, 1922-2010, 1981, 21(1): 675-681. DOI: 10.1080/03680770.1980.11897067.
|
| [27] |
Jin XC, Tu QY. Specification for lake eutrophication investigation. 2nd ed. Beijing: China Environmental Science Press, 1990. [金相灿, 屠清瑛. 湖泊富营养化调查规范: 第二版. 北京: 中国环境科学出版社, 1990.]
|
| [28] |
EditoEditorial Board of Water and Wastewater Monitoring and Analysis Method, State Environmental Protection Bureaurial. Methods for monitoring and analysis of water and wastewater. Beijing: China Environmental Science Press, 1989. [国家环境保护局水和废水监测分析方法编委会. 水和废水监测分析方法. 北京: 中国环境科学出版社, 1989.]
|
| [29] |
Ministry of Environmental protection. Determination of chlorophyll a in water quality—spectrophotometric method. Beijing: Ministry of Environmental Protection, PRC, 2018. [环境保护部. 水质叶绿素a的测定分光光度法. 北京: 中华人民共和国环境保护部, 2018. ]
|
| [30] |
Zheng BH, Xu QJ, Zhu TZ et al. Primary study on enacting the lake nutrient control standard. Environmental Science, 2009, 30(9): 2497-2501. [郑丙辉, 许秋瑾, 朱延忠. 湖泊营养盐控制标准制订方法的初步研究. 环境科学, 2009, 30(9): 2497-501. DOI:10.13227/j.hjkx.2009.09.014] |
| [31] |
Royston P. Approximating the Shapiro-Wilk W-test for non-normality. Statistics and Computing, 1992, 2(3): 117-119. DOI:10.1007/bf01891203 |
| [32] |
Zhu MY, Zhu GW, Leena N et al. The influence of macrophytes on sediment resuspension and the effect of associated nutrients in a shallow and large lake (Lake Taihu, China). PLoS One, 2015, 10(6): e0127915. DOI:10.1371/journal.pone.0127915 |
| [33] |
Yang XD, Anderson NJ, Hui DX et al. Surface sediment diatom assemblages and epilimnetic total phosphorus in large, shallow lakes of the Yangtze floodplain: their relationships and implications for assessing long-term eutrophication. Freshwater Biology, 2008, 53(7): 1273-1290. DOI:10.1111/j.1365-2427.2007.01921.x |
| [34] |
Dong XH, Anderson NJ, Yang XD et al. Carbon burial by shallow lakes on the Yangtze floodplain and its relevance to regional carbon sequestration. Global Change Biology, 2012, 18(7): 2205-2217. DOI:10.1111/j.1365-2486.2012.02697.x |
| [35] |
Dearing JA, Yang XD, Dong XH et al. Extending the timescale and range of ecosystem services through paleoenvironmental analyses, exemplified in the lower Yangtze basin. PNAS, 2012, 109(18): 6808-6809. DOI:10.1073/pnas.1118263109 |
| [36] |
Qin B. The changing environment of Lake Taihu and its ecosystem responses. Journal of Freshwater Ecology, 2015, 30(1): 1-3. DOI:10.1080/02705060.2014.992053 |
| [37] |
Zhang Y, Shi K, Liu J et al. Meteorological and hydrological conditions driving the formation and disappearance of black blooms, an ecological disaster phenomena of eutrophication and algal blooms. Science of the Total Environment, 2016, 569-570: 1517-1529. DOI:10.1016/j.scitotenv.2016.06.244 |
| [38] |
Qin B, Zhu G, Gao G et al. A drinking water crisis in Lake Taihu, China: linkage to climatic variability and lake management. Environmental Management, 2010, 45(1): 105-112. DOI:10.1007/s00267-009-9393-6 |
| [39] |
Reynolds C. The ecology of phytoplankton. Choice Reviews Online, 2006, 44(4): 2114. DOI:10.5860/choice.44-2114 |
| [40] |
Liu X, Lu XH, Chen YW. The effects of temperature and nutrient ratios on Microcystis blooms in Lake Taihu, China: An 11-year investigation. Harmful Algae, 2011, 10(3): 337-343. DOI:10.1016/j.hal.2010.12.002 |
| [41] |
Paerl HW. Climate. Blooms like it hot. Science, 2008, 320(5872): 57-58. DOI:10.1126/science.1155398 |
| [42] |
Ho JC, Michalak AM, Pahlevan N. Widespread global increase in intense lake phytoplankton blooms since the 1980s. Nature, 2019, 574(7780): 667-670. DOI:10.1038/s41586-019-1648-7 |
| [43] |
Ma JR, Qin BQ, Paerl HW et al. The persistence of cyanobacterial (Microcystis spp.) blooms throughout winter in Lake Taihu, China. Limnology and Oceanography, 2016, 61(2): 711-722. DOI:10.1002/lno.10246 |
| [44] |
Shi K, Zhang YL, Zhang YB et al. Phenology of phytoplankton blooms in a trophic lake observed from long-term MODIS data. Environmental Science & Technology, 2019, 53(5): 2324-2331. DOI:10.1021/acs.est.8b06887 |
| [45] |
Wu TF, Qin BQ, Yan WM et al. The influence of changes in wind patterns on the areal extension of surface cyanobacterial blooms in a large shallow lake in China. Science of the Total Environment, 2015, 518-519: 24-30. DOI:10.1016/j.scitotenv.2015.02.090 |
| [46] |
Wu XQ, Noss C, Liu L et al. Effects of small-scale turbulence at the air-water interface on Microcystis surface scum formation. Water Research, 2019, 167: 115091. DOI:10.1016/j.watres.2019.115091 |
| [47] |
Wu TF, Qin BQ, Zhu GW et al. Dynamics of cyanobacterial bloom formation during short-term hydrodynamic fluctuation in a large shallow, eutrophic, and wind-exposed Lake Taihu, China. Environmental Science and Pollution Research, 2013, 20(12): 8546-8556. DOI:10.1007/s11356-013-1812-9 |
| [48] |
Weyhenmeyer GA, Willénand E, Sonesten L. Effects of an extreme precipitation event on water chemistry and phytoplankton in the Swedish Lake Mälaren. Boreal Environment Research, 2004, 9: 409-420. |
| [49] |
Cao J, Hou ZY, Li ZK et al. Succession of phytoplankton functional groups and their driving factors in a subtropical plateau lake. Science of the Total Environment, 2018, 631-632: 11127-1137. DOI:10.1016/j.scitotenv.2018.03.026 |
| [50] |
Xu LG, Zhang Q, Xu J et al. Migration and leaching losses of nutrients in relation to rainfall intensity. Acta Pedologica Sinica, 2008, 45(3): 437-444. [徐力刚, 张奇, 徐进等. 不同降雨强度对营养盐垂向迁移过程和淋失量的影响. 土壤学报, 2008, 45(3): 437-444. DOI:10.3321/j.issn:0564-3929.2008.03.008] |
| [51] |
Zhu W, Cheng L, Xue ZP et al. Changes of water exchange cycle in Lake Taihu (1986-2018) and its effect on the spatial pattern of water quality. J Lake Sci, 2021, 33(4): 1087-1099. [朱伟, 程林, 薛宗璞等. 太湖水体交换周期变化(1986—2018年)及对水质空间格局的影响. 湖泊科学, 2021, 33(4): 1087-1099. DOI:10.18307/2021.0411] |
| [52] |
Fujita RM. The role of nitrogen status in regulating transient ammonium uptake and nitrogen storage by macroalgae. Journal of Experimental Marine Biology and Ecology, 1985, 92(2/3): 283-301. DOI:10.1016/0022-0981(85)90100-5 |
| [53] |
Torres AI, Gil MN, Esteves JL. Nutrient uptake rates by the alien alga Undaria pinnatifida (Phaeophyta) (Nuevo Gulf, Patagonia, Argentina) when exposed to diluted sewage effluent. Hydrobiologia, 2004, 520(1-3): 1-6. DOI:10.1023/B:HYDR.0000027686.63170.6c |
| [54] |
Bouvy M, Ba N, Ka S et al. Phytoplankton community structure and species assemblage succession in a shallow tropical lake (Lake Guiers, Senegal). Aquatic Microbial Ecology, 2006, 45: 147-161. DOI:10.3354/ame045147 |
| [55] |
Ptacnik R, Solimini AG, Andersen T et al. Diversity predicts stability and resource use efficiency in natural phytoplankton communities. PNAS, 2008, 105(13): 5134-5138. DOI:10.1073/pnas.0708328105 |
| [56] |
Zhu GW, Qin BQ, Zhang YL et al. Fluctuation of phosphorus concentration in Lake Taihu in the past 70 years and future control strategy. J Lake Sci, 2021, 33(4): 957-973. [朱广伟, 秦伯强, 张运林等. 近70年来太湖水体磷浓度变化特征及未来控制策略. 湖泊科学, 2021, 33(4): 957-973. DOI:10.18307/2021.0401] |
 2022, Vol. 34
2022, Vol. 34 


