(2: 南京水利科学研究院生态环境研究所, 南京 210029)
(3: 水灾害防御全国重点实验室, 南京 210098)
(2: Eco-Environmental Research Department, Nanjing Hydraulic Research Institute, Nanjing 210029, P.R. China)
(3: The National Key Laboratory of Water Disaster Prevention, Nanjing 210098, P.R. China)
蓝藻水华是水体生态系统退化的重要原因之一[1]。富营养化水体中藻类大量繁殖,超过一般水体中的生物量平均值,并垂向迁移至水体表面,形成肉眼可见的群体一般被定义为“水华”[2]。全球超68%的湖泊面临着蓝藻水华暴发问题,我国已报道过的蓝藻水华种类有上百种,较为普遍且危害较大的是微囊藻属(Microcystis)[3-4]。蓝藻能通过伪空胞的合成、伪空胞的破裂以及细胞内碳水化合物的合成与消耗3种方式进行垂向迁移,以改变群体在水柱的位置[2, 5]。近年来,在气候变暖与营养物质富集相结合促进蓝藻大量繁殖的背景下,蓝藻通过自身特性进行垂向迁移极大地促进了蓝藻暴发的强度和频率[6-7]。因此,研究蓝藻垂向迁移特征及其影响因素对于理解蓝藻水华形成机制和蓝藻水华预测预警具有重要意义。
自然环境条件复杂,蓝藻水华时空动态变化较快。受浮标定点等传统监测设备的限制,蓝藻垂向迁移研究最初以室内实验或者原位定点的方式为主,主要关注水温、光照强度、风速、营养盐等单一环境要素对单细胞蓝藻浮力的影响[8-10]。光照通过影响光合作用效率改变蓝藻细胞内的碳水化合物含量,从而调节蓝藻密度及垂向迁移[11]。温度主要通过影响蓝藻细胞的光合速率、呼吸代谢速率以及伪空胞的体积来改变细胞密度进而改变蓝藻在水柱中的垂向分布[11-13]。Webster等[14]发现垂向紊动对于湖泊中蓝藻群体垂向分布的影响存在明显的风速阈值,在太湖梅梁湾风速高于3.1 m/s时表层水华消失,较大的风速能够克服蓝藻的垂向迁移,使得蓝藻在垂向完全混合[15]。除光照和温度外,营养盐也是影响蓝藻上浮下沉的重要因素之一。Konopka[16]发现在水温和营养盐分层明显的深水湖泊中,为满足自身生长需要,蓝藻会通过调节浮力改变垂向分布特征。杨波[17]通过分离培养实验发现在氮、磷限制的不同水体里蓝藻垂向藻密度变化明显。然而,区别于室内培养实验和深水湖泊,浅水湖泊蓝藻常以多细胞的群体形式存在,群体垂向分布更易受外界温度、光照、营养物质及风浪扰动的影响[18-20]。而现有研究大多聚焦于定点、单一要素变化对蓝藻垂向分布的影响,气象、水环境等多因子综合作用对浅水湖泊蓝藻垂向迁移的影响尚不明晰。随着监测技术的发展,MODIS(moderate resolution imaging spectroradiometer)和Landsat、GOCI(geostationary ocean color imager)等时效性高、覆盖范围广和成本低的高频率卫星遥感影像逐渐成为蓝藻水华监测的重要手段,GOCI遥感影像更是弥补了传统卫星遥感访问周期较长的不足,每日提供的8景影像使得大型浅水湖泊水华日变化监测成为可能[21-23]。不少研究者通过GOCI以太湖为整体分析了蓝藻的垂向迁移及驱动因素[24-26]。受气象和水文条件的影响,太湖不同湖区的水质和蓝藻水华具有较大的时空差异性。因此,有必要对太湖不同湖区的气象、水环境因子及其综合作用对蓝藻垂向迁移的影响进行详细研究。
本文旨在利用2015-2020年GOCI遥感影像,反演太湖蓝藻水华日变化过程,分析太湖不同湖区的蓝藻水华日变化规律,揭示气象和水环境因子对蓝藻水华日变化的影响,阐明浅水湖泊蓝藻垂向迁移的关键影响因素。
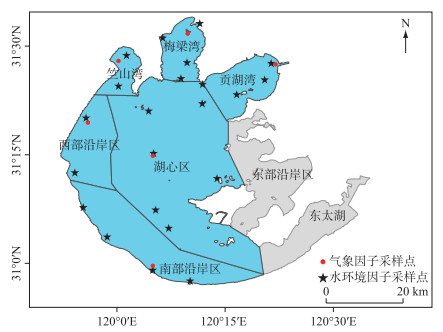
1 研究材料与方法 1.1 研究区域概况太湖(30°55′~31°33′N,119°52′~120°37′E)是我国第三大淡水湖泊,属亚热带季风气候,水域面积为2338.1 km2,平均水深为1.9 m[27],湖区主要分为竺山湾、梅梁湾、贡湖湾、西部沿岸区、南部沿岸区、湖心区、东部沿岸区、东太湖8个部分(图 1)。受气候变暖和人为活动的影响,太湖长期处于富营养化状态,夏秋两季常有大范围蓝藻水华暴发[13]。太湖蓝藻主要以微囊藻属为主,藻华高发期微囊藻占蓝藻总生物量的40%~98%[28-29]。微囊藻大多以群体形式排列于一个共同的胶被中,聚集的群体细胞通过伪空胞和镇重物提供浮力,从而调节蓝藻垂向迁移速率[19-20, 30]。
|
图 1 太湖湖区及采样点分布 Fig.1 Distribution of lake areas and water quality sampling locations in Lake Taihu |
本研究收集太湖湖区2015-2020年4-12月水环境、卫星遥感影像和气象数据。水环境数据来自太湖流域水文水资源监测中心提供的湖区22个点位逐月水质数据(采样点见图 1,具体采样点位见附表 Ⅰ),采样于每月上旬进行,指标包括水下0.5 m处总氮(TN)和总磷(TP)。卫星遥感影像来自韩国海洋卫星中心2010年发射的地球静止海洋彩色成像仪(geostationary ocean color imager,GOCI)的L1B级数据,空间分辨率500 m,时间分辨率1 h,每日8景影像(08:00-15:00)。每小时风速和温度数据下载自ERA5-Land气象网站,水平分辨率为0.1°×0.1°,风速为距地表 10 m的u和v分量数据,温度为距地表 2 m的气温数据(气象数据采样点位见图 1)。累积光合有效辐射从GOCI数据中提取。
GOCI遥感数据由SeaDAS代码处理,剔除有云和无明显水华图像,最后获得可用影像1147景,共获取竺山湾539景、梅梁湾695景、贡湖湾349景、南部沿岸区686景、西部沿岸区928景、湖心区874景。大量沉水植物分布在东部沿岸区和东太湖,会干扰蓝藻水华的提取,故本研究不考虑这两个区域[31]。
1.3 数据统计分析由于GOCI遥感具有较低的信噪比,近红外波段反射率较强,可以利用可见和近红外波段识别遥感影像上聚集在水体表面的蓝藻水华[32]。基于可见和近红外波段提出了可以有效识别蓝藻水华的AFAI指数[24]。
| $ AFAI=R_{\mathrm{rc}, \lambda 2}-R_{\mathrm{rc}, \lambda 2^{\prime}} $ | (1) |
| $ R_{\mathrm{rc}, \lambda 2^{\prime}}=R_{\mathrm{rc}, \lambda 1}+\left(R_{\mathrm{rc}, \lambda 3}-R_{\mathrm{rc}, \lambda 1}\right) \times\left(\lambda_2-\lambda_1\right) /\left(\lambda_3-\lambda_1\right) $ | (2) |
式中,λ1、λ2、λ3分别为660、745、865 nm波段中心,λ1为可见波段,λ2、λ3为近红外波段,Rrc为对应波段光谱。
利用AFAI指数阈值(-0.001)能将覆盖太湖的像素分为非水华像素和水华像素。基于AFAI指数,利用以下公式对各湖区分区计算太湖水华暴发强度[26](cyanobacterial bloom intensity,CBI):
| $ CBI=\sum\limits_{i=1}^n\left(A F A I_i+0.001\right) $ | (3) |
式中,AFAIi为第i个点的AFAI值,n为发生水华的像素点数。
我们假设蓝藻在垂向水柱中为均匀分布,以相同速度向水体表面漂浮。基于CBI计算各湖区蓝藻垂向迁移率[26]:
| $ V_c=\left[D-D \times\left(\frac{C B I_{\min }}{C B I_{\max }}\right)\right] / \Delta T $ | (4) |
式中,CBImin为每日发生水华最大值前的最小水华强度值,CBImax为每日最大水华强度值,ΔT为水华时间差值(h),D为湖体深度(本研究取1.9 m),Vc单位为m/h。对每个湖区按类型分别计算垂向上浮速率和下沉速率(表 1)。
| 表 1 太湖不同湖区水华类型及蓝藻垂向运动速率统计 Tab. 1 Statistics on the number of water bloom types and the rate of vertical movement of cyanobacteria in different lake areas of Lake Taihu |
藻细胞浮力对不同光强和不同光周期的响应不同,细胞的响应时间、伪空胞的合成、伪空胞的破裂和碳水化合物的累积与消耗等过程均显著受到光的影响。然而,在自然环境中受到水动力、风速、温度等影响,很难直接对光的影响进行判定。通过Li等[26]提出的蓝藻接受的累积光辐射指标ΔIp与ΔCBI,可以衡量不同光强对太湖蓝藻垂向运动的影响:
| $ \Delta I_{\mathrm{p}}=\sum\limits_t\left(A F A I_{(t)} \times i P A R_{(t)} \times T \times S\right), t=t_{\max } \sim t_{\min } $ | (5) |
| $ \Delta C B I=C B I_{\max }-C B I_{\min } $ | (6) |
式中,iPAR(t)为水华时的光辐射,tmax为水华最大值发生时的时间,tmin为水华最小值发生时的时间,T为GOCI时间分辨率,取3600 s,S为GOCI空间分辨率,取250000 m2,ΔIp单位为kmol photons。
采用IBM SPSS Statistics 26.0软件对风速与Vc、ΔIp与ΔCBI、气温与CBImax/CBImin进行相关性分析,检验分为显著水平(P<0.01)和不显著水平(P>0.05)。偏最小二乘法结构方程模型(partial least squares structural equation modeling,PLS-SEM)以水华强度为研究对象,评估气象因子(气温、累积光辐射、风速)和水环境因子(TN、TP)与水华强度变化量和最大水华强度的关系,量化各气象因子和水环境因子对蓝藻垂向迁移的贡献大小。PLS-SEM一般采用共线性指数(collinearity statistics,VIF)、构面信度与效度(construct reliability and validity)、区别效度(discriminant validity)、模型适配度(model fit)等指数判断模型整体拟合程度[33]。分析运算主要在软件SmartPLS 3.0中进行。
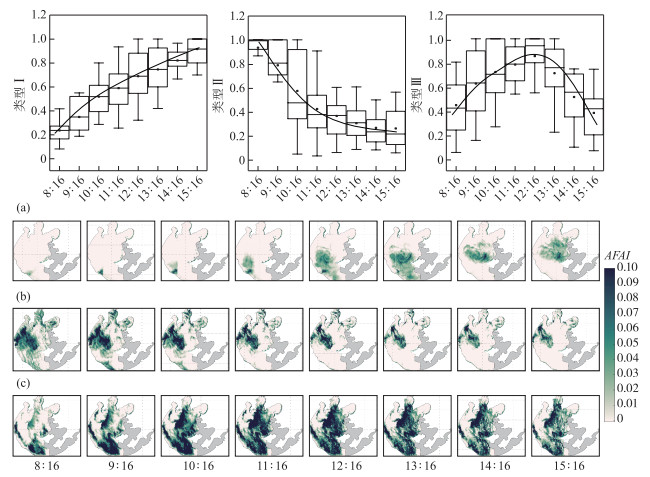
2 结果 2.1 太湖蓝藻水华日变化特征根据CBI对太湖蓝藻水华日变化进行分类,主要分为类型Ⅰ(上升)、类型Ⅱ(下降)、类型Ⅲ(先上升后下降)、类型Ⅳ(先下降后上升,样本数量较少,本研究中未进行分析),前3种类型见图 2。如表 1所示,湖心区以类型Ⅰ和类型Ⅲ为主,其它湖区以类型Ⅱ和类型Ⅲ为主,类型Ⅰ发生频率较低。太湖蓝藻垂向上浮速率范围在0.282~0.386 m/h之间,各年份垂向上浮速率均值分别为0.329、0.294、0.308、0.283、0.341和0.300 m/h。太湖蓝藻垂向下沉速率相对较小,范围在0.246~0.309 m/h之间。
|
图 2 太湖蓝藻水华日变化遥感影像反演3种类型 (a)类型Ⅰ:上升(2017年12月18日);(b)类型Ⅱ:下降(2018年5月13日);(c)类型Ⅲ:先上升后下降(2017年11月1日) Fig.2 Three types of remote sensing images of cyanobacteria bloom variation in Lake Taihu (a)Type Ⅰ: Rise (18 December, 2017); (b) Type Ⅱ: Decline (May 13, 2018); (c) Type Ⅲ: First up and then down (November 1, 2017) |
基于ERA5-Land数据统计得到水华发生时平均风速及水华前一天平均风速(前24 h)。将6个区域水华发生时风速按6个范围(0~1、1~2、2~3、3~4、4~5和>5 m/s)进行统计,得到水华发生风速大小频率(图 3a)。如图所示,各湖区水华发生时风速主要在1~4 m/s,发生明显水华频率最高的风速范围为2~3 m/s,在此范围内竺山湾共发生水华26 d、梅梁湾30 d、贡湖湾20 d、南部沿岸区31 d、西部沿岸区38 d、湖心区41 d,风速大于5 m/s时水华发生频率较低。同时,对水华发生时不同风速范围内平均CBI进行统计(图 3b)可以发现,风速越大,各湖区平均水华面积越小。

|
图 3 不同风速下各湖区蓝藻水华次数(a)及平均水华强度(b) Fig.3 The number of cyanobacteria blooms(a) and the average bloom intensity (b)of cyanobacteria in each lake area under different wind speeds |
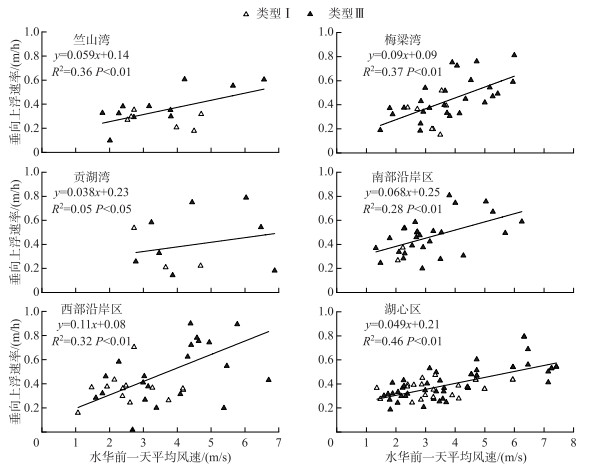
风速大于3 m/s时,蓝藻垂向变化更易受风浪扰动影响[31-33],本研究筛选当日平均风速小于3 m/s的情景进行分析。对不同湖区水华发生时风速小于3 m/s的蓝藻垂向上浮速率(包含类型Ⅰ和类型Ⅲ上升部分)与水华前一天平均风速进行Pearson相关性分析(图 4)发现,除了贡湖湾其它湖湾都与水华前一天风速存在显著正相关关系(P < 0.01)。相关性关系R2大小关系为湖心区>梅梁湾>竺山湾>西部沿岸区>南部沿岸区。
|
图 4 不同湖区水华前一天风速与垂向上浮速率的相关性 Fig.4 Correlation between wind speed and vertical uplift rate the day before bloom in different lake areas |
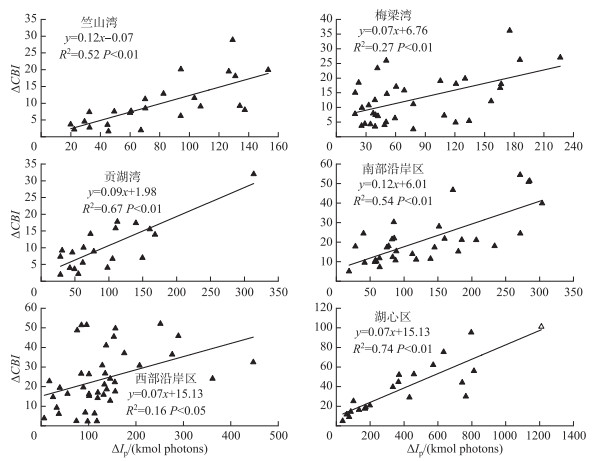
对各湖区风速小于3 m/s时类型Ⅱ ΔIp与ΔCBI进行Pearson相关性分析。相关性分析结果如图 5所示。总体而言,研究区域中6个湖区CBI的减少量均与累积光辐射存在显著的正相关关系(P < 0.05)。湖心区由于面积较大,CBI的减少量和累积光辐射接受量都远大于其它5个湖区,且相关性最强(R2=0.74)。贡湖湾、南部沿岸区、竺山湾相关性结果相对较好(R2分别为0.67、0.54、0.52),西部沿岸区和梅梁湾相关系数较低(R2分别为0.16、0.27)。
|
图 5 风速小于3 m/s时类型ⅡΔIp与ΔCBI相关性 Fig.5 Correlation between ΔIp and ΔCBI for Type II at wind speeds less than 3 m/s |
综合太湖不同湖区中3种水华发生类型,发现随水华当日平均气温升高,CBImax/CBImin减小值越小,两者存在非线性关系。因此,对风速小于3 m/s时的日平均气温与CBImax/CBImin进行幂函数曲线拟合,结果如图 6所示(R2=0.48)。发生明显水华时太湖日平均气温在3~35℃之间,不同温度区间内样本数量差异较大,水华当日平均气温低于15℃时,样本数量较少(N=28),气温高于15℃时,统计样本明显增多(n=157)。为排除温度较高的同时风速较小对蓝藻垂向分布的影响,对气温和风速进行相关性分析,相关性结果表明气温与风速之间不存在自相关(N=185, P>0.05)。

|
图 6 风速小于3 m/s时日平均气温与CBImax/CBImin相关性 Fig.6 Correlation between daily mean temperature and CBImax/CBImin at wind speeds less than 3 m/s |
为进一步分析各环境因子对蓝藻水华垂向迁移的贡献率,确定各个分区的蓝藻水华主要驱动因子,采用PLS-SEM结构方程模型进行筛选。气象因子包括温度、累积光辐射和风速(当天平均风速、前一天平均风速),水环境因子素包括TN和TP。偏最小二乘法结构方程模型的共线性指数(collinearity statistics, VIF)均小于10,不存在共线性问题,构面信度与效度(construct reliability and validity)均大于0.50,区别效度(discriminant validity)中HTMT指数均小于0.90,模型适配度(model fit)中SRMR < 0.10,d_ULS < 0.95,d_G < 0.95,模型拟合程度较好,结果可信。
PLS-SEM结构方程模型中R2显示了因变量被模型解释的方差量,一般R2值最小应大于0.1,大于0.67时模拟精度较高。可以看出,模型对水环境因子的解释度较低,但对水华强度解释度较高,系数分别为0.737、0.420、0.722、0.636、0.581、0.863。路径系数(path coefficients)显示了气象与水环境、气象与水华强度基本呈现正因果效应,湖泊水环境与水华强度只有贡湖湾和湖心区表现为弱的负因果效应。太湖6个湖区均表现为气象因子比水环境因子的影响权重高,各湖区气象因子路径系数分别为0.858、0.550、0.862、0.720、0.761、0.915,湖心区气象因子权重最大。水环境因子路径系数仅在贡湖湾、南部沿岸区相对较大(0.151、0.400),其它4个湖区分别为0.074、0.047、0.004、0.018。气象因子中光辐射变量权重均为正,代表光照越强,水华强度及水华变化值越高;风速变量权重基本为负,代表水华发生时风速越大,水华强度越小;气温变量权重正负各湖区不一样,竺山湾、西部沿岸区为正,其它湖区权重指数为负。水环境因子中各湖区参数权重正负关系呈现较大差别,但TN、TP权重主要都为正,浓度越高,各湖区水华强度及水华日变化越明显。
在太湖6个湖区中对水华强度产生较大影响的为气象因子,且气象因子中累积光辐射变量均为主要影响因子,各湖区累积光辐射变量权重分别为0.811、0.994、0.998、0.974、0.908、1.037。结构模型结果显示水环境因子对蓝藻水华强度存在较弱的影响,各湖区中TN、TP变量权重大小存在较大差异,竺山湾、梅梁湾及南部沿岸区TP权重较大,其它湖区中TN权重较大。
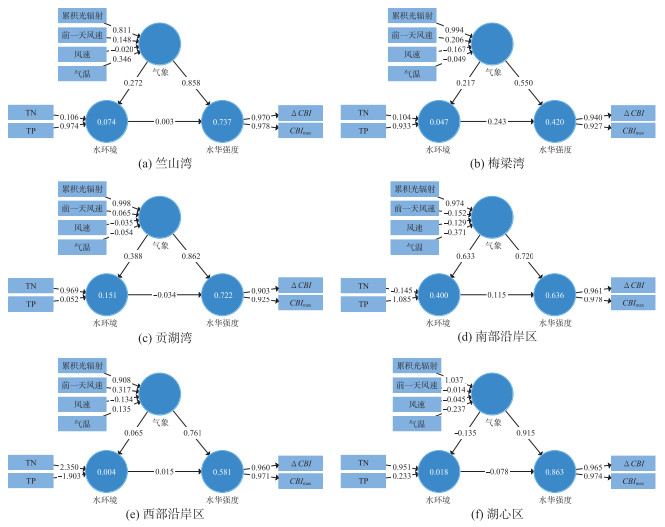
|
图 7 不同湖区PLS-SEM结构方程模型分析 Fig.7 PLS-SEM structural model analysis of different lake areas |
由于太湖不同湖区气象、水质及水华变化常存在较大的时空差异性,本文在日尺度上对太湖不同湖区、不同类型水华日变化过程与气象因子关系进行了研究,与已有研究结果一致,风速、累积光辐射、气温均会影响太湖的蓝藻垂向迁移过程[10-12]。Wu等[34]提出,风速可以改变湖泊内部垂向扰动和生物化学过程。对于大型浅水湖泊,风速大于4 m/s时,蓝藻的垂向上浮会受到抑制,小于3 m/s时蓝藻具备上浮的水动力条件[15]。在弱扰动条件下,相较于较小尺寸(直径 < 100 μm)蓝藻群体,大尺寸的蓝藻群体具有较大的垂向迁移速率[35]。2017年太湖蓝藻大量繁殖,蓝藻群体尺寸和密度均较大,与水华频率和面积较小的2016和2018年(上浮速率为0.294和0.283 m/h)相比,垂向上浮速率相对较大(0.308 m/h)。因此,我们认为蓝藻的垂向迁移运动可能会导致蓝藻水华大面积暴发,但蓝藻水华暴发受多因素的影响,为明确2017年水华大面积暴发原因还需深入研究。对太湖不同湖区水华垂向迁移速率分析发现,各湖区垂向迁移速率差异不大,这可能与我们假设各湖区水深均为1.9 m有关。本研究还通过不同类型水华发生时风速小于3 m/s的蓝藻水华日变化过程进行分析发现,类型Ⅰ和类型Ⅲ水华发生主要与水华前一天和当天风速有关,前一天风速较大时,风浪产生的较强的湍流紊动会引起蓝藻群体的分散和下沉,当天风速较低时,较弱的湍流扰动会促使蓝藻颗粒相互碰撞形成大尺寸的群体,较大尺寸的蓝藻群体可以获得更大的浮力,更快地上浮到水体表面[36]。这也解释了强风天气后平静湖面总是发生大面积水华的原因[37]。
蓝藻细胞的垂向迁移对光强也有不同响应,低光强下浮力上升,高光强下浮力会降低[12]。当风速 < 3 m/s时,各湖区类型Ⅱ的CBI的减少量与累积光辐射呈显著正相关(图 5)。蓝藻在经历长时间的光照后会丧失浮力,逐渐下沉,而通过光合作用合成碳水化合物导致自身密度增大是蓝藻下沉的主要原因。蓝藻能接受的累积光辐射与湖体的透明度密切相关,深水湖泊中透明度主要与风浪扰动产生的悬浮物有关,而在富营养化浅水湖泊中藻类大量生长繁殖也会使湖水透明度下降[38-39]。在竺山湾、梅梁湾和西部沿岸区,透明度主要受藻类生长引起的叶绿素a浓度的影响,但ΔIp中未考虑叶绿素a浓度对累积光辐射的贡献,AFAI与叶绿素a浓度并非线性关系[25]。因此,在竺山湾、梅梁湾等湖区相对于湖心区相关性较差。
不少研究发现,温度高于15℃时,蓝藻细胞的光合、呼吸作用速率会呈指数上升[13]。从图 6看出当气温高于15℃时,统计样本明显增多,说明蓝藻在夜晚通过呼吸作用消耗碳水化合物获得浮力,从而在遥感第一幅图时通常就能观察到较大水华。You等通过不同温度下的室内实验证明,与17.5℃相比,28℃时蓝藻群体表现出更大的上浮位移的同时蓝藻群体密度也不断减小[40]。我们通过分析发现气温越高,CBI变化比值越小,这说明温度越高时,蓝藻群体能在水体表面持续聚集。在较高的温度下,群体通过光合作用合成大量的碳水化合物,蓝藻的生长速率明显增加,而蓝藻细胞内的酶活性随着温度升高而增强,较高的代谢及时消耗光合作用合成的产物。因此,蓝藻群体常呈现出高温下密度明显小于低温下的密度,能在水体表面持续悬浮。近年来,气候变暖趋势越来越明显,本研究表明,温度可以通过改变蓝藻群体密度促使蓝藻持续上浮,可能会导致蓝藻水华暴发面积扩张、频率增加和持续时间延长。
3.2 蓝藻垂向迁移的主要影响因子蓝藻成为水体中优势藻群往往归功于蓝藻的垂向迁移能力。蓝藻群体的垂向迁移速率受到粒径大小、温度、光照、压强、营养盐等多种环境因素的协同耦合影响。一般认为,短期的垂向迁移主要归因于碳水化合物的积累和消耗[8]。在夜晚,蓝藻通过呼吸作用消耗碳水化合物获得浮力,在清晨时刻大量上浮形成水华;随着光照逐渐增强,蓝藻细胞通过光合作用改变细胞密度,在中午时刻光合作用合成的碳水化合物重量抵消并超过细胞产生的浮力,蓝藻开始逐渐下沉。蓝藻细胞昼夜周期性迁移的过程中,细胞密度与碳水化合物的含量呈显著线性关系[41]。偏最小二乘法结构方程模型结果显示,驱动蓝藻垂向迁移和水华日变化的关键因素为气象因子,其中,累积光辐射是气象因子中影响蓝藻水华日变化的主要影响因子。
蓝藻垂向迁移除受气象因子影响外,营养盐也可通过影响蓝藻细胞内的伪空胞的合成与破裂调控蓝藻浮力。在深水湖泊中,水体热力分层导致垂向水柱中营养盐浓度呈现明显的梯度差,表层水体常出现营养限制,为满足自身生长需要,蓝藻群体会丧失浮力迁徙到营养盐充足的水底,当蓝藻细胞在水底生长繁殖到限制因素不再是营养盐后,又通过代谢消耗碳水化合物获得浮力,上升至水表进行光合作用[42-43],这一过程周期相对较长。杨波[17]通过实验也发现细胞的营养状态是控制蓝藻长期上浮下沉的重要因素,氮限制和磷限制的水体都会影响蓝藻的浮力。而对大型浅水湖泊太湖分析发现,水环境因子在太湖湖区中与蓝藻水华强度基本为较弱的正相关关系。我们认为存在此结果主要有两点原因:首先是因为相较于深水湖泊,太湖这种大型富营养化浅水湖泊中营养盐水平本来就较高,同时,水体受水动力、风浪扰动等影响较大,营养物质垂向混合剧烈,营养盐垂向分布可能足够蓝藻细胞的营养需要。其次,本研究中水环境采样数据为逐月数据,缺乏水质高频采样数据,用于与蓝藻水华日变化分析其影响可能会被低估。近年来,太湖经历了四阶段的综合治理后,水体富营养化状况逐渐减轻,随着水质状况不断改善未来营养盐可能会成为蓝藻垂向迁移的重要影响因素。
本研究中GOCI影像应用场景较广,除可用于蓝藻水华强度反演外,还可进行总悬浮物浓度TSS(total suspended solid)、可溶性有色有机物质CDOM(color dissolved organic matter)、归一化植被指数反演及营养盐反演等研究[44]。其提供的8 h影像数据,可以用于观测水体中漂浮蓝藻的连续动态变化,能为太湖这种水华时空差异较大、动态变化剧烈的湖泊提供可靠的监测和预警信息。但相比于设置于水表面的陆基高光谱监测仪及无人机监测,GOCI影像受云层覆盖等影响较大,在精度和灵敏度仍存在缺陷。后续研究可通过近地面的光谱监测仪及湖泊营养盐的高频监测,进一步研究浅水湖泊中营养盐对蓝藻垂向迁移的影响。
4 结论利用2015-2020年太湖地区气象、水环境和遥感影像数据,分析了太湖不同湖区蓝藻水华日变化过程,探究了太湖蓝藻垂向迁移引起的水华日变化过程与环境因素的关系。研究发现:太湖蓝藻水华日变化过程主要有3种类型:上升、下降、先上升后下降,沿岸湖区主要发生下降和先上升后下降两种类型,湖心区主要发生上升和先上升后下降两种类型。统计分析和偏最小二乘法结构方程模型(PLS-SEM)结果表明,气象因子是影响太湖蓝藻垂向迁移的关键要素。其中,累积光辐射是蓝藻垂向迁移过程的主要驱动因子;气温升高有利于蓝藻持续维持上浮能力;风速能影响蓝藻垂向迁移,前一天风速较大且当天风速较小会加速蓝藻上浮。相较于沿岸湖区,湖心区受累积光辐射、风速的影响更大,蓝藻水华日变化过程更剧烈。水环境因子对蓝藻垂向迁移过程影响较小,为明确水环境因子的影响后续还需进行高频监测研究。
5 附录附表 Ⅰ见电子版(DOI: 10.18307/2024.0211)。
| 附表 Ⅰ 太湖水环境因子采样点位经纬度信息 Appendix Ⅰ Longitude and latitude information of sampling sites for environmental factors in Lake Taihu |
| [1] |
Huisman J, Codd GA, Paerl HW et al. Cyanobacterial blooms. Nature Reviews Microbiology, 2018, 16(8): 471-483. DOI:10.1038/s41579-018-0040-1 |
| [2] |
Kong FX, Gao G. Hypothes is on cyanobacteria bloom-forming mechanism in large shallow eutrophic lakes. Acta Ecologica Sinica, 2005, 25(3): 589-595. [孔繁翔, 高光. 大型浅水富营养化湖泊中蓝藻水华形成机理的思考. 生态学报, 2005, 25(3): 589-595. DOI:10.3321/j.issn:1000-0933.2005.03.028] |
| [3] |
Ho JC, Michalak AM, Pahlevan N. Widespread global increase in intense lake phytoplankton blooms since the 1980s. Nature, 2019, 574(7780): 667-670. DOI:10.1038/s41586-019-1648-7 |
| [4] |
Wu ZX, Yu GL, Shi JQ et al. The two newly recorded species of bloom-forming cyanobacterial genus Aphanizomenon morr. ex born. et flah. (cyanophyta) from China. Acta Hydrobiologica Sinica, 2009, 33(6): 1140-1144. [吴忠兴, 虞功亮, 施军琼等. 我国淡水水华蓝藻——束丝藻属新记录种. 水生生物学报, 2009, 33(6): 1140-1144. DOI:10.3724/SP.J.0000.2009.61140] |
| [5] |
Zhang YS, Kong FX, Yu Y et al. The characteristics and buoyancy regulations of cyanobacterial gas vesicles. Acta Ecologica Sinica, 2010, 30(18): 5077-5090. [张永生, 孔繁翔, 于洋等. 蓝藻伪空胞的特性及浮力调节机制. 生态学报, 2010, 30(18): 5077-5090.] |
| [6] |
Paerl HW, Huisman J. Blooms like it hot. Science, 2008, 320(5872): 57-58. DOI:10.1126/science.1155398 |
| [7] |
Qin BQ. Shallow lake limnology and control of eutrophication in Lake Taihu. J Lake Sci, 2020, 32(5): 1229-1243. [秦伯强. 浅水湖泊湖沼学与太湖富营养化控制研究. 湖泊科学, 2020, 32(5): 1229-1243. DOI:10.18307/2020.0501] |
| [8] |
Gallon JR, Jones DA, Page TS. Trichodesmium, the paradoxical diazotroph. Archiv für Hydrobiologie, Supplement Volumes, 1996, 83: 215-243. DOI:10.1127/algol_stud/83/1996/215 |
| [9] |
Visser PM, Passarge J, Mur LR. Modelling vertical migration of the cyanobacterium Microcystis. Hydrobiologia, 1997, 349(1): 99-109. DOI:10.1023/A:1003001713560 |
| [10] |
Webster IT, Hutchinson PA. Effect of wind on the distribution of phytoplankton cells in lakes revisited. Limnology and Oceanography, 1994, 39(2): 365-373. DOI:10.4319/lo.1994.39.2.0365 |
| [11] |
Brookes JD, Ganf GG. Variations in the buoyancy response of Microcystis aeruginosa to nitrogen, phosphorus and light. Journal of Plankton Research, 2001, 23(12): 1399-1411. DOI:10.1093/plankt/23.12.1399 |
| [12] |
Zhou B, Bi YH, Hu ZY. Effects of temperature on the buoyancy of Microcystis aeruginosa. China Environmental Science, 2014, 34(7): 1847-1854. [周贝, 毕永红, 胡征宇. 温度对铜绿微囊藻细胞浮力的调控机制. 中国环境科学, 2014, 34(7): 1847-1854.] |
| [13] |
Robarts RD, Zohary T. Temperature effects on photosynthetic capacity, respiration, and growth rates of bloom-forming cyanobacteria. New Zealand Journal of Marine and Freshwater Research, 1987, 21(3): 391-399. DOI:10.1080/00288330.1987.9516235 |
| [14] |
Webster IT. Effect of wind on the distribution of phytoplankton cells in lakes. Limnology and Oceanography, 1990, 35(5): 989-1001. DOI:10.4319/lo.1990.35.5.0989 |
| [15] |
Cao HS, Kong FX, Luo LC et al. Effects of wind and wind-induced waves on vertical phytoplankton distribution and surface blooms of Microcystis aeruginosa in Lake Taihu. Journal of Freshwater Ecology, 2006, 21(2): 231-238. DOI:10.1080/02705060.2006.9664991 |
| [16] |
Konopka A. Metalimnetic cyanobacteria in hard-water lakes: Buoyancy regulation and physiological state. Limnology and Oceanography, 1989, 34(7): 1174-1184. DOI:10.4319/lo.1989.34.7.1174 |
| [17] |
杨波. 蓝藻伪空胞的特征及其浮力对氮、磷和温度的响应机制研究[学位论文]. 长沙: 湖南农业大学, 2007.
|
| [18] |
Ma JR, Brookes JD, Qin BQ et al. Environmental factors controlling colony formation in blooms of the cyanobacteria Microcystis spp. in Lake Taihu, China. Harmful Algae, 2014, 31: 136-142. DOI:10.1016/j.hal.2013.10.016 |
| [19] |
Qin BQ, Yang GJ, Ma JR et al. Spatiotemporal changes of cyanobacterial bloom in large shallow eutrophic Lake Taihu, China. Frontiers in Microbiology, 2018, 9: 451. DOI:10.3389/fmicb.2018.00451 |
| [20] |
Xiao M, Li M, Reynolds CS. Colony formation in the cyanobacterium Microcystis. Biological Reviews of the Cambridge Philosophical Society, 2018, 93(3): 1399-1420. DOI:10.1111/brv.12401 |
| [21] |
Song Y, Song XD, Jiang H. Recent progress in remote sensing of algae in Lake Taihu. Remote Sensing Information, 2008, 23(4): 102-108. [宋瑜, 宋晓东, 江洪. 太湖藻类的遥感监测研究. 遥感信息, 2008, 23(4): 102-108. DOI:10.1016/S1001-0742(08)62079-3] |
| [22] |
Ma RH, Dai JF. Investigation of chlorophyll-a and total suspended matter concentrations using Landsat ETM and field spectral measurement in Lake Taihu, China. International Journal of Remote Sensing, 2005, 26(13): 2779-2795. DOI:10.1080/01431160512331326648 |
| [23] |
Hu CM, Lee ZP, Ma RH et al. Moderate Resolution Imaging Spectroradiometer (MODIS) observations of cyanobacteria blooms in Lake Taihu, China. Journal of Geophysical Research, 2010, 115(C4): C04002. DOI:10.1029/2009jc005511 |
| [24] |
Qi L, Hu CM, Visser PM et al. Diurnal changes of cyanobacteria blooms in Lake Taihu as derived from GOCI observations. Limnology and Oceanography, 2018, 63(4): 1711-1726. DOI:10.1002/lno.10802 |
| [25] |
Wang SQ, Zhang X, Chen NC et al. Classifying diurnal changes of cyanobacterial blooms in Lake Taihu to identify hot patterns, seasons and hotspots based on hourly GOCI observations. Journal of Environmental Management, 2022, 310: 114782. DOI:10.1016/j.jenvman.2022.114782 |
| [26] |
Li JD, Li YM, Bi S et al. Utilization of GOCI data to evaluate the diurnal vertical migration of Microcystis aeruginosa and the underlying driving factors. Journal of Environmental Management, 2022, 310: 114734. DOI:10.1016/j.jenvman.2022.114734 |
| [27] |
王苏民, 窦鸿身. 中国湖泊志. 北京: 科学出版社, 1998.
|
| [28] |
Wu TF, Qin BQ, Ma JR et al. Movement of cyanobacterial colonies in a large, shallow and eutrophic lake: A review. Chinese Science Bulletin, 2019, 64(36): 3833-3843. [吴挺峰, 秦伯强, 马健荣等. 浅水富营养化湖泊中蓝藻群体运动研究述评. 科学通报, 2019, 64(36): 3833-3843. DOI:10.1360/TB-2019-0033] |
| [29] |
Tan X, Kong FX, Zeng QF et al. Seasonal variation of Microcystis in Lake Taihu and its relationships with environmental factors. Journal of Environmental Sciences, 2009, 21(7): 892-899. DOI:10.1016/S1001-0742(08)62359-1 |
| [30] |
Zhang YS, Li HY, Kong FX et al. Role of conony intercellular space in the cyanobacteria bloom-forming. Environmental Science, 2011, 32(6): 1602-1607. [张永生, 李海英, 孔繁翔等. 群体细胞间空隙在微囊藻水华形成过程中的浮力调节作用. 环境科学, 2011, 32(6): 1602-1607. DOI:10.13227/j.hjkx.2011.06.002] |
| [31] |
Shi K, Zhang YL, Zhang YB et al. Understanding the long-term trend of particulate phosphorus in a cyanobacteria-dominated lake using MODIS-Aqua observations. Science of the Total Environment, 2020, 737: 139736. DOI:10.1016/j.scitotenv.2020.139736 |
| [32] |
Hu CM, Feng L, Lee ZP. Evaluation of GOCI sensitivity for At-Sensor radiance and GDPS-Retrieved chlorophyll-a products. Ocean Science Journal, 2012, 47(3): 279-285. DOI:10.1007/s12601-012-0028-0 |
| [33] |
Joseph FH, Jeffrey JR, Marko S et al. When to use and how to report the results of PLS-SEM. European Business Review, 2019, 31(1). DOI:10.1108/EBR-11-2018-0203 |
| [34] |
Wu TF, Qin BQ, Brookes JD et al. The influence of changes in wind patterns on the areal extension of surface cyanobacterial blooms in a large shallow lake in China. Science of the Total Environment, 2015, 518/519: 24-30. DOI:10.1016/j.scitotenv.2015.02.090 |
| [35] |
Li JD, Li YM, Lv H et al. Vertical distribution characteristics of cyanobacteria and its dynamic mechanism in shallow eutrophic lakes: A case of Lake Taihu. Acta Scientiae Circumstantiae, 2022, 42(7): 318-328. [李俊达, 李云梅, 吕恒等. 浅水富营养化湖泊蓝藻垂向分布特征及其动力机制研究——以太湖为例. 环境科学学报, 2022, 42(7): 318-328. DOI:10.13671/j.hjkxxb.2021.0464] |
| [36] |
Wang C, Feng T, Wang PF et al. Understanding the transport feature of bloom-forming Microcystis in a large shallow lake: A new combined hydrodynamic and spatially explicit agent-based modelling approach. Ecological Modelling, 2017, 343: 25-38. DOI:10.1016/j.ecolmodel.2016.10.017 |
| [37] |
Chen H, Zhu Y, Zhang Y et al. Cyanobacterial bloom expansion caused by typhoon disturbance in Lake Taihu China. Environmental Science and Pollution Research, 2020, 27: 42294-42303. DOI:10.1007/s11356-020-09292-0 |
| [38] |
Chen HM, Zhu YY, Zhang Y et al. Cyanobacterial bloom expansion caused by typhoon disturbance in Lake Taihu China. Environmental Science and Pollution Research International, 2020, 27(34): 42294-42303. DOI:10.1007/s11356-020-09292-0 |
| [39] |
Zhang YL, Qin BQ, Chen WM et al. Distribution, seasonal variation and correlation analysis of the transparency in Lake Taihu. Transactions of Oceanology and Limnology, 2003(2): 30-36. [张运林, 秦伯强, 陈伟民等. 太湖水体透明度的分析、变化及相关分析. 海洋湖沼通报, 2003(2): 30-36. DOI:10.3969/j.issn.1003-6482.2003.02.005] |
| [40] |
You JQ, Mallery K, Hong JR et al. Temperature effects on growth and buoyancy of Microcystis aeruginosa. Journal of Plankton Research, 2018, 40(1): 16-28. DOI:10.1093/plankt/fbx059 |
| [41] |
Wallace BB, Hamilton DP. The effect of variations in irradiance on buoyancy regulation in Microcystis aeruginosa. Limnology and Oceanography, 1999, 44: 273-281. DOI:10.4319/lo.1999.44.2.0273 |
| [42] |
Song KS, Fang C, Jacinthe PA et al. Climatic versus anthropogenic controls of decadal trends (1983-2017) in algal blooms in lakes and reservoirs across China. Environmental Science & Technology, 2021, 55(5): 2929-2938. DOI:10.1021/acs.est.0c06480 |
| [43] |
Qin BQ, Zhou J, Elser JJ et al. Water depth underpins the relative roles and fates of nitrogen and phosphorus in lakes. Environmental Science & Technology, 2020, 54(6): 3191-3198. DOI:10.1021/acs.est.9b05858 |
| [44] |
Li GN, Wang L, Wang X et al. Geostationary Ocean color imager and application progress. Marine Environmental Science, 2014, 33(6): 966-971. [李冠男, 王林, 王祥等. 静止水色卫星GOCI及其应用进展. 海洋环境科学, 2014, 33(6): 966-971.] |
 2024, Vol. 36
2024, Vol. 36 

