(2: 成都理工大学地质灾害防治与地质环境保护国家重点实验室, 成都 610059)
(3: 成都理工大学水土污染协同控制与联合修复国家环境保护重点实验室, 成都 610059)
(4: 四川万豪企业管理咨询有限公司, 成都 610023)
(5: 成都市兴蓉再生能源有限公司, 成都 610100)
(6: 四川省生态环境科学研究院, 成都 610041)
(2: State Key Laboratory of Geohazard Prevention and Geoenvironment Protection, Chengdu University of Technology, Chengdu 610059, P.R.China)
(3: State Environmental Protection Key Laboratory of Synergetic Control and Joint Remediation for Soil & Water Pollution, Chengdu University of Technology, Chengdu 610059, P.R.China)
(4: SiChuan Wanhao Consulting Co., LTD., Chengdu 610023, P.R.China)
(5: Chengdu Xingrong Renewable Energy Co., LTD., Chengdu 610100, P.R.China)
(6: Sichuan Academy of Eco-Environmental Sciences, Chengdu 610041, P.R.China)
地下水NO3-污染是一个普遍存在的环境问题,尤其在农业活动密集的地区。我国作为农业大国,大规模地使用氮肥和高水量的灌溉需求导致农业流域地下水NO3-污染较为严重[1-3]。地下水是重要水资源,长期饮用含有高浓度NO3-的地下水会增加人体患高铁血红蛋白症和多发性硬化症等疾病的风险[2]。基于人类健康考虑,世界卫生组织(WHO)将饮用水中NO3--N的最大允许限量定为10 mg/L[4]。针对地下水中NO3-对人体健康产生的影响,国际常用人类健康风险评价(HHRA)方法来评估地下水中NO3-对不同年龄段人群接触NO3-而产生的潜在健康风险[5-6]。此外,地表水和地下水之间普遍存在交互作用[7-8],地下水中的NO3-可以通过频繁的交互作用进入到周边地表水体,是地表水中NO3-的一个潜在的重要来源。因此,准确识别地下水NO3-来源对地下水和地表水中NO3-的污染防治具有重要意义。
地下水中NO3-来源十分广泛,主要包括大气降水、粪肥/生活污水、化肥和土壤有机氮等[3]。传统的水质图解法[9]和水质定量解析法[10]难以准确识别水体中NO3-的来源。大量的研究表明,氮氧同位素(δ15N-NO3-和δ18O-NO3-)示踪技术能有效识别地下水和地表水中NO3-来源[11-12]。此外,确定不同NO3-来源的贡献率对地下水NO3-的综合防治具有重要的意义。当前,质量平衡模型、IsoSource模型、SIAR模型和MixSIAR(Bayesian Mixing Models in R)模型被用于确定不同NO3-来源的贡献率[13-14]。其中,SIAR模型因其精度高,且能同时考虑多种来源及同位素分馏效应而被广泛应用[11-13]。
水库是重要的地表水资源,在防洪、供水和能源等方面发挥重要作用。据2022年《中国生态环境状况公报》统计数据显示,在开展营养状况监测的204个重要湖泊(水库)中,轻度和中度富营养化状态湖泊(水库)分别占24.0%和5.9%[15]。为遏制水库富营养化发展,国家加强了外源控制,但水库富营养化现象仍时有发生,推测可能与地下水与地表水交互作用有关。地下水中NO3-进入到水库,导致水库中NO3-浓度增加,进而引发富营养化[16]。我国共建有各类水库9.8万余座,其中中小型水库占比超过95%[17],然而大部分研究主要集中于大型水库,对中小型水库关注较少。众多的中小型水库在抵御洪旱灾害、保障饮用水供给、维护生态环境等方面发挥着巨大作用。因此,研究中小型水库流域周边地下水NO3-的来源及不同来源的贡献率,为地下水和水库中NO3-污染防治及水资源管理具有重要意义。
本研究拟以四川省内江市黄河镇水库周边地下水为研究对象,主要研究内容为:(1)确定丰、枯水期水库水和地下水中NO3-的污染现状;(2)利用HHRA法对地下水中NO3-引起的潜在健康风险进行评估;(3)利用多种稳定同位素(δD-H2O和δ18O-H2O,δ15N-NO3-和δ18O-NO3-)识别水库水和地下水中NO3-的来源和主要生物地球化学过程;(4)运用SIAR模型定量评估各来源对地下水NO3-的贡献率。
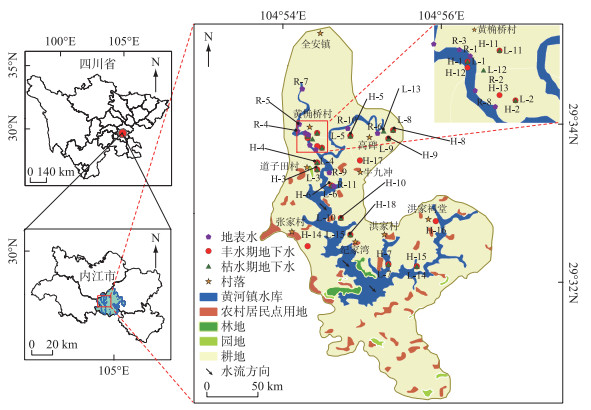
1 材料与方法 1.1 研究区域内江是四川省粮食和经济作物的集中产区,为满足农业灌溉、生活用水等方面的需求,先后修建了大量水库。黄河镇水库作为其中的一个中型水库,不仅是当地农业生产活动的重要支撑,同时也是内江城区及库区周边居民的重要水源,其水体质量至关重要。黄河镇水库(29°31′~29°35′N, 104°54′~104°56′E)(图 1),于1960年建成,其最大容量为1450万m3,其形状狭长且流域内耕地占比大(62.8%),属于农业河流型水库。
|
图 1 黄河镇水库流域地下水采样点分布 Fig.1 Distribution of groundwater sampling points in Huanghezhen Reservoir Basin |
研究区气候属于亚热带湿润季风气候,年平均降水量906 mm,约60%的降水发生在6-9月。区内地下水类型主要包括松散沉积物孔隙水和基岩裂隙水。孔隙水主要分布在沱江Ⅰ级阶地上,厚度为0~2 m,由第四系冲积层淤泥质黏土、砂卵石组成。基岩裂隙水广泛分布于全市,含水层厚度不同,由砂岩和泥岩互层组成,含水层渗透性均较好。地下水水位埋深浅,属于浅层地下水。水文地质调查表明,地下水与地表水之间存在着很强的水力联系[18]。
1.2 样品采集与测试方法利用经纬度网格法对黄河镇水库均匀布点,并结合水库流域特征及土地利用情况,分别于2019年8月(丰水期)和2019年12月(枯水期)采集了33个地下水样品(丰水期18个,枯水期15个)和20个水库水样品(丰水期11个,枯水期9个)。现场使用便携式多参数水质测定仪(HI98194 HANNA)测定水温(T)、pH、溶解氧(DO)、电导率(EC)、氧化还原电位(ORP)、总溶解固体(TDS)等指标。水样采集后,利用0.45 μm滤膜过滤并储存在100 mL的聚四氟乙烯采样瓶中(原水样润洗3遍),置于2~4℃条件下冷藏保存并运送实验室进行分析测试。
NO3--N和NO2--N浓度采用离子色谱法(IC-2100, Dionex)测定,检测限为0.01 mg/L。NH3-N浓度采用纳氏试剂分光光度法(HJ 535-2009)测定。δ15N-NO3-和δ18O-NO3-采用反硝化细菌法[19]进行测定,δ15N-NO3-的平均精度为±0.25‰,δ18O-NO3-的平均精度为±0.50‰。
1.3 人类健康风险评估人体主要通过两种方式接触NO3-:口服摄入和皮肤吸收,其中口服摄入是主要的接触途径。本研究采用美国环境保护署(USEPA)推荐的HHRA模型对地下水中NO3-的潜在人类健康风险进行评价。健康风险评价计算公式如下:
| $ \text { 慢性每日摄入量 }(C D I)=\frac{C \cdot I R \cdot E D \cdot E F}{B W \cdot A T} $ | (1) |
式中,CDI表示单位重量通过摄入途径的每日平均暴露剂量(mg/(kg·d));C为污染物浓度(mg/L);IR为摄入量(L/d;婴儿为0.7,儿童为0.78,青少年为2,成人为2.5);ED为暴露持续时间(a;婴儿为1.5,儿童为4,青少年为13,成人为40);EF为暴露频率(d/a;通常为365);BW为平均体重(kg;婴儿为7.5,儿童为50,青少年为50,成人为78);AT为平均时间(d;按ED×365 d/a计算)[5-6]。
| $ \text { 风险系数 }(H Q)=\frac{C D I}{R f D} $ | (2) |
式中,HQ为风险系数,当HQ>1时,地下水NO3-对人体产生的非致癌风险超过可接受的水平[6];RfD为参考剂量(mg/(kg·d),参考美国环境保护署设为1.6)[20]。
1.4 基于SIAR模型的不同来源硝酸盐贡献率计算贝叶斯同位素混合模型(SIAR)是由Parnell等[21]开发的一个基于R统计软件的稳定同位素混合模型,可以得出不同NO3-来源贡献率的最优概率分布。SIAR模型表示如下:
| $ X_{i j}=\sum\limits_{k=1}^K p_k\left(S_{j k}+C_{j k}\right)+\varepsilon_{i j} $ | (3) |
| $ S_{j k}-N\left(\mu_{j k}, \omega_{j k}^2\right) $ | (4) |
| $ C_{j k}-N\left(\lambda_{j k}, \tau_{j k}^2\right) $ | (5) |
| $ \varepsilon_{i j}-N\left(0, \sigma_j^2\right) $ | (6) |
式中,Xij是混合样i中同位素j的值(i=1,2,3, …, N;j=1,2,3, …, J);pk为NO3-源k的贡献率(k=1, 2, 3, …, K);Sjk是NO3-源k中同位素j的值,服从平均值为μjk、标准差为ωjk的正态分布;Cjk是NO3-源k中同位素j的分馏系数,服从平均值为λjk、标准差为τjk的正态分布;εij是残差,表示不同样品之间未能确定的变量,服从平均值为0、标准差为σj的正态分布。
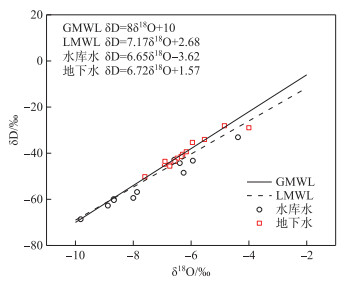
2 结果和讨论 2.1 地下水和水库水的氢氧同位素特征研究区水库水的δD-H2O和δ18O-H2O范围分别为-68.61‰~-25.26‰和-9.82‰~-3.43‰。地下水的δD-H2O值范围为-50.20‰~-28.08‰,平均值为-40.19‰;δ18O-H2O值范围为-7.60‰~-4.00‰,平均值为-6.22‰。通过对比分析水库水、地下水、全球大气降水线(GMWL)和四川大气降水线(LMWL)[22-23],得出大气降水是研究区水库水和地下水的主要来源(图 2)。结合含水层的高渗透性和地下水的埋藏深度,以及地下水(6.72)和水库水(6.65)的氢氧同位素比值斜率相似,推测水库水和地下水之间存在着水力交换(混合)[5]。因此,地下水中高浓度的NO3-可能对水库水产生潜在的影响。
|
图 2 黄河镇水库流域δD-H2O与δ18O-H2O关系图 Fig.2 Relationship between δD-H2O and δ18O-H2O in Huanghezhen Reservoir Basin |
研究区丰、枯水期地下水与水库水的水化学参数见附表 Ⅰ。丰、枯水期地下水和水库水均呈中性偏弱碱性。地下水的TDS值分别为231~753 mg/L(丰水期)和62~646 mg/L(枯水期),水库水的TDS值范围分别为105~429 mg/L(丰水期)和203~362 mg/L(枯水期)。丰水期地下水和水库水DO浓度分别为0~5.60和3.01~5.40 mg/L,枯水期DO浓度分别为3.03~4.89和3.52~5.10 mg/L,表明研究区地下水和水库水整体上处于有氧环境。
丰水期地下水NO3--N浓度为1.24~42.91 mg/L,平均值为18.56 mg/L,其中61%的样品超过WHO规定饮用水标准限值(10 mg/L)。相比之下,水库水NO3--N浓度较低,为0~44.65 mg/L,平均值为7.33 mg/L,超标率为18%。枯水期地下水NO3--N值为0~42.96 mg/L,平均值为11.12 mg/L,超标率为40%。水库水NO3--N值为0~0.35 mg/L。丰水期地下水中NH3-N浓度为0.12~0.88 mg/L,平均值为0.41 mg/L。33.3%的地下水样品超过生活饮用水卫生标准(0.5 mg/L,GB 5749-2006)。水库水中NH3-N浓度为0.26~1.84 mg/L,平均值为0.97 mg/L,超标率高达91%。枯水期地下水和水库水中NH3-N浓度分别为0.40~1.38和0.62~17.57 mg/L,超标率高达80%和100%。大多数样品的NO2--N浓度低于检出限。因此,NO3--N是研究区地下水中氮的主要存在形式。
结合图 1可知,丰、枯水期地下水中高浓度NO3-主要集中在黄河镇水库上部地区(黄桷桥村和高碑附近),该区域村镇密集且分布着大量耕地。野外调查发现,研究区居民的生活污水处理设施不完善,大部分生活污染废水是直接排放到水库中。此外,研究区农业活动频繁,导致大量未被作物吸收的氮素在降雨和灌溉的作用下进入水体中。这些都可能是地下水中高浓度NO3-的潜在来源。
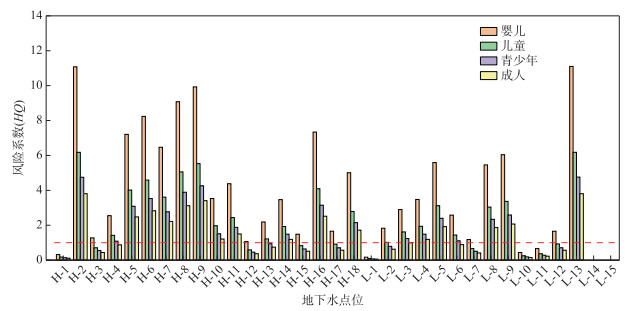
2.3 地下水硝酸盐健康风险评估本研究主要计算地下水中NO3-潜在的人类健康风险。结果表明(图 3),丰水期,婴儿、儿童、青少年和成人的HQ范围分别为0.32~11.08、0.18~6.18、0.14~4.75和0.11~3.81。94%、72%、67%和61%的婴儿、儿童、青少年和成人的HQ值超过了可接受水平(HQ>1)。枯水期时婴儿、儿童、青少年和成人的HQ值范围分别为0~11.10、0~6.18、0~4.76和0~3.81。67%、53%、47%和40%的婴儿、儿童、青少年和成人的HQ值超过了可接受水平(HQ>1)。若长期饮用该区地下水,有患高铁血红蛋白症、多发性硬化症等疾病的风险[2]。
|
图 3 丰、枯水期地下水中硝酸盐对各年龄段人群的风险系数(H-丰水期;L-枯水期) Fig.3 Risk factors of nitrate in groundwater for various age groups during the high and low water periods(H-high water periods; L-low water periods) |
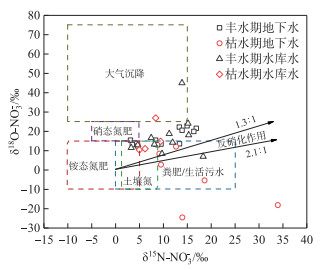
由图 4可知,研究区大部分地下水和水库水样品的δ15N-NO3-与δ18O-NO3-值落在粪肥/生活污水的范围内[24],表明粪肥/生活污水是地下水NO3-污染的主要来源。部分水样的δ18O-NO3-值位于粪肥/生活污水、铵态氮肥、土壤有机氮和大气降水之间,结合研究区地下水和水库水主要来自大气降水,推测大气降水可能是这部分水样中NO3-的重要来源[25]。枯水期部分地下水水样的δ18O-NO3-值较低,这可能是由于枯水期高浓度的NH4+为硝化作用提供更多的反应底物,促使更多的δ18O-H2O被硝化细菌利用进入到NO3-中,致使NO3-中δ18O值偏低[26]。
|
图 4 研究区地下水与水库水δ15N-NO3-与δ18O-NO3-关系图 Fig.4 Relationship between δ15N-NO3- and δ18O-NO3- in groundwater and reservoir water of the study area |
地下水中δ15N-NO3-和δ18O-NO3-的组成不仅与其来源密切相关,还受氮的生物地球化学过程的影响。氮的生物地球化学过程主要包括反硝化作用、硝化作用、氨挥发作用等[9]。反硝化是氮循环的关键过程之一,当水中DO浓度较低(<2.0 mg/L)时,容易发生反硝化[11]。研究区地下水DO平均浓度为3.67 mg/L,不利于反硝化作用发生。另一方面,微生物的反硝化作用会使水体中δ15N-NO3-和δ18O-NO3-的值升高,水体中NO3-浓度降低,δ15N-NO3-和δ18O-NO3-的比值接近1.3 ~2.1[10]。研究区丰、枯水期采样点中δ15N-NO3-和δ18O-NO3-的比值(0.64和-0.92)不在典型的反硝化比率范围内,因此,推测反硝化不是研究区地下水中氮循环的主要过程。氮循环的另外一个关键过程是硝化作用,可以利用δ18O-NO3-的值判别是否发生硝化作用,其范围为-10‰~15‰[27]。研究区63%的地下水水样的δ18O-NO3-值均在此范围内,表明地下水中氮的关键过程可能是硝化作用。硝化过程的发生会加剧地下水中NO3-污染。此外,研究区农业生产中主要使用的尿素和氨肥,在一定温度和pH条件下会发生氨挥发作用,NH3可以通过大气干、湿沉降返回陆地和水体,可能是研究区地下水和地表水NH4+的重要来源[28]。
2.5 地下水硝酸盐污染贡献比计算根据前文分析,将土壤有机氮、大气沉降、粪肥/生活污水和化肥的初始同位素特征值和方差代入SIAR模型中[29-31],得出不同NO3-来源对研究区地下水NO3-的贡献比例。由于地下水中的反硝化作用不明显,将Cjk设为0[32]。
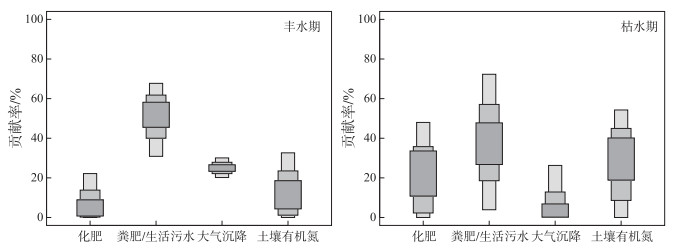
由图 5可知,无论是丰水期还是枯水期,粪肥/生活污水都是地下水NO3-的主要来源。丰水期NO3--N的主要来源表现为粪肥/生活污水(50%)>大气沉降(25%)>土壤有机氮(15%)>化肥(10%),枯水期表现为粪肥/生活污水(38%)>土壤有机氮(29%)>化肥(24%)>大气沉降(9%)。实地调查发现,研究区居民的污水排放设施尚不完善,家禽养殖废水和生活污水均未经处理排放。丰水期大气沉降中NO3-的贡献率较枯水期显著增加,与丰水期丰沛的降雨有关[33]。而化肥贡献率较低,可能与氨挥发有关。丰水期温度较高,加速了土壤中铵态氮肥的挥发,进而减少通过淋滤作用进入地下水中NH4+浓度[34]。丰水期土壤有机氮的贡献率小于枯水期,可能是丰水期的气候条件以及田间管理措施(施肥等)有利于土壤有机氮的矿化作用,促使有机氮在微生物作用下转化为无机氮,被植物或微生物吸收利用[8]。
|
图 5 丰、枯水期地下水各个污染来源的贡献率 Fig.5 Contribution of each source of groundwater pollution in high and low water periods |
研究区丰、枯水期地下水中NO3--N浓度范围分别为1.24~42.91和0~42.96 mg/L,其中丰水期地下水NO3--N超标率为61%,枯水期地下水NO3--N超标率为40%。健康风险评估结果表明,地下水中NO3-对不同人群的健康存在潜在风险。通过分析δ15N-NO3-和δ18O-NO3-发现,研究区地下水中NO3-的主要来源为粪肥/生活污水。硝化作用可能是研究区氮循环的一个重要过程。SIAR模型表明,丰水期NO3-来源(土壤有机氮、大气沉降、粪肥/生活污水和化肥)的贡献率分别为15%、25%、50%和10%,枯水期各来源的贡献率分别为29%、9%、38%、24%。无论是丰水期还是枯水期,粪肥/生活污水都是地下水NO3-的主要来源。为减轻NO3-污染及保护周边居民饮水安全,应将生活污水治理与农村改厕衔接,建立厕所粪污资源化利用体系,避免污水直排。另一方面,提高畜禽粪污资源化利用,推动畜禽粪肥就近还田利用等。
4 附录附表 Ⅰ见电子版(DOI: 10.18307/2024.0427)。
| 附表Ⅰ 研究区丰枯水期地下水与水库水水化学参数 Appendix Ⅰ Hydrochemical parameters of groundwater and reservoir water during the high and low water periods in the study area |
| [1] |
Kim HR, Yu S, Oh J et al. Nitrate contamination and subsequent hydrogeochemical processes of shallow groundwater in agro-livestock farming districts in South Korea. Agriculture, Ecosystems & Environment, 2019, 273: 50-61. DOI:10.1016/j.agee.2018.12.010 |
| [2] |
Sadler R, Maetam B, Edokpolo B et al. Health risk assessment for exposure to nitrate in drinking water from village wells in Semarang, Indonesia. Environmental Pollution, 2016, 216: 738-745. DOI:10.1016/j.envpol.2016.06.041 |
| [3] |
Shang X, Huang H, Mei K et al. Riverine nitrate source apportionment using dual stable isotopes in a drinking water source watershed of southeast China. Science of the Total Environment, 2020, 724: 137975. DOI:10.1016/j.scitotenv.2020.137975 |
| [4] |
Sayato Y. WHO guidelines for drinking-water quality. Eisei Kagaku, 1989, 35(5): 307-312. DOI:10.1248/jhs1956.35.307 |
| [5] |
USEPA. Supplemental Guidance for Developing Soil Screening Levels for Superfund Sites Peer Review Draf, 2001.
|
| [6] |
Bazeli J, Ghalehaskar S, Morovati M et al. Health risk assessment techniques to evaluate non-carcinogenic human health risk due to fluoride, nitrite and nitrate using Monte Carlo simulation and sensitivity analysis in Groundwater of Khaf County, Iran. International Journal of Environmental Analytical Chemistry, 2022, 102(8): 1793-1813. DOI:10.1080/03067319.2020.1743280 |
| [7] |
Zhang QQ, Wang HW, Liu L et al. Multiple isotopes reveal the driving mechanism of high NO3- level and key processes of nitrogen cycling in the lower reaches of Yellow River. Journal of Environmental Sciences, 2024, 138: 597-606. DOI:10.1016/j.jes.2023.05.001 |
| [8] |
Jimenez-Fernandez O, Schwientek M, Osenbrück K et al. Groundwater-surface water exchange as key control for instream and groundwater nitrate concentrations along a first-order agricultural stream. Hydrological Processes, 2022, 36(2): e14507. DOI:10.1002/hyp.14507 |
| [9] |
Wang SQ, Zheng WB, Currell M et al. Relationship between land-use and sources and fate of nitrate in groundwater in a typical recharge area of the North China Plain. Science of the Total Environment, 2017, 609: 607-620. DOI:10.1016/j.scitotenv.2017.07.176 |
| [10] |
Liang X, Sun LQ, Zhang X et al. Mechanism of inorganic nitrogen transformation and identification of nitrogen sources in water and soil. Environmental Science, 2020, 41(9): 4333-4344. [梁杏, 孙立群, 张鑫等. 无机态氮素转化机制及水土体氮源识别方法. 环境科学, 2020, 41(9): 4333-4344. DOI:10.13227/j.hjkx.202001047] |
| [11] |
Kou XY, Ding JJ, Li YZ et al. Tracing nitrate sources in the groundwater of an intensive agricultural region. Agricultural Water Management, 2021, 250: 106826. DOI:10.1016/j.agwat.2021.106826 |
| [12] |
Hu MP, Liu YM, Zhang YF et al. Coupling stable isotopes and water chemistry to assess the role of hydrological and biogeochemical processes on riverine nitrogen sources. Water Research, 2019, 150: 418-430. DOI:10.1016/j.watres.2018.11.082 |
| [13] |
Jin ZX, Wang JF, Chen JG et al. Identifying the sources of nitrate in a small watershed using δ15N-δ18O isotopes of nitrate in the Kelan Reservoir, Guangxi, China. Agriculture, Ecosystems & Environment, 2020, 297: 106936. DOI:10.1016/j.agee.2020.106936 |
| [14] |
Saka D, Adu-Gyamfi J, Skrzypek G et al. Disentangling nitrate pollution sources and apportionment in a tropical agricultural ecosystem using a multi-stable isotope model. Environmental Pollution, 2023, 328: 121589. DOI:10.1016/j.envpol.2023.121589 |
| [15] |
中华人民共和国国家统计局. 中国统计年鉴. 北京: 中国统计出版社, 2019.
|
| [16] |
Le F, Li RF, Ruan XH et al. Isotopic tracing of nitrogen source and interaction between surface water and groundwater of a small valley plain in the Zhangxi watershed. Applied Geochemistry, 2023, 151: 105615. DOI:10.1016/j.apgeochem.2023.105615 |
| [17] |
中华人民共和国生态环境部. 中国生态环境状况公报, 2022.
|
| [18] |
李佑才. 内江幅H-48-22 1/20万区域水文地质报告. 四川: 四川省地质局水文工程大队, 1977.
|
| [19] |
Kendall C, Elliott EM, Wankel SD. Tracing anthropogenic inputs of nitrogen to ecosystems. In: Michener R, Lajtha K eds. Stable Isotopes in Ecology and Environmental Science. Oxford: Blackwell Publishing Ltd, 2007: 375-449. DOI: 10.1002/9780470691854.ch12.
|
| [20] |
USEPA. Integrated risk information system (IRIS), 2013.
|
| [21] |
Parnell AC, Inger R, Bearhop S et al. Source partitioning using stable isotopes: Coping with too much variation. PLoS One, 2010, 5(3): e9672. DOI:10.1371/journal.pone.0009672 |
| [22] |
Craig H. Isotopic variations in meteoric waters. Science, 1961, 133(3465): 1702-1703. DOI:10.1126/science.133.3465.1702 |
| [23] |
Li WJ, Wang JL, Wang JL. Characteristics of the stable isotopes in precipitation and the source of water vapor in different terrain in the Southwest Region. Resources and Environment in the Yangtze Basin, 2018, 27(5): 1132-1142. [李维杰, 王建力, 王家录. 西南地区不同地形降水稳定同位素特征及其水汽来源. 长江流域资源与环境, 2018, 27(5): 1132-1142. DOI:10.11870/cjlyzyyhj201805020] |
| [24] |
Xue DM, Botte J, De Baets B et al. Present limitations and future prospects of stable isotope methods for nitrate source identification in surface- and groundwater. Water Research, 2009, 43(5): 1159-1170. DOI:10.1016/j.watres.2008.12.048 |
| [25] |
Li LX, Li YL, Yang ZR et al. Quantitative analysis and seasonal differences of nitrate sources in upper reaches of Qin River. Research of Environmental Sciences, 2021, 34(11): 2636-2644. [李林霞, 李艳利, 杨梓睿等. 沁河上游硝酸盐的定量源解析及其季节性差异. 环境科学研究, 2021, 34(11): 2636-2644.] |
| [26] |
Ren K, Pan XD, Peng C et al. Identification of nitrate sources of groundwaters in the Zhaotong Basin using hydrochemistry, nitrogen and oxygen isotopes and its impact on the environment. Geology in China, 2022, 49(2): 409-419. [任坤, 潘晓东, 彭聪等. 氮氧同位素和水化学解析昭通盆地地下水硝酸盐来源及对环境的影响. 中国地质, 2022, 49(2): 409-419. DOI:10.12029/gc20220205] |
| [27] |
Zhang HD, Kang XR, Wang XM et al. Quantitative identification of nitrate sources in the surface runoff of three dominant forest types in subtropical China based on Bayesian model. Science of the Total Environment, 2020, 703: 135074. DOI:10.1016/j.scitotenv.2019.135074 |
| [28] |
Liu BS, Huang LH, Huang JX et al. Research progress toward and emission reduction measures of ammonia volatilization from farmlands in China. Chinese Journal of Eco-Agriculture, 2022, 30(6): 875-888. [刘伯顺, 黄立华, 黄金鑫等. 我国农田氨挥发研究进展与减排对策. 中国生态农业学报, 2022, 30(6): 875-888. DOI:10.12357/cjea.20210820] |
| [29] |
Jin ZF, Zheng Q, Zhu CY et al. Contribution of nitrate sources in surface water in multiple land use areas by combining isotopes and a Bayesian isotope mixing model. Applied Geochemistry, 2018, 93: 10-19. DOI:10.1016/j.apgeochem.2018.03.014 |
| [30] |
Liu CQ, Li SL, Lang YC et al. Using delta 15N- and delta 18O-values to identify nitrate sources in Karst ground water, Guiyang, southwest China. Environmental Science & Technology, 2006, 40(22): 6928-6933. DOI:10.1021/es0610129 |
| [31] |
Yang LP, Han JP, Xue JL et al. Nitrate source apportionment in a subtropical watershed using Bayesian model. Science of the Total Environment, 2013, 463/464: 340-347. DOI:10.1016/j.scitotenv.2013.06.021 |
| [32] |
Nyilitya B, Mureithi S, Bauters M et al. Nitrate source apportionment in the complex Nyando tropical river basin in Kenya. Journal of Hydrology, 2021, 594(12): 125926. DOI:10.1016/j.jhydrol.2020.125926 |
| [33] |
Wang J, Ye Y, Wang YQ et al. Using δ15N and δ18O values to identify sources of nitrate in the Dianbu River in the Chaohu Lake Basin. Journal of Hydraulic Engineering, 2017, 48(10): 1195-1205. [王静, 叶寅, 王允青等. 利用氮氧同位素示踪技术解析巢湖支流店埠河硝酸盐污染源. 水利学报, 2017, 48(10): 1195-1205.] |
| [34] |
Chen ZX, Liu HQ, Liu G et al. Tracing nitrogen sources and cycle in freshwater system using nitrogen and oxygen isotopic values in nitrate. Environmental Chemistry, 2012, 31(12): 1855-1864. [陈自祥, 柳后起, 刘广等. 淡水水体中氮污染源的识别——利用硝酸根中氮和氧同位素组成. 环境化学, 2012, 31(12): 1855-1864.] |
 2024, Vol. 36
2024, Vol. 36 


